硫化氢 知识点题库
下列物质在一定条件下与碳作用所产生的无色气体能与H2S反应的是( )
A . 二氧化硅
B . 浓硫酸
C . 浓硝酸
D . 水
下列实验中没有硫生成的是( )
A . H2S气体受热分解
B . 氢硫酸中滴入少量氯水
C . SO2气体中通入H2S气体
D . 在足量氧气里充分燃烧H2S气体
在①H2S②SO2③CO④Cl2⑤HI⑥CO2六种气体中,符合下列要求的是:(填序号)
(1)属于酸性氧化物的是 ;
(2)能使品红溶液褪色的是 ;
(3)通入石蕊试液先变红后褪色的是 ;
(4)能使湿润淀粉碘化钾试纸变蓝的是 ;
(5)能与Br2水反应的是
天然气中的H2S杂质常用氨水吸收,产物为NH4HS.一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:
合成氨是人类科学技术上的一项重大突破,其反应原理为:N2(g)+3H2(g)⇌2NH3(g),一种工业合成氨,进而合成尿素的简易流程图如下:
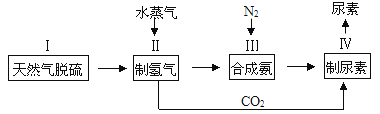
-
(1) 天然气中的H2S杂质常用氨水吸收,产物为NH4HS,一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式为
-
(2) CO2和H2在高温、高压、催化剂条件下可合成CH3CH2OH,反应的化学方程式 .氨是一种潜在的清洁能源,可用作碱性燃料电池的燃料.电池的总反应为:4NH3(g)+3O2(g)═2N2(g)+6H2O(g)则该燃料电池的负极反应式是
-
(3)
已知尿素的结构简式为
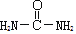 ,请写出尿素的同分异构体中含有离子键的化学式
,请写出尿素的同分异构体中含有离子键的化学式
2006年8月下旬科特迪瓦的“毒垃圾”事件造成了严重的环境污染.这些毒垃圾在雨水的浸泡下,散发出类似臭鸡蛋的刺鼻气味,并随雨水流到河流和地下.
-
(1) 据当地科研人员说具有类似臭鸡蛋气味的气体可能就是H2S和溴(化学式为Br2 , 其性质与氯气相似),如果用CaS表示这些污染物中的硫化物,其与水反应的化学方程式为
-
(2) 产生的溴可能是酸性环境中溴Br﹣和BrO3﹣发生化学反应而形成,其反应的离子方程式为
-
(3) 要消除这些污染物可用 (填试剂的化学式或分子式)溶液来处理.
根据所学知识完成下面题目:
-
(1) H2S分子中H﹣S键的键角为92°,说明H2S分子是(选填“极性”“非极性”)分子.可用FeS与稀硫酸制取 H2S气体,而CuS不溶于稀硫酸,请据此比较FeS、H2S、CuS这三种物质电离或溶解出S2﹣的能力.实验室制取并收集H2S气体,除FeS和稀硫酸外,还必需的试剂是.
-
(2) 在NaOH和NaClO混合溶液中,多硫化钠(Na2SX)会被氧化为Na2SO4 , 此时1molNa2SX失去的电子数为 mol;若Na2SX与NaClO反应的物质的量之比为1:10,则x=.
-
(3) 往Na2S和Na2S2O3混合溶液中加入稀硫酸,指出反应现象.
-
(4) 已知25℃:H2S Ki1=9.1×10﹣8 Ki2=1.1×10﹣12;H2SO3 Ki1=1.5×10﹣2 Ki2=1.0×10﹣7将amolSO2通入含bmolNa2S的溶液中完全反应,若没有硫化氢气体产生,则a:b的值为.
已知X、Y、Z、W(含同一元素)有如下所示转化关系,且X能与W发生反应生成一种易溶于水的盐,则X可能是( )
![]() .
.
A . N2
B . H2S
C . NH3
D . CH4
阅读下列信息:
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
|
元素性质 |
元素编号 |
|||||
|
① |
② |
③ |
④ |
⑤ |
⑥ |
|
|
氢化物沸点(℃) |
-33.4 |
100 |
19.54 |
-87.7 |
-60.7 |
-84.9 |
|
主要化合价 |
+5 -3 |
-2 |
-1 |
+5 -3 |
+6 -2 |
+7 -1 |
A,B,C均为上表中的元素;
Ⅱ.A与B可形成化合物A
B、AB2 , AB2与水反应生成强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3 , CB3与水反应生成强酸乙。
请回答:
-
(1) 表中两种同族元素的氢化物所含电子数相同,这两种氢化物之间能发生氧化还原反应生成一种单质和一种化合物,写出该反应的化学方程式。
-
(2) 测定元素③的氢化物的相对分子质量时常常偏大,原因是。为了尽可能减小偏差,通常选择温度压强条件(选填“高”、“低”)。
-
(3) 甲、乙分别与元素①的氢化物反应生成丙、丁、戊三种盐。0.1 mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)。
-
(4) 一种断路器的气体绝缘介质是③、⑤两种元素的原子形成的正八面体分子,⑤原子位于中心,其分子式为,该分子属于(选填“极性”、“非极性”)分子,该气体不能燃烧,原因是(指出两种元素的化合价并做简单分析)。
H2S是一种具有气味的有毒气体,分子的电子式是,把H2S气体通入到CuSO4溶液中,现象是,反应的化学方程式。
将导出H2S气体的导管点燃后伸入盛有一定量O2的集气瓶内,下列3个反应发生的先后顺序是( )
① 2H2S + O2→ 2S + 2H2O ② 2H2S + SO2→ 3S + 2H2O ③ 2H2S + 3O2→ 2SO2+ 2H2O
A . ①②③
B . ③①②
C . ①③②
D . ③②①
下列反应中,不能产生黑色固体的是( )
A . Cu在硫蒸气中燃烧
B . Fe粉和S粉混合后点燃
C . H2S通入硫酸亚铁溶液中
D . H2S通入硫酸铜溶液
硫化氢气体不具有( )
A . 毒性
B . 可燃性
C . 还原性
D . 漂白性
喷泉实验装置如图所示。应用下列各组气体—溶液,能出现喷泉现象的是( )
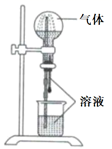
|
气体 |
溶液 |
|
|
A. |
H2S |
稀盐酸 |
|
B. |
HCl |
稀氨水 |
|
C. |
NO |
稀H2SO4 |
|
D. |
CO2 |
饱和NaHCO3溶液 |
A . A
B . B
C . C
D . D
室温下,向100mL饱和的H2S溶液中通入SO2气体(气体体积换算成标准状况),发生反应:2H2S+SO2=3S↓+2H2O,测得溶液pH与通入SO2的关系如图所示。下列有关说法错误的是( )
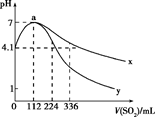
A . a点水的电离程度最大
B . 该温度下H2S的Ka1≈10-7.2
C . 曲线y代表继续通入SO2气体后溶液pH的变化
D . a点之后,随SO2气体的通入,  的值始终减小
的值始终减小
 的值始终减小
的值始终减小
H2S是无色有恶臭味的有毒气体,空气中含0.1%的H2S就会迅速引起头痛、晕眩等症状,吸入大量H2S会造成昏迷或死亡。是一种神经毒剂。亦为窒息性和刺激性气体。其毒作用的主要靶器是中枢神经系统和呼吸系统,亦可伴有心脏等多器官损害,下列有关H2S的性质和用途说法错误的是( )
A . 硫化氢能被氧气、氯气、碘、溴等单质氧化成硫单质
B . 将H2S通入Pb(NO3)2溶液得到黑色沉淀,再加双氧水,沉淀会转化为白色
C . 将H2S气体通入CuSO4溶液中得到CuS沉淀,通入FeSO4溶液会产生FeS沉淀
D . H2S通入到FeCl3 溶液中,溶液酸性增强
下列物质不能用于吸收H2S的是( )
A . NaOH溶液
B . FeSO4溶液
C . CuCl2溶液
D . 酸性KMnO4溶液
下列物质鉴别的方法错误的是( )
A | B | C | D | |
物质 | H2S、SO2 | FeS、CuS | CH4、C2H2 | Na2CO3、Na2SO4 |
鉴别方法 | 通入溴水 | 加入水 | 燃烧 | 加入AlCl3溶液 |
A . A
B . B
C . C
D . D
在“价—类”二维图中融入“杠杆模型”,可直观辨析部分物质转化及其定量关系。如图中的字母分别代表硫及其常见化合物,相关推断不合理的是( )
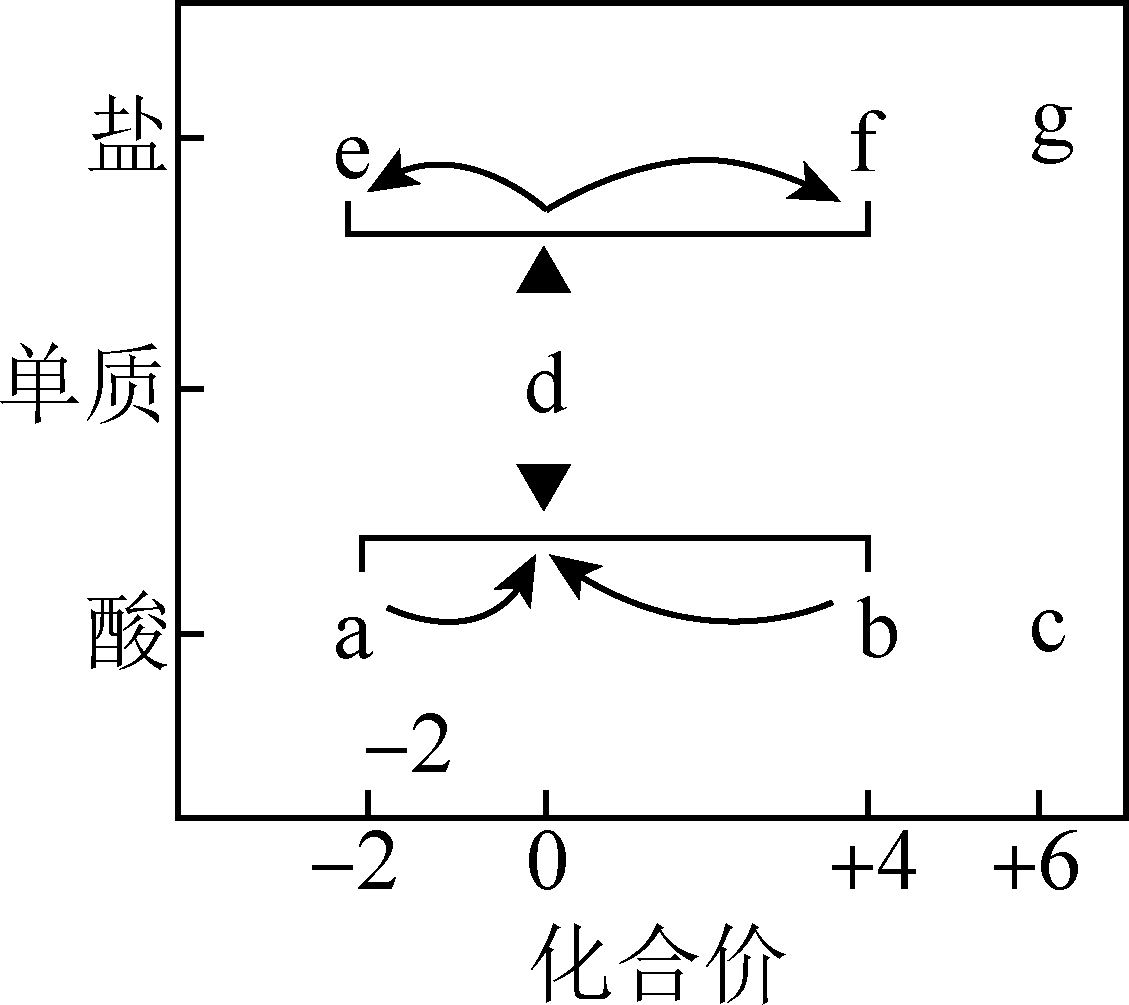
A . b既具有氧化性又具有还原性
B . 硫酸型酸雨的形成过程涉及b到c的转化
C . a溶液与b溶液反应过程中有淡黄色沉淀生成
D . d在加热下与强碱溶液反应生成e和f,且n(e):n(f)=1:2
硫化氢( )、二氧化硫(
)、二氧化硫( )是有害气体,可用多种方法进行脱除。
)是有害气体,可用多种方法进行脱除。
 )、二氧化硫(
)、二氧化硫( )是有害气体,可用多种方法进行脱除。
)是有害气体,可用多种方法进行脱除。
-
(1) 实验室制取乙炔时,用硫酸铜溶液除去乙炔气体中混有的
 气体,发生反应:
气体,发生反应: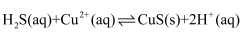 , 计算25℃时,该反应的平衡常数为。(已知25℃时
, 计算25℃时,该反应的平衡常数为。(已知25℃时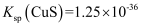 ,
,  的
的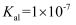 ,
, 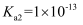 )
)
-
(2) 某科研小组将微电池技术用于去除天然气中的
 , 装置示意图如图,主要反应:
, 装置示意图如图,主要反应: (FeS难溶于水),室温时,pH=7的条件下,研究反应时间对
(FeS难溶于水),室温时,pH=7的条件下,研究反应时间对 的去除率的影响。
的去除率的影响。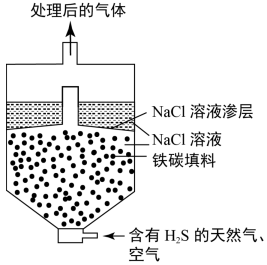
①装置中微电池负极的电极反应式为。
②一段时间后,单位时间内
 的去除率降低,可能的原因是。
的去除率降低,可能的原因是。 -
(3)
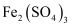 溶液脱除空气中
溶液脱除空气中 并再生的原理如图所示。
并再生的原理如图所示。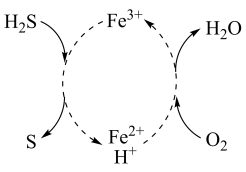
将一定体积含
 的空气匀速通入
的空气匀速通入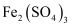 溶液中,反应相同时间,初始
溶液中,反应相同时间,初始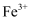 浓度。
浓度。 及其pH与
及其pH与 脱除率的关系如图所示。当
脱除率的关系如图所示。当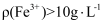 ,
,  脱除率下降的原因是。
脱除率下降的原因是。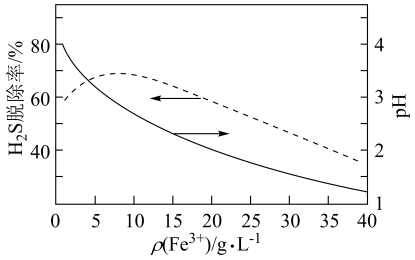
-
(4) 在恒容密闭容器中,用H2还原
 生成S的反应分两步完成(如图所示),该过程中部分物质的物质的量浓度随时间的变化关系如图所示:
生成S的反应分两步完成(如图所示),该过程中部分物质的物质的量浓度随时间的变化关系如图所示: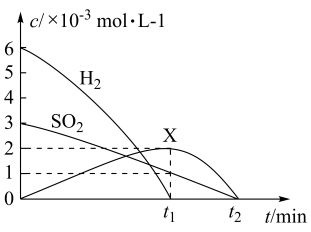
依据上图描述H2还原
 生成S的过程:。
生成S的过程:。
最近更新
- 下列物质的性质属于物理性质的是……( ) A、二氧化硫的漂白性 B、浓硫酸的脱水性 C、浓硝酸的不稳定
- 在切西瓜时,会有许多甜甜的汁液流出,这种汁液主要存在于() A.液泡内 B.细胞膜上 C.细胞核内
- 南宋大臣文天样在被俘押往元朝大都的途中写道:“草合离宫转夕晖,孤云飘泊复何依。山河风景元无异,城郭人民半已非。满地芦花和
- 要使二次根式有意义,应满足的条件是 。
- The Guangyue Tower of Liaocheng carries its legends,and ever
- 琥珀酸乙酯的键线式结构如图所示。下列关于它的说法不正确的是( )A.琥珀酸乙酯的化学式为C8H14O4B.琥珀酸乙
- 下列胰岛细胞中物质运输的途径,不存在的是() A.CO2:线粒体基质产生→细胞质基质→细胞膜→细胞外 B.RNA聚合酶(
- How long has 3-D technology been around? Most of us might th
- 若z=-i,则z2的共轭复数是__________.
- 读“我国西气东输主干运输线路示意图”,回答下列问题。(10分)(1)西气东输主干线路沿途自然带体现了
- 若一个直角三角形三内角的正弦值成等比数列,则其中最小内角的正弦值为_________.
- — How long _____ at this job ? — Since 2008. A. were you c
- 医学界早已知道,与正常细胞相比,肿瘤细胞需要吸收更多的葡萄糖才能维持其生长。美国一项最新研究发现,如果限制体内谷氨酰胺的
- 1906年2月,清政府拟定了一项决议:凡派去日本留学的,只限于那些擅长中文并精通儒家经典的学生。对该决议的理解,正确的是
- 1880年美国生物学家恩格尔曼设计了一个实验研宄光合作用的光谱。他将棱镜产生的光谱投射到丝状水绵体上,并在水绵悬液中放入
- 浓度均为0.1mol/L的NH4Cl、(NH4)2SO4、NH4HSO4、(NH4)2Fe(SO4)2四种溶液中,设NH
- 国家游泳中心“水立方”以及国家体育场“鸟巢”的设计充分发挥了中国传统的空间观、宇宙观和建筑观,两种建筑在外形上相呼应,体
- 自古至今,人口迁移与人口流动都对经济和社会的发展产生了重大影响。阅读下列材料,回答有关问题。 材料二 表1 20
- 读“我国西北地区不同程度荒漠化土地分布图” 我国近50年来土地荒漠化严重的原因有() A.降水量减少,蒸发旺盛 B.人类
- 下图为蒸馏实验装置: ⑴ 写出下列仪器的名称: ① ;② 。 ⑵ 在仪器①中



