测定溶液pH的方法 知识点题库
(1)你支持 (填“乙”或“丙”)同学的观点,原因是 .
(2)若用此法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是 ,原因是 .
(3)只从下列试剂中选择实验所需的物品,你(填“能”或“不能”)区分0.1mol/L的硫酸和0.01mol/L的硫酸.若能,简述操作过程.
①紫色石蕊试液 ②酚酞试液 ③甲基橙试液④蒸馏水 ⑤BaCl2溶液 ⑥pH试纸.
A | 乙烯使溴水褪色 苯使溴水褪色 | 均发生了加成反应 |
B | 用pH试纸测定某盐酸的pH 用红色石蕊试纸检验某气体为氨气 | 试纸均需要蒸馏水湿润 |
C | MnO2与浓盐酸反应制备Cl2 CaCO3与稀盐酸反应制备CO2 | 均发生氧化还原反应 |
D | 淀粉在酶的作用下生成葡萄糖 蛋白质在酶的作用下生成氨基酸 | 均发生了水解反应 |
| 选项 | 实验操作和现象 | 结论 |
| A | 某溶液 | 原溶液中一定含有CO32- |
| B | 用湿润的pH试纸测某碱液的pH,测定值偏小 | 湿润的pH试纸测量任何溶液都会产误差 |
| C | 将浓硫酸倒入蔗糖中搅拌蔗糖迅速变黑并伴有刺激性气味 | 浓硫酸具有脱水性和强氧化性 |
| D | 将乙烯和苯分别加入到溴水中,都能使溴水层褪色 | 乙烯和苯分子中都含有碳碳双键 |
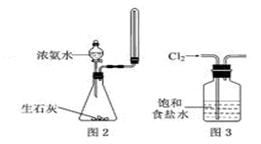

-
(1) 由此可以得到的结论是(填字母)。
a.NH3·H2O是弱碱
b.溶液中c(H+)>c(OH-)
c.NH4+水解是吸热反应
d.由H2O电离出的c(H+)<10-7mol/L
e.物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
-
(2) 室温下,用0.10mol/LNaOH溶液分别滴定20.00mL0.10mol/L的盐酸和醋酸,滴定曲线如图所示
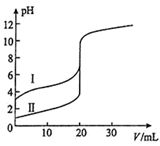
①表示滴定盐酸的曲线是(填序号)。
②若此实验选用酚酞为指示剂,则滴定到达终点的现象是。
③若用标准NaOH溶液测定未知盐酸溶液的浓度,下列实验操作会使实验结果偏低的是。
a.锥形瓶用待测液润洗后再注入待测液
b.碱式滴定管滴定前有气泡,滴定后无气泡
c.碱式滴定管滴定前仰视读数,滴定后平视读数
②在滴定醋酸溶液的过程中:V(NaOH)=10.00mL时,溶液中离子浓度由大到小的顺序为。当c(Na+)=c(CH3COO-)+c(CH3COOH)时,溶液pH7(填“>”、“=”或“<”)。
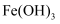 胶体:将
胶体:将  浓溶液滴加到饱和的
浓溶液滴加到饱和的  溶液中
B . 检验溶液中的
溶液中
B . 检验溶液中的  取一根洁净的铂丝,放在酒精灯外焰上灼烧至与原来的火焰颜色相同时为止,再蘸取少量试液,在外焰上灼烧,透过蓝色钴玻璃观察,若火焰呈紫色,则含有
取一根洁净的铂丝,放在酒精灯外焰上灼烧至与原来的火焰颜色相同时为止,再蘸取少量试液,在外焰上灼烧,透过蓝色钴玻璃观察,若火焰呈紫色,则含有 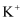 C . 测定
C . 测定  溶液
溶液 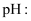 用玻璃棒蘸取溶液,点在湿润的
用玻璃棒蘸取溶液,点在湿润的  试纸上
D . 配制
试纸上
D . 配制 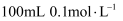 氯化钠溶液:称取
氯化钠溶液:称取 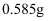 氯化钠固体,放入
氯化钠固体,放入 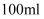 量筒中,加水定容至
量筒中,加水定容至 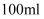 刻度线
刻度线
|
选项 |
实验目的 |
实验方法 |
相关解释 |
|
A |
测量氯水的pH |
|
pH试纸遇酸变红 |
|
B |
测量锌粒和3mol/L硫酸反应生成 |
|
|
|
C |
探究正戊烷 |
|
|
|
D |
用 |
|
|
 溶液用托盘天平称取5.85g
溶液用托盘天平称取5.85g  固体
固体
| 方案设计 | 现象 | 结论 | |
| A | 用pH试纸测定NaCl与NaF溶液的pH | 前者小于后者 | F元素的非金属性强于Cl |
| B | 压缩装有HI、I2、H2混合气体(已达平衡)的容器 | 颜色加深 | 平衡向生成I2的方向移动 |
| C | 用pH试纸测量饱和新制氯水的pH | pH试纸变为红色 | 饱和新制氯水呈酸性 |
| D | 向酸性KMnO4和H2C2O4的混合液中加入一小块MnSO4 | 生成气体(CO2)的速率加快,溶液迅速褪色 | MnSO4是该反应的催化剂 |
- 下列细胞器,光学显微镜下能看到的是( ) A. 核糖体 B.内质网 C.叶绿体 D.A、B、C都
- NO2、O2和熔融KNO3可制作燃料电池,其原理如图所示。该电池在放电过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用。下列
- 10. Sometimes I really wonder how I could make friends with
- Youmay know the difference between an American accent and a
- 你也是网民吗?我国的网络队伍正在日益扩大,网民在一些词前加“被”字,如“被就业”“被增长…被代表”“被自愿”等。这些词
- 实验室常用二氧化锰与浓盐酸反应制取氯气,反应的化学方程式为: MnO2+4HCI(浓)MnCl2+2X+Cl2↑,其中X
- 只用胶头滴管和试管,就能区别的溶液(均为0.1 mol·L-1)是() A.CaCl2和Na2CO3
- 化学用语是学习化学的基本工具,请用化学符号或化学式填空: (1)2个磷原子 (2)地壳中含量最多的元素 (3)5个
- Ifyou stand here, you'll get a better ________ of the river.
- 恩格斯说:“当法国革命使这个理性的社会和这个理性的国家成为现实的时候,新制度就表明,不论它较之旧制度如何合理,却决不是绝
- 下列各句中,加点的成语或熟语使用正确的一项是( ) A、随着外出务工收入的逐渐提高,息州人购买私家车的热情蔚然
- 如图,①~④表示某细胞内的部分细胞器。下列有关叙述正确的是 A.该图是在高倍光学显微镜下看到的结构 B.此细胞不可能是
- 如图所示,一根均匀的导体棒ab,长为l,质量为m,电阻为R0,处在磁感应强度为B的匀强磁场中,导体ab由两根相同的轻质弹
- 西周初年,疆域空前辽阔。周王为巩固对周边的统治,“封建亲戚,以藩屏周”。这是下面的哪一种制度( ) A.禅让制
- 阅读《蒹葭》一诗的第一节,按要求做题。 蒹葭苍苍,白露为霜。所谓伊人,在水一方。 溯洄从之,道阻且长。邀游从之,宛在水中
- 已知以F为焦点的抛物线上的两点A、B满足,则弦AB的中点到准线的距离为___________
- 人体内二氧化碳浓度最大的地方是() A. 肺泡 B.肺泡周围毛细血管 C. 组织
- 已知向量=(1,2),=(3,1),则与的夹角为() A.30° B.45° C.120° D.135°
- a※b是新规定的这样一种运算法则:a※b=a2+2ab,若(-2)※x=8, 则x=________。
- 在森林群落中,乔木、灌木、草本植物三类绿色植物在空间位置配备上形成了有序的组合,从而使它们能( ) A.
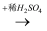 生成使石灰水变浑浊的无色气体
生成使石灰水变浑浊的无色气体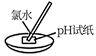
 的体积
的体积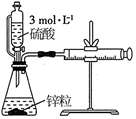
 会与锌粒反应生成
会与锌粒反应生成  催化裂解
催化裂解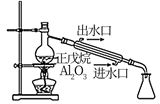
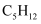 裂解为分子较小的烷烃和烯烃,可以冷凝收集
裂解为分子较小的烷烃和烯烃,可以冷凝收集 溶液制备
溶液制备