物质的检验和鉴别 知识点题库
下列实验方法正确的是
A . 用NaOH溶液鉴别SO2和CO2
B . 用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体
C . 用Na2CO3溶液鉴别HCl溶液和H2SO4溶液
D . 用焰色反应鉴别NaCl和NaNO3
为鉴别K2CO3和NaHCO3两种白色固体,有4位同学分别设计了以下四种不同的方案,其中方法和现象判断正确的是( )
A . 分别加入1mol/L的盐酸溶液,看有无气泡产生
B . .分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀
C . 用铂丝粘取固体在酒精灯火焰上灼烧,观察火焰的颜色,NaHCO3的焰色为紫色
D . 分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊
现有MgCl2、AlCl3、CuCl2、FeCl3、NH4Cl五种溶液,只用一种试剂把它们区别开来,这种试剂是( )
A . 氨水
B . AgNO3
C . NaOH
D . H2SO4
对于某些离子的检验及结论一定正确的是( )
A . 通入Cl2后,溶液变为黄色,加淀粉液后溶液变蓝,则原溶液中一定有I﹣
B . 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,则原溶液中一定有SO42﹣
C . 加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,则原溶液中一定有CO32﹣
D . 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
下列不能用于鉴别SO2 和CH2=CH2两种无色气体的试剂是( )
A . 含酚酞的氢氧化钠溶液
B . 品红溶液
C . 酸性高锰酸钾溶液
D . 溴的四氯化碳溶液
下列说法正确的是( )
A . 用澄清石灰水可以鉴别碳酸钠和碳酸氢钠
B . 新制氯水经光照一段时间pH减小
C . 自然界硅元素贮量丰富,并存在大量的单质硅
D . 等质量的碳酸钠与碳酸氢钠分别于足量盐酸反应,产生二氧化碳质量相同
某混合物X由Al2O3、Fe2O3、Cu、SiO2中的一种或几种物质组成.某校课外兴趣小组以两条途径分别对X进行如下实验探究.下列有关说法不正确的是( )
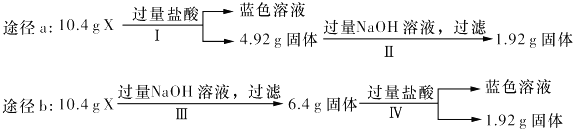
A . 由工可知X中一定存在Fe2O3、Cu
B . 无法判断混合物中是否含有Al2O3
C . 1.92 g固体成分为Cu
D . 原混合物中m( Fe2O3):m(Cu)=1:1
有一包白色粉末,其中可能含有NaCl、Ba(NO3)2、CuSO4、Na2CO3 , 现做以下实验:
①将部分粉末加入水中,振荡,有白色沉淀生成,过滤,滤液呈无色
②向①中的沉淀物中加入足量稀硝酸,固体完全溶解,并有气泡产生
③取少量②的溶液,滴入稀硫酸,有白色沉淀产生
试根据上述实验现象判断,原白色粉末中一定含有的物质是,可能含有的物质是(以上物质均写化学式),第②步反应中离子方程式为
A,B,C,D为原子序数依次增大的短周期元素,A元素气态氢化物的水溶液呈碱性,B为最活泼的非金属元素,C元素原子的电子层数是最外层电子数的3倍,D元素最高化合价为+6价。
-
(1) A元素气态氢化物的电子式为;B在元素周期表中的位置为。
-
(2) DBn做制冷剂替代氟利昂,对臭氧层完全没有破坏作用,是一种很有发展潜力的制冷剂。该物质的摩尔质量为146 g·mol-1 , 则该物质的化学式为。已知DBn在温度高于45℃时为气态,DBn属于晶体。该物质被称为人造惰性气体,目前广泛应用于电器工业,在空气中不能燃烧,请从氧化还原角度分析不能燃烧的理由。
-
(3) C与氢元素组成1∶1的化合物,与水发生剧烈反应生成碱和一种气体,写出该反应的化学反应方程式,生成1mol气体转移的电子的数目为个。
-
(4) A和C两元素可形成离子化合物甲。取13.0g化合物甲,加热使其完全分解,生成A的单质和C的单质,生成的A单质气体折合成标准状况下的体积为6.72L。化合物甲分解的化学方程式为。
-
(5) D元素的+4价含氧酸钠盐在空气中容易变质,设计实验方案证明该盐已经变质。
只用一种试剂区别乙醇、乙醛、己烯、甲酸四种无色液体,应选用( )
A . 酸性 KMnO4溶液
B . 溴水
C . 紫色石蕊溶液
D . 新制氢氧化铜悬浊液
某100mL溶液可能含有Na+、NH  、Fe3+、CO
、Fe3+、CO  、SO
、SO  、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法错误的是( )。
、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法错误的是( )。
 、Fe3+、CO
、Fe3+、CO  、SO
、SO  、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法错误的是( )。
、Cl-中的若干种,取该溶液进行连续实验,实验过程如图:(所加试剂均过量,气体全部逸出)下列说法错误的是( )。
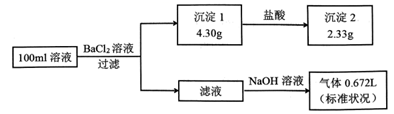
A . 原溶液一定存在CO  和SO
和SO  ,一定不存在Fe3+
B . 是否存在Na+只有通过焰色试验才能确定
C . 原溶液一定存在Na+ , 可能存在Cl-
D . 若原溶液中不存在Cl- , 则c(Na+)=0.1mol·L-1
,一定不存在Fe3+
B . 是否存在Na+只有通过焰色试验才能确定
C . 原溶液一定存在Na+ , 可能存在Cl-
D . 若原溶液中不存在Cl- , 则c(Na+)=0.1mol·L-1
 和SO
和SO  ,一定不存在Fe3+
B . 是否存在Na+只有通过焰色试验才能确定
C . 原溶液一定存在Na+ , 可能存在Cl-
D . 若原溶液中不存在Cl- , 则c(Na+)=0.1mol·L-1
,一定不存在Fe3+
B . 是否存在Na+只有通过焰色试验才能确定
C . 原溶液一定存在Na+ , 可能存在Cl-
D . 若原溶液中不存在Cl- , 则c(Na+)=0.1mol·L-1
以下实验设计能达到实验目的的是( )
| 选项 | 实验目的 | 实验设计 |
| A | 除去NaHCO3固体中的Na2CO3 | 将固体加热至恒重 |
| B | 制备无水AlCl3 | 蒸发Al与稀盐酸反应后的溶液 |
| C | 重结晶提纯苯甲酸 | 将粗品水溶、过滤、蒸发、结晶 |
| D | 鉴别NaBr和KI溶液 | 分别加新制氯水后,用CCl4萃取 |
A . A
B . B
C . C
D . D
下列说法正确的是( )
A . 向蛋白质溶液中加入重金属盐溶液可使蛋白质产生盐析
B . 油脂在碱性条件下水解生成高级脂肪酸和甘油
C . 区别棉花和蚕丝的方法是灼烧后闻其是否有烧焦羽毛的气味
D . 淀粉和纤维素组成都是(C6H10O5)n , 二者属于同分异构体
某研究小组利用如图所示的装置,进行  还原
还原  的实验(固定装置略)。
的实验(固定装置略)。
 还原
还原  的实验(固定装置略)。
的实验(固定装置略)。 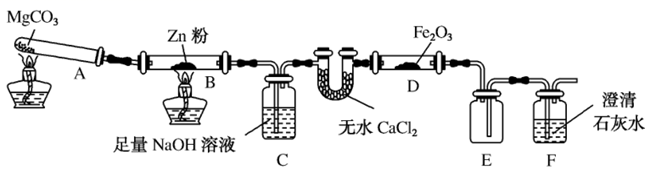
-
(1) 写出装置B中发生反应的化学方程式。
-
(2) 用酒精喷灯对装置D加热,得到灰黑色粉末,用灰黑色粉末进行以下实验:
步骤
操作
现象
1
取灰黑色粉末加入稀硫酸
溶解,有气泡
2
取步骤1中溶液,滴加
 溶液后,在空气中,搅拌放置
溶液后,在空气中,搅拌放置白色沉淀最终变为红褐色
3
取步骤1中溶液,滴加
 溶液
溶液无现象
4
向步骤3溶液中滴加新制氯水至过量
先变红,后褪色
①得到的灰黑色粉末一定有(填写化学式)。
②步骤2中“白色沉淀最终变为红褐色”的化学反应方程式为。
③步骤4中,溶液变红的原因为
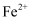 被氧化为
被氧化为 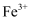 ,
, 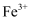 遇
遇 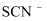 显红色;写出
显红色;写出 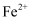 被氧化的离子方程式;溶液褪色的可能原因是
被氧化的离子方程式;溶液褪色的可能原因是 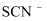 可能被
可能被 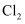 氧化;验证上述原因的实验操作方法为。
氧化;验证上述原因的实验操作方法为。 -
(3) 上述装置,从实验安全考虑,需要采取的改进措施是。
-
(4) 聚合硫酸铁(铁元素均为+3价)可用于水的净化,其化学式可表示为
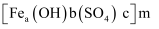 。取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份,一份溶液中加入足量的
。取一定量聚合硫酸铁样品与足量盐酸反应,所得溶液平均分为两份,一份溶液中加入足量的 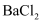 溶液,得到白色沉淀
溶液,得到白色沉淀 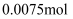 ,另一份溶液,先将
,另一份溶液,先将 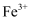 还原为
还原为 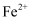 ,再用
,再用  标准溶液滴定至终点,消耗
标准溶液滴定至终点,消耗  标准溶液
标准溶液 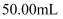 。该聚合硫酸铁样品中
。该聚合硫酸铁样品中 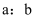 的比值为。(没有计算过程不得分)(已知:
的比值为。(没有计算过程不得分)(已知: 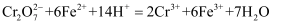 )
)
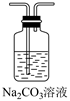
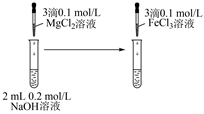
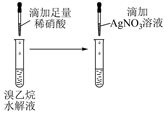
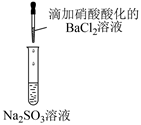
下列实验方案能达到相应目的的是( )
| A | B | C | D |
| | | | |
| 除去 | 相同温度下的溶解度: | 检验溴乙烷水解产物中含有 | 检验 |
A . A
B . B
C . C
D . D
某固体可能含有  、
、  、
、  、
、  、
、  、
、  中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离)
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离)
 、
、  、
、  、
、  、
、  、
、  中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离)
中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离) ⑴一份固体溶于水得无色透明溶液,加入足量  溶液,得沉淀4.30 g,在沉淀中加入过量稀盐酸,仍有2.33 g沉淀。
溶液,得沉淀4.30 g,在沉淀中加入过量稀盐酸,仍有2.33 g沉淀。
⑵另一份固体与过量NaOH固体混合后充分加热,产生 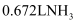 (标准状况)。
(标准状况)。
下列说法正确的是( )
A . 根据以上实验,无法确定该固体中有  B . 该固体中一定含有
B . 该固体中一定含有  、
、  、
、  、
、  C . 该固体中只含有
C . 该固体中只含有  、
、  、
、  、
、  D . 该固体中一定没有
D . 该固体中一定没有  、
、  、
、 
 B . 该固体中一定含有
B . 该固体中一定含有  、
、  、
、  、
、  C . 该固体中只含有
C . 该固体中只含有  、
、  、
、  、
、  D . 该固体中一定没有
D . 该固体中一定没有  、
、  、
、 
下列实验方案能达成目的的是( )
A . 用乙醇萃取溴水中的溴单质
B . 用焰色反应鉴别KCl和NaOH
C . 用KOH溶液提纯NaCl(其中含有MgCl2)
D . 用BaCl2溶液鉴别Na2CO3溶液与Na2SO4溶液
某固体混合物X,含有 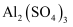 、
、  、
、  和
和 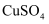 中的几种,进行如下实验:
中的几种,进行如下实验:
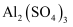 、
、  、
、  和
和 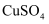 中的几种,进行如下实验:
中的几种,进行如下实验: ①X与水作用有气泡冒出,得到有色沉淀Y和弱碱性溶液Z;
②沉淀Y中加入足量的  溶液,沉淀减少但不消失。
溶液,沉淀减少但不消失。
下列说法错误的是( )
A . 混合物X中必定含有  、
、 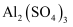 B . 溶液Z中溶质主要是钠盐,且必含
B . 溶液Z中溶质主要是钠盐,且必含  C . 灼烧沉淀Y,可能得到黑色物质
D . 往溶液Z中加入
C . 灼烧沉淀Y,可能得到黑色物质
D . 往溶液Z中加入 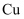 粉,若不溶解,说明X中不含
粉,若不溶解,说明X中不含 
 、
、 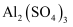 B . 溶液Z中溶质主要是钠盐,且必含
B . 溶液Z中溶质主要是钠盐,且必含  C . 灼烧沉淀Y,可能得到黑色物质
D . 往溶液Z中加入
C . 灼烧沉淀Y,可能得到黑色物质
D . 往溶液Z中加入 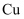 粉,若不溶解,说明X中不含
粉,若不溶解,说明X中不含 
有一包白色固体粉末,其中可能含有 KCl、Ba(NO3)2、CuSO4 、Na2CO3中的一种或几种,现做以下实验(所加试剂均足量):
则下列说法正确的是( )
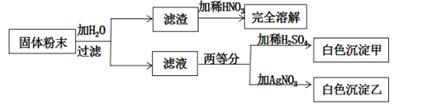
A . 原粉末中一定有 KCl、Na 2 CO 3 、Ba(NO 3 ) 2
B . KCl 是否存在无法确定,可以通过焰色反应来确定
C . 白色沉淀乙可能是 AgCl 和 Ag 2 CO 3 的混合物
D . 原粉末中一定没有 CuSO 4 , 可能有 KCl
能够用来鉴别BaCl2、NaCl、Na2CO3三种物质的试剂是( )
A . AgNO3
B . HCl
C . H2SO4
D . HNO3
最近更新
- 细胞膜功能的复杂程度主要取决于膜上的 A.磷脂的含量
- 下列各组离子能在溶液中大量共存的是A.K+、Ag+、NO、Cl-
- 如图,△ABC中,∠ABC=45°,AC=4,H是高AD和BE的交点,则线段BH的长度为 _____________。
- 下图为我国部分优质农产品基地分布图,读图回答10~1l题。10.甲、乙两地均为我国重要的反季节蔬菜生产基地,其形成的主要
- 李瑞环同志在《学哲学,用哲学》一书中说:“哲学是‘明白学’,许多事情只有学了哲学才能真正明白;哲学是‘智慧学’,学了哲学
- 34.用32P标记的噬菌体侵染大肠杆菌,经培养、搅拌、离心、检测,上清液的放射性占15%,沉淀物的放射性占85%,上清液
- 下列句子中,加点的成语使用恰当的一项是( ) A.在国产动画电影《风云决》的首映典礼上,任贤齐坦言配音过程“很困难
- 2010年10月中共中央在中南海召开党外人士座谈会,介绍了中共中央起草的 《中共十七届五中全会关于制定国民经济和社会发展
- 下图为“自然界碳、水物质循环示意图”。读图回答下列各题。人类对碳循环过程的影响是造成目前全球气候变暖的主要原因,其中最主
- 下列技术依据DNA分子杂交原理的是()①用DNA分子探针诊断疾病 ②B淋巴细胞与骨髓瘤细胞的
- 物体从地面被竖直上抛,最后落回抛出点.若其所受阻力随速度增大而增大,则下列说法中正确的是()A.因为物体在上升过程中比下
- 以“净化”为话题作文导写 在现实生活中,随着商品经济的发展,我们的心灵也在时时刻刻被撞击着、触动着。或许我们的心灵受到污
- 假如某地只有10个铜板和10个梨子,且一个梨子=一个铜板。后该地发行10元纸币代替10个铜板,则1元纸币=1个铜板,这时
- 空气是生命赖以存在的物质基础,也是人类生产活动的重要资源,下列有关空气的说法正确的是() A.空气中分离出的氮气化学性质
- 已知两个等差数列和的前项和分别为A和,且,则使得为整数的正整数的个数是() A.2 B.3
- 建全国文明城市,保“舌尖上的安全”。下列做法符合安全要求的是() A.甲醛溶液保鲜食物 B.问题食盐禁止销售 C.亚硝
- 如图所示,在正六边形的a、c两个顶点上各放一个带正电的点电荷,电荷量的大小都是q1,在b、d两个顶点上各放一个带负电的点
- 我国制碱工业先驱侯德榜发明了“侯氏制碱法”(这里的“碱”即纯碱:Na2CO3)。其模拟流程如下:(1)操作a的名称是
- The population in Beijing is much larger than ________ in Ji
- 下列加点词古今用法相同的一项是( ) A 亦有用法煨 B 可谓智力孤危 C 而告以成功 D 即免冰冻,仍得发生
 中的
中的 

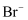
 溶液是否变质
溶液是否变质


