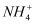氮气的化学性质 知识点题库
-
(1) 氮分子的电子式为 ,通常情况下氮气化学性质比较稳定的原因是
-
(2) 氮气在一定条件下与镁反应生成氮化镁(Mg3N2),氮化镁与水反应生成两种碱,其反应的化学方程为
气体,这种气体是( )
-
(1) Ⅰ.Cu(NO3)2 的氧化性
将光亮的铁丝伸入Cu(NO3)2 溶液中,一段时间后将铁丝取出。为检验溶液中Fe 的氧化产物,将溶液中的Cu2+除尽后,进行了如下实验。可选用的试剂KSCN 溶液、K3[Fe(CN)6]溶液、氯水。
请完成下表:
操作
反应或现象
结论
取少量除尽Cu2+后的溶液于试管中,加入溶液,振荡
现象
存在Fe3+
取少量除尽 Cu2+后的溶液于试管中,加入 K3[Fe(CN)6]溶液,振荡
离子方程式
存在Fe2+
-
(2) Ⅱ.Cu(NO3)2 的热稳定性
在如图所示的实验装置A 中,用酒精喷灯对Cu(NO3)2 固体加强热,产生红棕色气体,在装置C中收集到无色气体,经验证为O2。当反应结束以后,试管中残留固体为红色。
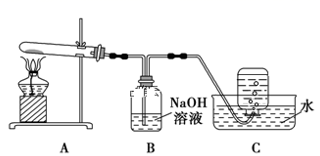

①装置B 的作用是 。
②从实验安全角度考虑,需要在A、B 间加入装置M,请在方框中画出M 装置。
③下图为Cu(NO3)2 样品高温过程的热重曲线(样品质量分数w%随温度变化的曲线)。Cu(NO3)2 加热到200℃的化学方程式为 ,继续高温至1000℃生成(填化学式)固体。
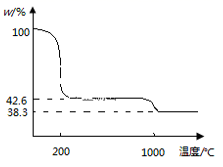 。
。
-
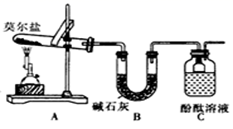
(1) I.探究莫尔盐晶体加热时的分解产物。
甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是,由此可知分解产物中有(填化学式)。
-
(2) 乙同学认为莫尔盐晶体分解的产物中还可能含有SO3(g)、SO2(g)及N2(g)。为验证产物的存在,用下列装置进行实验。
D. 品红溶液
 E.NaOH溶液
E.NaOH溶液  F.BaCl2溶液和足量盐酸
F.BaCl2溶液和足量盐酸  G.排水集气法
G.排水集气法 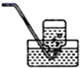 H. 安全瓶
H. 安全瓶 
①乙同学的实验中,装置依次连按的合理顺序为:A→H→() →() →() →G。
②证明含有SO3的实验现象是;安全瓶H的作用是。
-
(3) II.为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成500mL溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取25.00mL样品溶液用0.1000mol/L的酸性K2Cr2O7溶液分三次进行滴定。
乙方案(通过NH4+测定):实验设计装置如图所示。取25.00mL样品溶液进行该实验。
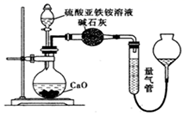
请回答:
甲方案中的离子方程式为。
-
(4) 乙方案中量气管中最佳试剂是。
a.水 b.饱和NaHCO3溶液 c.CCl4 d.饱和NaCl溶液
-
(5) 乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是。
-
(6) 若测得NH3为VL(已折算为标准状况下),则硫酸亚铁铵纯度为(列出计算式)
| 选项 | 实验操作及现象 | 结论 |
| A | 将充满氨气的试管倒置于滴有酚酞的水槽中,试管内迅速充满红色液体 | NH3极易溶于水且溶液显碱性 |
| B | 蔗糖中加入浓硫酸出现发黑现象 | 浓硫具有吸水性和强氧化性 |
| C | 向酸性KMnO2溶液中通入SO2 , 溶液褪色 | SO2有漂白性 |
| D | 向某盐溶液中加入NaOH溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝 | 该溶液中含有 |
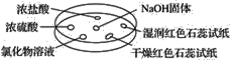
| 选项 | 实验现象 | 解释 |
| A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应产生了NH4Cl固体 |
| B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
| C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
| D | 干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝 | NH3是一种可溶性碱 |
-
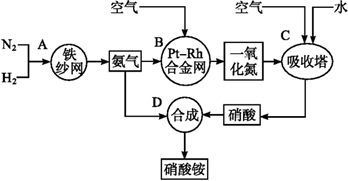
(1) 写出N2和H2通过红热的铁纱网生成氨气的反应方程式:。
-
(2) B装置中Pt-Rh合金网的作用是,写出B中有关反应方程式:。
-
(3) 写出D中反应方程式:。
-
(4) 吸收塔C中通入空气的目的是。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
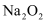 与
与  反应生成碳酸钠,则
反应生成碳酸钠,则 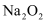 与
与  反应生成亚硫酸钠
B .
反应生成亚硫酸钠
B .  含有叁键,化学性质稳定,则
含有叁键,化学性质稳定,则 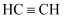 的化学性质也很稳定
C .
的化学性质也很稳定
C .  与
与  反应生成
反应生成 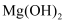 和
和  ,则
,则  与
与  反应生成
反应生成 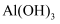 和
和  D .
D . 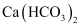 溶解度大于
溶解度大于 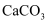 ,则
,则  溶解度大于
溶解度大于 
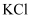 和
和  (溶解过滤,再蒸发结晶)
D . 氮气和氧气(蒸馏)
(溶解过滤,再蒸发结晶)
D . 氮气和氧气(蒸馏)
 NO(g)
NO(g)  NaNO2(aq)
B . SiO2
NaNO2(aq)
B . SiO2  Na2SiO3
Na2SiO3 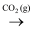 H2SiO3
C . S
H2SiO3
C . S  SO2
SO2  SO3→H2SO4
D . NH3
SO3→H2SO4
D . NH3  NO
NO  NO2→HNO3
NO2→HNO3
-
(1)
 的结构式是。
的结构式是。 常用作粮食、瓜果的保护气,其主要原因是。
常用作粮食、瓜果的保护气,其主要原因是。
-
(2) 目前工业合成氨的原理是
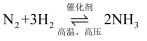 , 该反应正反应为放热反应。下列催化剂措施中,能加快该反应的化学反应速率的是____(填标号)。
A . 其他条件不变,适当增大
, 该反应正反应为放热反应。下列催化剂措施中,能加快该反应的化学反应速率的是____(填标号)。
A . 其他条件不变,适当增大 的浓度
B . 其他条件不变,降低反应体系的温度
C . 其他条件不变,减小反应体系的压强
D . 其他条件不变,使用更高效的催化剂
的浓度
B . 其他条件不变,降低反应体系的温度
C . 其他条件不变,减小反应体系的压强
D . 其他条件不变,使用更高效的催化剂
-
(3) 三元催化器是汽车排气系统重要的机外净化装置,可同时将碳氢化合物、一氧化碳和氮氧化物(
 )三种污染物转化为无害物质,其工作原理如下图所示。反应过程中被氧化的元素名称是。若
)三种污染物转化为无害物质,其工作原理如下图所示。反应过程中被氧化的元素名称是。若 为
为 , 则写出
, 则写出 和
和 反应的化学方程式为。
反应的化学方程式为。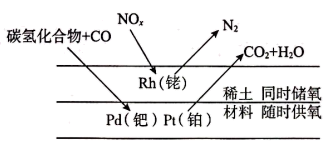
-
(4) 某汽车安全气囊的气体发生剂主要含有叠氮化钠(
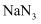 )、氧化铁、高氯酸钾、碳酸氢钠等物质。
)、氧化铁、高氯酸钾、碳酸氢钠等物质。①其中叠氮化钠是气体发生剂,受撞击时产生氮气和金属钠。若该反应生成67.2L(标准状况下)氮气时,转移电子的物质的量为
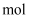 。
。②高氯酸钾是助氧化剂,在反应过程中与金属钠作用生成氯化钾和氧化钠。鉴别高氯酸钾中钾元素的实验操作及现象为。
 B .
B . 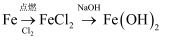 C .
C .  D .
D . 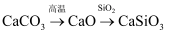
- 关于大西洋中部海岭的叙述正确的是 ①板块碰撞边界 ②板块张裂边界 ③生长边界 ④消亡边界 A.①④ B
- 下列反应的产物中,有的有同分异构体,有的没有同分异构体,其中一定不存在同分异构体的反应是
- 水箱中有水20m3,如果打开出水孔,水箱中的水5min可以流完,当打开出水孔时,水箱中的水的剩余量Vm3是时间t(s)的
- 下列命题正确的序号是________. ①定义在(a,b)上的函数f(x),若存在x1,x2∈(a,b)使得x1<
- 据美国全国广播公司报道,当地时间8月29日清晨6时10分,飓风“卡特里娜”裹胁狂风暴雨在美国墨西哥湾沿岸登陆,登陆时风速
- .已知向量,.若向量满足,,则 .
- 上海接连发生“钓鱼式”执法,引起全国民众的关注。以下对“钓鱼式”执法认识不正确的是( ) A.是解黑车问题的治本之策 B
- .以下两题,请任选一题作文。 (1)请以“我眼中的 ”为题,写一篇作文。 要求:请补全题目,除诗歌外,文
- 节日是非物质文化遗产之一,也在一定程度上反映了社会发展的进程。回答下面小题。 “五一”国际劳动节,是下列哪一重大事件后设
- 棉花是一个四倍体植株。它的单倍体细胞内含有的染色体组数是( ) A.1个B.2个C.3个D.4个
- .分解因式:a5-a3b2+ab4
- 有一个几何体的三视图及其尺寸如图(单位:cm),则该几何体的表面积及体积为()A.24π cm2,12π cm3
- 我国商业银行的主要业务是 A.存款业务、结算业务、买
- (09广州市调研)在以下选项中,含有核酸的细胞器是A.中心体 B.叶绿体 C.线粒体www.k
- 下图为某反应的微观示意图,“”、“”各表示一种原子,下列说法不正确的是 A.反应物是两种单质 B.反应物有剩余 C.该反
- 阅读下面文章,完成以下题目 阳台上的遗憾 从某种意义上来说,建筑是人心的外化和物化。南方在古代为蛮。化外之地,建筑上就多
- 在光照明亮的实验室里,用白色洋葱表皮细胞做质壁分离实验,在显微镜视野中能清晰看到细胞壁,但看不清楚细胞是否发生质壁分离,
- 函数图象交点的横坐标所在区间是( ) A.(1,2) B.(2,3) C.(3,4
- 把铝条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是A.盐酸的浓度
- 为了帮助日本地震灾区重建家园,某公司号召员工自愿捐款.请你根据两位经理的对话,计算出第一次捐款的人数.