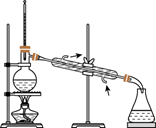
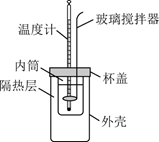
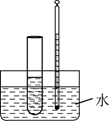
乙烯的实验室制法 知识点题库
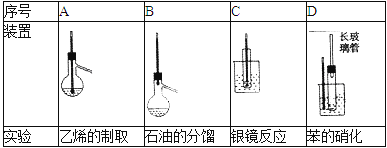
A~D是中学化学实验中使用温度计的装置示意图,其中所做实验与装置不相符的是( )
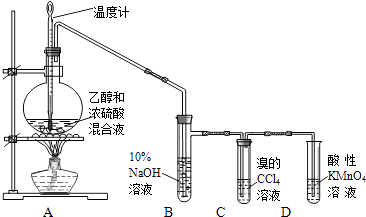
请回答有关问题:
-
(1) 烧瓶中除反应物以外,还应放2﹣3块碎瓷片,目的是.
-
(2) 烧瓶中产生乙烯的反应方程式为.
-
(3) 反应开始后,可观察到C和D中共同的现象是;
C中的反应类型为反应、D中的反应类型为反应.
-
(4) 反应结束冷却至室温,处理烧瓶中废液发现,反应液变黑、且有强烈的刺激性气味气体,其原因是;10%的NaOH溶液起的作用是.
①石油分馏时把温度计插入液面以下
②用溴水除去乙烯中混有的SO2气体
③用乙醇与1mol/L的H2SO4混合共热到170℃制取乙烯
④将饱和食盐水滴入盛有电石的烧瓶中制乙炔.
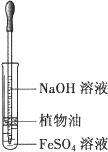 观察Fe(OH)2的生成
B .
观察Fe(OH)2的生成
B . 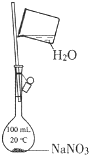 配制一定物质的量浓度的NaNO3溶液
C .
配制一定物质的量浓度的NaNO3溶液
C . 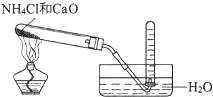 实验室制取氨
D .
实验室制取氨
D . 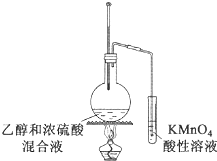 验证乙烯的生成
验证乙烯的生成
 实验室制乙烯
B .
实验室制乙烯
B . 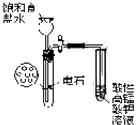 实验室制乙炔并验证乙炔发生氧化反应
C .
实验室制乙炔并验证乙炔发生氧化反应
C . 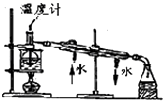 实验室中分馏石油
D .
实验室中分馏石油
D . 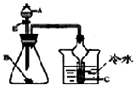 若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的强弱(不考虑醋酸的挥发)
若A为醋酸,B为贝壳(粉状),C为苯酚钠溶液,验证醋酸、苯酚、碳酸酸性的强弱(不考虑醋酸的挥发)
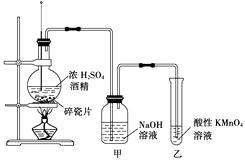
请回答:
-
(1) 实验步骤
①;
②在各装置中注入相应的试剂(如图所示);
③;实验时烧瓶中液体混合物逐渐变黑。
-
(2) 能够说明乙烯具有还原性的现象是;装置甲的作用是。若无甲装置,是否也能检验乙烯具有还原性,简述其理由:。
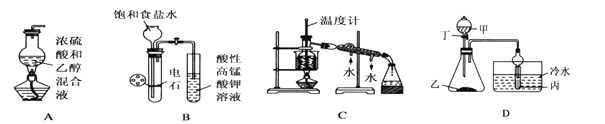
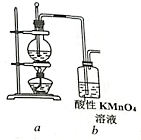
-
(1) 首先检验该装置气密性。检验气密性的操作是:。
-
(2) 向圆底烧瓶中加入药品的顺序是:先加入,再缓慢加入,最后再加入几粒碎瓷片。
-
(3) 加热圆底烧瓶,使温度迅速上升到℃,观察到烧瓶中的无色液体逐渐变黑。该黑色的物质是。
-
(4) 酸性KMnO4溶液很快褪色,但不能说明乙烯具有还原性。理由是:。
-
(5) 选用下列装置(可重复使用也可不用)来证明乙烯具有还原性,请将装置按编号依次排列,并在装置序号对应位置的下一行写出装置内所放的药品。
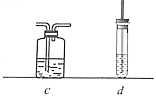
装置a→→b。
药品:(a药品略)(b酸性KMnO4溶液)。
-
(6) 若将b中酸性KMnO4溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,如何通过实验证明该无色油状液体中含有溴元素?。如何通过实验证明乙烯和溴水发生的是加成反应而不是取代反应?。
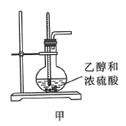
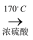 CH2=CH2↑+H2O,选用下图A进行反应。但常因温度过高而使乙醇和浓硫酸生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中存在乙烯和二氧化硫,试回答下列问题。
CH2=CH2↑+H2O,选用下图A进行反应。但常因温度过高而使乙醇和浓硫酸生成少量的二氧化硫。有人设计下列实验以确认上述混合气体中存在乙烯和二氧化硫,试回答下列问题。 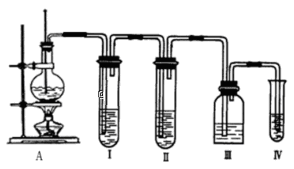
-
(1) 将下列所给的试剂中选出所必需的试剂,按气流方向从左到右依次是:(可重复,填字母)。
A. 品红溶液 B. NaOH溶液 C. 浓H2SO4 D. 溴水
-
(2) 能说明二氧化硫气体存在的现象是。
-
(3) 使用装置Ⅲ的目的是。
-
(4) 确定含有乙烯的现象是。
-
(5) 写出IV中发生的化学反应方程式。
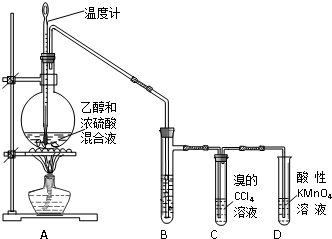
请回答有关问题:
-
(1) 烧瓶中除反应物以外,还应放2-3块碎瓷片,目的是:;
-
(2) 烧瓶中产生乙烯的反应方程式为:,反应类型为:;
-
(3) C中的现象是发生反应的化学方程式为:,反应类型为:;反应一段时间后,可观察到D中的现象是:;
-
(4) 制得的乙烯中混有 等杂质气体,写出生成杂质气体的化学方程式,B中所装的溶液是:溶液,起的作用是:。
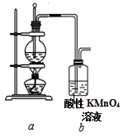
-
(1) 首项检验该装置气密性。检验气密性的操作是。
-
(2) 向圆底烧瓶中加入药品的顺序是:先加入,再缓慢加入,最后再加入几粒碎瓷片。
-
(3) 加热圆底烧瓶,使温度迅速上升到℃,观察到烧瓶中的无色液体逐渐变黑。该黑色的物质是。
-
(4) 酸性KMnO4溶液很快褪色,但不能说明乙烯具有还原性。理由是。
-
(5) 选用下列装置(可重复使用也不可用)来证明乙烯具有还原性,请在a,b装置间补充装置,按编号依次排列,并按照对应顺序写出装置内所放的药品。
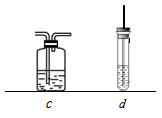
装置:a→ →b
药品:(a药品略)(b酸性KMnO4溶液)
-
(6) 若将b中酸性KMnO4溶液换成溴水,溴水也能褪色且可观察到b底部有少量无色油状液体生成,如何通过实验证明该无色油状液体中含有溴元素?
-
(7) 试设计一条以
 为原料合成
为原料合成 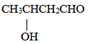 的合成路线。(合成路线常用的表示方式为:甲
的合成路线。(合成路线常用的表示方式为:甲 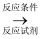 乙
乙 
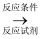 目标产物)
目标产物)
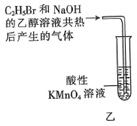
 与
与  的乙醇溶液反应生成的气体中含有乙烯
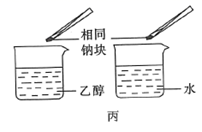
C . 操作丙可用于比较乙醇中羟基的氢原子和水分子中氢原子的活泼性
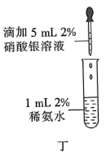
D . 操作丁可用于配制银氨溶液
的乙醇溶液反应生成的气体中含有乙烯
C . 操作丙可用于比较乙醇中羟基的氢原子和水分子中氢原子的活泼性
D . 操作丁可用于配制银氨溶液
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向溴水中滴加乙醛溶液 | 溶液褪色 | 乙醛能与Br2发生加成反应 |
| B | 无水乙醇和浓硫酸共热到170℃,将气体通入酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | 反应生成了乙烯 |
| C | 将乙烯通入溴的四氯化碳溶液 | 溶液最终变为无 色透明 | 生成的1,2-二溴乙烷 无色、可溶于四氯化碳 |
| D | 把卤代烃RX与烧碱水溶液混合加热,待冷却后先加入稀硝酸酸化,再加入硝酸银溶液 | 产生白色沉淀 | X为氯原子 |
目的 | 方案设计 | 现象和结论 | |
A | 检验溶液中是否含有 | 取少量该溶液于试管中,先滴加 | 若沉淀不溶解,则说明溶液中含有 |
B | 探究淀粉水解程度 | 在试管中加入2mL淀粉溶液和适量稀硫酸,加热 | 若溶液中没有出现砖红色沉淀,则说明淀粉未水解 |
C | 验证乙醇脱水生成乙烯 | 向无水乙醇中加入浓硫酸,加热至170℃,将产生的气体通入溴水中 | 若溴水褪色,则有乙烯生成 |
D | 比较金属铝和氧化铝熔点的高低 | 用坩埚夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝箔熔化但不滴落,说明金属铝的熔点比氧化铝低 |
 。下列实验操作中,温度计使用错误的是( )
。下列实验操作中,温度计使用错误的是( ) | | | | |
| A.分离碘的四氯化碳 | B.制备乙烯 | C.测定中和反应热 | D.测定CCl4的沸点 |
- 下列做法中,不符合安全用电要求的是 A.家用电器的金属外壳要接地线 B.使用测电笔时,手不能接触笔尖金属体
- 2010年9月27日,“穿越号”盾构机历经720个日夜、4 250米的掘进,顺利到达黄河南岸。至此,全长19.3千米的中
- 写出下列化学符号的意义或题目所要求的化学符号. (1)2Cl (2)2个氮分子 (3)Al3+ (4)五氧
- 下列反应是吸热反应的是A.碳酸钙受热分解 B.乙醇燃烧 C.铝粉与氧化铁粉末反应
- 苏格拉底坐牢时,听到有一犯人在唱一首新歌,就要求教他唱。唱歌的犯人很吃惊:“您就要被处决了,为什么还要学唱新歌啊?”这个
- 两汉与秦朝对匈奴采取的相同措施不包括( ) A.修建防御工事 B.和亲与互市 C.进行战争
- 我国地大物博,分为四大区域,对四大区域的有关叙述正确的是 ( ) A.甲区域与两个国家接壤
- 已知函数,若的解集为,则下列说法正确的是:() A. B. C. D. 必与异号
- . Are you suggesting that I _____ too old for the job? A.
- 假定你是中学生李华。美国一个中学校长代表团即将访问你校并出席英语周的一项活动。请根据写作要点和写作要求写一篇欢迎词。写作
- Mydemand is that the information_______ in my report _____
- 读下图,完成有关该图所示地区的叙述正确的是A.该地为自给农业 B.该地位于我国南方地区C.
- Tom works very hard. His brother, ______,doesn’t do anything
- 把铁片放入下列溶液中,铁片溶解,但没有气体沉淀放出的是 A、稀硫酸 B、 CuSO4溶液 C、Fe2(S
- _______ are the days when the teachers were looked down upon
- I have just heard on the radio that Nanjing Road is jammed
- 鸟类的生殖和发育比昆虫高等,主要表现在 ( ) A.体内受精 B.非变态发育 C.卵生
- 下列周恩来参加的外交活动,按时间先后排列正确的是①出席万隆会议 ②会晤日本首相田中角荣 ③会见美国总统尼克松 ④参加
- 直流电池组的电动势为E,内电阻为r,用它给电阻为R的直流电动机供电,当电动机正常工作时,电动机两端的电压为U,通过电动机
- Afterthe earthquake, the police ______ the ruins day after

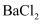 溶液,再加入稀盐酸
溶液,再加入稀盐酸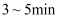 , 冷却后加入新制
, 冷却后加入新制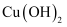 悬浊液加热煮沸
悬浊液加热煮沸