常见化学电源的种类及其工作原理 知识点题库
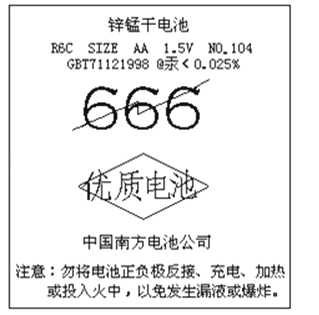
(1)该电池的种类是 (填序号).
①干电池 ②蓄电池 ③燃料电池
(2)该电池含有的金属元素中毒性最大的是 (写元素符号).
(3)该电池的使用和性能,说法正确的是
A.该电池可应用于闹钟、收音机、照相机等
B.该电池可充电后反复使用
C.该电池使用后不能投入火中,应埋入地下以防污染环境.
 2PbSO4+2H2O,现设计如图1所示装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时铁电极的质量减小11.2g.请回答下列问题:
2PbSO4+2H2O,现设计如图1所示装置进行电解(电解液足量),测得当铅蓄电池中转移0.4mol电子时铁电极的质量减小11.2g.请回答下列问题: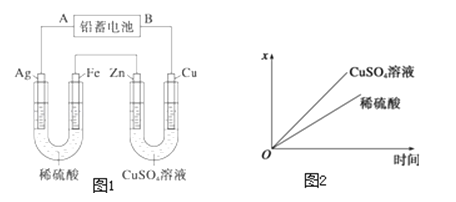
(1)A是铅蓄电池的 (填“正”或“负”)极,铅蓄电池的正极反应式为
(2)Ag电极上的反应式为 ,析出的物质共 g.
(3)Cu电极上的反应式为 ,CuSO4溶液的浓度 (填“减小”、“增大”或“不变”).
(4)如图2表示电解时某个量(纵坐标x)随时间变化的曲线,这个量x最有可能表示的是(填序号).
a.两个U形管中析出的气体体积
b.两个U形管中阳极质量的减少量
c.两个U形管中阴极质量的增加量.
-
(1) 电池正极发生的电极反应为;
-
(2) SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2 , 有Na2SO3和NaCl生成. 如果把少量水滴到SOCl2中,实验现象是,反应的化学方程式为.
①锌为正极,石墨为负极②锌为负极,石墨为正极③工作时,电子由石墨极经过外电路流向锌极④长时间连续使用时,内装糊状物可能流出腐蚀用电器.
 Li2S2O4 . 下列说法正确的是( )
Li2S2O4 . 下列说法正确的是( )
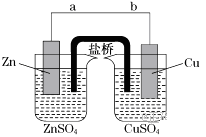
按照实验步骤依次回答下列问题:
-
(1) 导线中电流方向为(用a、b表示)。
-
(2) 原电池的正极为
-
(3) 写出装置中铜电极上的电极反应式:;
-
(4) 若装置中铜电极的质量增加32 g,则导线中转移的电子数目为;
-
(5) 装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,盐桥中的K+向(填“左侧”或“右侧”)烧杯移动
Pb(s) + PbO2(s) + 2H2SO4(aq)  2PbSO4(s) + 2H2O(l)
2PbSO4(s) + 2H2O(l)
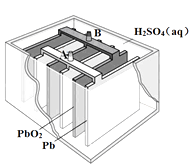
下列说法错误的是( )
 Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是( )
Cd(OH)2 + 2Ni(OH)2。有关该电池的说法正确的是( )
I.有人提出利用H2还原CO2使其转化为有机化工的主要原料乙烯。
-
(1) 查阅资料:H2的燃烧热为285.8kJ/mol,C2H4的燃烧热为l41lkJ/mol,1molH2O(1)转化为H2O(g)需吸收44kJ的热量。则反应

△H=kJ/mol。
-
(2) 下图是探究不同温度对CO2的转化率和催化剂的催化效率影响的示意图。
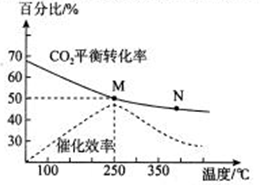
①生产中通常选用的温度最好是,理由是。
②图中表示的化学平衡常数:MN(填>、=、<)
③250℃时,在2L密闭容器中分别充入6molH2和2 molCO2 , 到达平衡时体系中C2H4的体积分数为。
-
(3) Ⅱ.CO在一定条件下,能与H2合成二甲醚:
 。
。 在1L的密闭容器中分别充入2.5molH2与 bmol CO2发生反应,在不同温度下达到平衡状态时测得实验数据如下表:
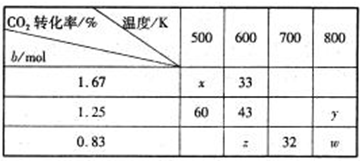
①到达平衡时若升高温度,则上述平衡方向移动(填“正反应”或“逆反应”)。
②转化率:xy(填>、=、<)
-
(4) 新型高效的二甲醚燃料电池工作时总反应式:
 。
。 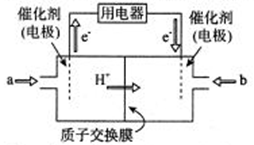
①该电池的负极是(填a或b),负极电极反应式为;
②利用该电池冶铝,若制得金属铝54g理论上消耗二甲醚g。
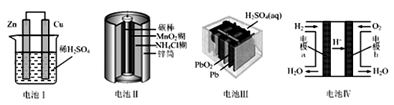

 向Cu电极方向移动,溶液中
向Cu电极方向移动,溶液中  减小
B . 乙:正极的电极反应式为
减小
B . 乙:正极的电极反应式为  C . 丙:锌筒作负极,发生氧化反应,锌筒会变薄
D . 丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
C . 丙:锌筒作负极,发生氧化反应,锌筒会变薄
D . 丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
- 现有常温下的四种溶液(如下表),下列有关叙述中正确的是A.在③④中分别加入适量的醋酸铵晶体后,③的pH减小,④的pH不变
- 下列有关实验的现象或反应,与原理解释符合因果关系的是
- “The Lord of the Rings”, one of the best sellers in the new
- 根据所学知识判断下列几种叙述中正确的是() ①胸腺在免疫中的作用是先分化出造血干细胞,进而分化出T细胞 ②过敏反应是指已
- 2009年9月21日起,北京市在全国率先启动国庆庆典相关人员甲型H1N1流感疫苗接种,同时实施预防接种后不良反应主动监测
- 2009年亚太经合组织领导人非正式会议将于11月在新加坡举行。会议的主题是“持续增长,区域联合”。会议将会对世界经济金融
- 角膜接触镜,俗称隐形眼镜。目前大量使用的软质隐形眼镜,常用以下哪种材料制成( )A.有机玻璃
- 阅读理解;阅读下面语言材料,然后按文后要求做题。 Once upon a time, there was a ha
- 航空摄影人员从高空给城市拍照,若所用的照相机镜头的焦距为80㎜,则胶卷与镜头的距离应 (填“大于”或“小于
- 在xoy平面内,x轴的上方有匀强磁场,磁感应强度为B,方向如图所示,x轴的下方有匀强电场,电场强度为E,方向与y轴的正方
- (09天河区五校期末联考)细胞膜上与细胞识别有密切关系的物质是A.磷脂 B.蛋白质
- 下列说法正确的是 ( ) A.二氧化硅溶于水显酸性 B.二氧化碳通入水玻璃中可以得到原硅酸 C.因为高温时二氧化硅
- 读图,甲、乙、丙、丁四个地区的气温雷达图和降水柱状图,有关甲乙丙丁四个地区的气候特征叙述,正确的是( ) A
- 许多物质在溶液中都以离子形式存在。我们熟悉的复分解反应就是溶液中离子间结合得到水、气体或沉淀的一类化学反应。如:氢氧化钠
- 39.有关物质进出细胞的说法正确的是( ) A.细胞膜和液泡膜都具有控制物质进出的功能 B.胞吞和胞吐都要
- 下列关于自由落体运动的说法,正确的是:A.初速度为零的竖直向下的运动就是自由落体运动B.只在重力作用下的竖直向下的运动就
- 已知,若,则的值是( ) A. B.或 C.,或 D.
- 传说,从一株苹果树上坠落的苹果,激发牛顿发现了万有引力定律.2010年5月14日,英国皇家学会将这株苹果树的一截长10c
- 一物体的运动方程为s=2tsint+t,则它的速度方程为()A. v=2sint+2tcost+1 B. v=2sint
- 【甲】若夫霪雨霏霏,连月不开,阴风怒号,浊浪排空;日星隐耀,山岳潜形;商旅不行,樯倾楫摧;薄暮冥冥,虎啸猿啼。登斯楼也,



