测定溶液pH的方法 知识点题库
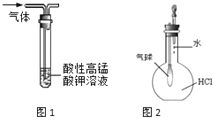
(1)现欲测定100℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显 色,溶液呈 性(填“酸”、“碱”或“中”).
(2)若用pH计测定,则pH 7.0(填“>”、“<”或“=”),溶液呈 性(填“酸”、“碱”或“中”).
①用pH试纸,测得氯水的pH为2
②用量筒、试管、胶头滴管、玻璃棒、蒸馏水和pH试纸,可鉴别pH相等的硫酸和醋酸
③分液时,分液漏斗中的下层液体从下口放出,上层液体从上口倒出
④将三氯化铁溶液蒸干,可制得无水三氯化铁
⑤可用渗析的方法除去淀粉中混有的少量氯化钠杂质
⑥在做中和热测定的试验,温度计至少使用2次.
①用稀盐酸洗涤盛放过石灰水的试剂瓶
②配制浓硫酸和浓硝酸的混合酸时,将浓硝酸沿器壁慢慢加入到浓硫酸中,并不断搅拌;
③用pH试纸测得氯水的pH为2;
④用稀硝酸清洗做过银镜反应实验的试管;
⑤浓硝酸保存在棕色细口瓶中;
⑥将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡
⑦某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+ .
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向苯酚溶液中滴加少量浓溴水、振荡,无白色沉淀。 | 苯酚浓度小 |
| B | 测定醋酸溶液pH,用玻璃棒蘸取溶液,点在pH试纸上,试纸显红色。 | 醋酸溶液显酸性 |
| C | 向20%蔗糖溶液中加入少量稀H2SO4 , 加热;再加入银氨溶液;未出现银镜。 | 蔗糖未水解 |
| D | 向某黄色溶液中加入淀粉KI溶液,溶液呈蓝色。 | 溶液中含Br2 |
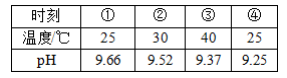
实验过程中,取①、④时刻的溶液,加入盐酸酸化的 BaCl2 溶液做对比实验,④产生白色沉淀多。下列说法错误的是( )
| 序号 | 实验目的 | 实验方案 | 所选玻璃仪器 |
| A | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 | 酒精灯、烧杯、玻璃棒 |
| B | 证明HClO与CH3COOH的酸性强弱 | 同温下用pH试纸测定浓度为0.1mol/L'NaClO溶液和0.1mol/LCH3COONa溶液 | 玻璃棒、玻璃片 |
| C | 检验蔗糖水解产物且具有还原性 | 向蔗糖容易中加入几滴稀硫酸,水浴加热5分钟,再向其中加入新制银氨溶液,水浴加热 | 试管、烧杯、酒精灯、滴管 |
| D | 配制1L1.6%的硫酸铜溶液(其密度为1.0g/mL) | 将25gCuSO4·5H2O溶解在975g水中 | 烧杯、量筒、玻璃棒 |
-
(1) 该学生的操作是(填“正确的”或“错误的”),理由是。
-
(2) 若用此方法分别测定c(H+)相等的盐酸和醋酸溶液的pH,误差较大的是。
-
(3) 该学生用此方法测定下列溶液的pH,其中测定结果无误差的是________(填序号)A . NaOH溶液 B . CH3COONa溶液 C . NaCl溶液 D . NaHSO4溶液
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向5mL浓度均为1mol·L-1的NaOH溶液中先滴入2滴1mol·L-1 MgCl2 , 再滴入2滴1mol·L-1FeCl3溶液 | 先有白色沉淀生成,再有红褐色沉淀生成 | Ksp[Fe(OH)3]<Ksp[Mg(OH)2] |
| B | 向盛有2mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液 | 黄色变为浅绿色 | 维生素C 具有还原性 |
| C | 向BaCl2溶液中通入NH3和SO2 | 无沉淀生成 | H2SO3不能与BaCl2反应生成BaSO3和HCl |
| D | 用 pH 试纸分别测量 NaCN 和 NaClO 溶液的 pH | NaClO 的碱性强 | Ka(HCN)>Ka(HClO) |
| 实验目的 | 实验设计 | |
| A | 检验溶液中 | 取少量待测液,滴加 |
| B | 净化实验室制备的 | 气体依次通过盛有饱和 |
| C | 测定 | 将待测液滴在湿润的pH试纸上,与标准比色卡对照 |
| D | 工业酒精制备无水乙醇 | 工业酒精中加生石灰,蒸馏 |
-
(1) 已知常温常压下,空气中的CO2溶于水,达到平衡时,溶液的pH=5.60,c(H2CO3)=1.5×10-5mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3⇌HCO
 + H+的平衡常数K1=。(已知10-5.60=2.5×10-6)
+ H+的平衡常数K1=。(已知10-5.60=2.5×10-6)
-
(2) 已知H2CO3的第二级电离常数Ka2=5.6×10-11 , HClO的电离常数K=3.0×10-8 , 写出下列所发生反应的离子方程式:
a.少量Cl2通入过量的Na2CO3溶液中:。
b.少量CO2通入过量的NaClO溶液中:。
-
(3) 人体血液里主要通过碳酸氢盐缓冲体系(
 )维持pH稳定。已知正常人体血液在正常体温时,H2CO3的一级电离常数Ka1=10-6.1 ,
)维持pH稳定。已知正常人体血液在正常体温时,H2CO3的一级电离常数Ka1=10-6.1 ,  ≈
≈ 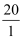 ,1g2=0.3。由题给数据可算得正常人体血液的pH约为,当过量的酸进入血液中时,血液缓冲体系中
,1g2=0.3。由题给数据可算得正常人体血液的pH约为,当过量的酸进入血液中时,血液缓冲体系中  的值将(填“变大、变小、不变”)。
的值将(填“变大、变小、不变”)。
-
(4) NaOH吸收CO2后某种产物的水溶液在pH从0至14的范围内H2CO3、HCO
 、CO
、CO  三种成分平衡时的组成分数如图所示,若用CO2和NaOH反应制取NaHCO3 , 宜控制溶液的pH为之间
三种成分平衡时的组成分数如图所示,若用CO2和NaOH反应制取NaHCO3 , 宜控制溶液的pH为之间 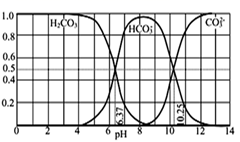
①氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂;
②测定新制氯水的  时,先用玻璃棒蘸取液体滴在
时,先用玻璃棒蘸取液体滴在  试纸上,再与标准比色卡对照;
试纸上,再与标准比色卡对照;
③用米汤直接检验食用盐中是否含有碘元素;
④  在5.6~7.0之间的降水通常称为酸雨;
在5.6~7.0之间的降水通常称为酸雨;
⑤加入 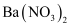 溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有
溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有  存在;
存在;
⑥  通入紫色石蕊试液,溶液先变红后褪色;
通入紫色石蕊试液,溶液先变红后褪色;
⑦配制一定物质的量浓度的氢氧化钠溶液,用烧杯称量后加蒸馏水溶解,未冷却到室温便转移到容量瓶中,导致结果偏高;
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质可用稀盐酸洗涤;
⑨蒸干  溶液可得纯净的无水氯化铝;
溶液可得纯净的无水氯化铝;
实验目的 | 操作步骤及现象 | |
A | 探究浓度对化学平衡的影响 |
|
B | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取NaClO溶液滴于试纸的中部,与标准比色卡对比得出结论 |
C | 证明酸性: | 向 |
D | 将 | 最终得到白色固体,成分为纯净的 |
- 蜜蜂是一种群聚的益虫,蜜蜂的筑巢、语言,以及采粉酿蜜都引起人们极大的兴趣。 (1)蜜蜂的侦查蜂在发现蜜源后,回到蜂窝内通
- 在静水中划船的速度是每分钟40米,水流的速度是每分钟20米.如果从岸边O点出发,沿着垂直于水流的航线到达对岸,试问小船的
- 19.下面是一篇论文的摘要,请根据其内容提取四个关键词。 李商隐的诗歌因晦涩难懂的含义和缥缈朦胧的美感广为人知,他的诗广
- 已知,且,则.
- 常温下,下列各组离子在指定溶液中一定能大量共存的是() A.1.0 mol·L-1 KNO3溶液:H+、Fe2+、SCN
- 除去下列物质中混有的少量杂质(括号内为杂质),所用方法正确的是 () A.CaCO3固体(CaO固体)——高温煅烧 B.
- 在明清之际出现了反对君主专制的进步思想,根本原因是 A、知识分子具有忧国忧民思想 B、封建专制统治的残酷压
- 苍耳果实表面的钩刺可以挂在动物的皮毛上,这说明动物在自然界中的作用是()A. 维持生态平衡 B. 对植物生活造成危害 C
- 下列各组物质中,全部属于纯净物的是()A. 福尔马林、白酒、食醋 B. 汽油、淀粉、酚醛树脂 C. 石炭酸、盐酸、冰醋酸
- 5.下列离子方程式书写正确的是()A.稀硫酸滴到铁片上: 2Fe +6 H+=2 Fe3++ 3H2↑ B.硫酸铜溶液与
- 下列说法中,不合理的是() A.饭后休息一段时间再做剧烈运动,有利于对食物的消化 B.青少年时期应该多吃些含蛋白质、钙、
- 某同学在探究牛顿第二定律的实验中,在物体受外力不变时,改变物体的质量,得到数据如下表所示。 实验次数物体质量m/kg物体
- 在社会公众的强烈呼吁下,近来国务院下属98个部门中的绝大部分已向社会公开了他们的“三公”经费(公车购置费、公务招待费、出
- 如图1-28(原图1-40)所示,在一粗糙水平面上有两个质量分别为m1和m2的木块1和2,中间用一原长为、劲度系数为k的
- Tom __________ in the library every night over the last thre
- 把函数y=sinx(x∈R)的图象上所有的点向左平行移动个单位长度,再把所得图象上所有点的横坐标缩短到原来的倍(纵坐标不
- 已知函数f(x)=x+2x,g(x)=x+lnx,h(x)=x--1的零点分别为x1,x2,x3,则x1,x2,x3的大
- 下列情况:①煤燃烧;②工业废气任意排放;③燃放鞭炮;④燃油汽车排放的尾气;⑤氢能源汽车排放的尾气,会引起空气污染的是()
- 读“香港、广州、兰州、乌鲁木齐和重庆5城市的气候资料表”,关于城市④的叙述,正确的是 ① ② ③
- If the weather had been better, we could have had a picnic.
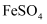 是否被氧化
是否被氧化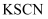 溶液,观察溶液颜色变化
溶液,观察溶液颜色变化
 溶液、浓
溶液、浓  的洗气瓶
的洗气瓶 溶液的pH
溶液的pH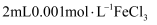 溶液与
溶液与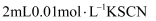 溶液混合后平分到两支试管,一支加入
溶液混合后平分到两支试管,一支加入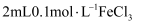 溶液,另一支加入
溶液,另一支加入 , 第一支试管中溶液颜色较深
, 第一支试管中溶液颜色较深
 溶液中滴入过量
溶液中滴入过量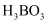 溶液,无气泡冒出
溶液,无气泡冒出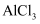 溶液加热蒸干
溶液加热蒸干


