极性键和非极性键 知识点题库
下列化学式表示的物质中,属于离子晶体并且含有非极性共价键的是( )
A . BaCl2
B . Na2O2
C . H2O2
D . NH4Cl
下列物质 ①H2O2②NaOH ③NH4NO3 ④CH2=CH2
(1)上述物质中存在非极性键的物质是 (填序号)
(2)既存在离子键又存在共价键的物质是 (填序号)
下列叙述正确的是( )
A . 分子晶体中的每个分子内一定含有共价键
B . 原子晶体中的相邻原子间只存在非极性共价键
C . 离子晶体中可能含有共价键
D . 金属晶体的熔点和沸点都很高
下列叙述中正确的是( )
A . NH3、CO,CO2都是极性分子
B . BF3、SiCl4都是含有极性键的非极性分子
C . HF,HCl,HBr、Hl的稳定性依次增强
D . CS2、H2O,C2H2都是直线型分子
根据所学知识填空:
-
(1) 在①CO2 , ②NaCl,③Na,④Si,⑤CS2 , ⑥金刚石,⑦(NH4)2SO4 , ⑧乙醇中,由极性键形成的非极性分子有(填序号,以下同),含有金属离子的物质是,分子间可形成氢键的物质是,属于离子晶体的是,属于原子晶体的是,①~⑤五种物质的熔点由高到低的顺序是
-
(2) A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS2 , 不溶于水
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3500℃
试推断它们的晶体类型:A.;B.;C.;D..
-
(3) 下图中A~D是中学化学教科书上常见的几种晶体结构模型,请填写相应物质的名称:
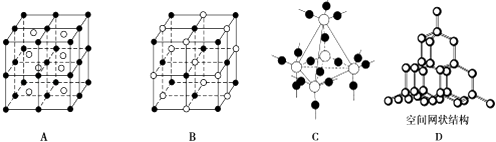
A.;B.;C.;D..
下列说法中正确的是( )
A . 含有共价键的化合物一定是共价化合物
B . 所有物质之间均存在化学键
C . 由非金属元素可以组成离子化合物
D . 不同元素组成的多原子分子里的化学键一定为极性键
下列关于粒子结构的描述不正确的是( )
A . H2S和NH3均是价电子总数为8的极性分子
B . OH﹣和HF均是含有极性键的10电子粒子
C . CHCl3和CCl4均是四面体构型的非极性分子
D . 1 mol D216O(重水)中含中子、质子、电子各10NA(NA代表阿伏加德罗常数的值)
下列物质中,只含有非极性共价键的是( )
A . NH3
B . MgO
C . CO2
D . Cl2
下列物质中,既含极性键又含配位键的离子晶体是( )
A . Ba(OH)2
B . H2SO4
C . (NH4)2SO4
D . CaF2
下列叙述中正确的是( )
A . CO、CO2都是极性分子
B . H2O2、C2H2都是直线型分子
C . CH4、CCl4都是含有极性键的非极性分子
D . BF3、NCl3都是平面三角形分子
下列变化过程中,原物质分子内共价键被破坏,同时有离子键形成的是( )
A . 盐酸与氢氧化钠溶液反应
B . 氯化氢溶于水
C . 氯化氢与氨气反应生成氯化铵固体
D . 锌与稀硫酸反应
下列物质中:①MgCl2②金刚石③NaCl④H2O⑤Na2O2⑥O2⑦H2SO4⑧CO2⑨NH4Cl⑩Ne。只含离子键的是,只含共价键的是,既含离子键又含共价键的是,不存在化学键的是,属于离子化合物的是,属于共价化合物的是。
下列物质中,含非极性共价键的化合物是( )
A . MgCl2
B . Na2O2
C . O2
D . NaOH
下列关于丙烯(结构简式为CH3-CH=CH2)的说法中正确的是( )
A . 丙烯分子中有8个σ键、1个π键
B . 丙烯分子中3个碳原子都是sp3杂化
C . 丙烯分子中不存在非极性共价键
D . 丙烯分子中所有原子都共平面
X、Y、Z、W为原子序数依次增大的短周期主族元素,X和Y形成的简单化合物常用作制冷剂,Z的一种氧化物与其氢化物在水溶液中反应产生沉淀,下列叙述正确的是( )
A . 简单离子半径:W>Z>Y>X
B . W的含氧酸的酸性比Z的含氧酸的酸性强
C . Y与X形成的化合物中一定只含有极性共价键
D . W的单质可以从Y的简单氢化物中置换出Y的单质
甲酸(HCOOH)被认为是一种有前途的储氢化合物。在催化剂作用下,甲酸分解制氢的过程如图所示。
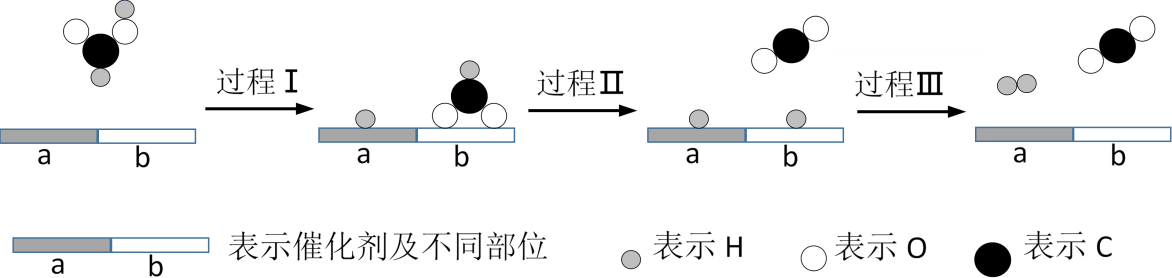
下列分析错误的是( )
A . 过程I,若用2HCOOH代替HCOOH,则在催化剂a处吸附的是2H
B . 过程II,生成的CO2分子是直线型结构
C . 过程Ⅲ,形成非极性共价键
D . HCOOH分解制氢的总反应为:HCOOH CO2↑+H2↑
CO2↑+H2↑
 CO2↑+H2↑
CO2↑+H2↑
下列说法正确的是( )
A . 过氧化氢分子中既含极性键又含非极性键
B . 干冰气化时吸收的热量用于克服分子内碳、氧原子间的作用力
C . 氯化氢和氯化钠溶于水都能电离出Cl- , 所以氯化氢和氯化钠均是离子化合物
D . CO2和H2O分子中所有原子的最外电子层都具有8电子的稳定结构
下列说法正确的是( )
A .  能与
能与 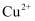 以配位键结合
B .
以配位键结合
B .  与
与  分子的空间结构均为四面体形
C .
分子的空间结构均为四面体形
C .  的沸点比
的沸点比  的高,是因
的高,是因  分子间存在氢键
D .
分子间存在氢键
D .  比
比 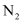 更易溶于水,是因
更易溶于水,是因 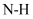 是极性键而
是极性键而 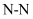 是非极性键
是非极性键
 能与
能与 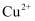 以配位键结合
B .
以配位键结合
B .  与
与  分子的空间结构均为四面体形
C .
分子的空间结构均为四面体形
C .  的沸点比
的沸点比  的高,是因
的高,是因  分子间存在氢键
D .
分子间存在氢键
D .  比
比 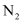 更易溶于水,是因
更易溶于水,是因 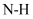 是极性键而
是极性键而 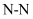 是非极性键
是非极性键
2021年9月24日《科学》杂志发表了中国科学家的原创性重大突破——首次在实验室实现 到淀粉的全合成。其部分合成路线如下。
到淀粉的全合成。其部分合成路线如下。
 到淀粉的全合成。其部分合成路线如下。
到淀粉的全合成。其部分合成路线如下。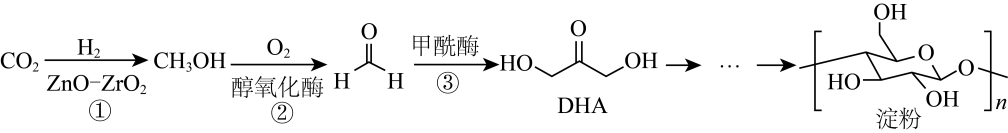
下列说法正确的是( )
A . DHA和淀粉中碳原子的成键方式完全相同
B . 反应①中有极性键和非极性键的断裂与生成
C . 升高温度一定会加快反应②的反应速率
D . 反应③属于加成反应
下列物质中既含有非极性键,又含有极性键的是( )
A . CCl4
B . C2H4
C . NaOH
D . H2O
最近更新
- 下列各项与巴黎公社革命爆发无关的是 A.生产力发展的要求 B.普鲁士对法国的侵略 C.临时政府的卖国行为 D.临时政府企
- 构建知识网络是一种重要的学习方法。某同学对物质组成与结构方面的知识进行归纳。请你参与填写空白,完成设计。 (1)物质、元
- 下图的四支试管甲、乙、丙、丁各装入2毫升淀粉糊,再将四支试管分别加入不同的物质,振荡使其反应充分,据图回答。(1)鉴定淀
- 下列各句中,没有语病的一句是( ) A.这次问题奶粉事件对中国的乳品行业打击相当沉重,据初步统计,三鹿、蒙牛、伊利三
- 把下面的文言文翻译成现代汉语。 孟子曰:“君子有三乐,而王天下不与存焉①。父母俱存,兄弟无故②,一乐也;仰不愧于天,俯不
- 如图所示,水平面上,质量为m的物块受到与水平方向夹角θ的推力F的作用(θ≠0),物块做匀速直线运动.现将F撤去,设此后物
- 2008年9月1日,新学期开学第一天,全国中小学生迎来“史上最牛的一节课”:以“知识守护生命”为主题的安全公益课《开学第
- 关于垃圾食品的阅读【垃圾食品】垃圾食品,一般情况下是指高热量食品,这些食品很容易使人发胖,而营养素却不足。世界卫生组织公
- 169. Many newly found old things ______ in the museum this m
- 某英文报社举办以“I Like Reading”为主题的征文活动,你打算投稿。请根据以下要点写一篇短文:. 你为什么喜欢
- It was already past midnight and only three young men ____ i
- 读表3(表中①、②、③、④代表西北干旱区、黄淮平原区、东北低产区和南方高产区等我国四类商品粮基地),关于①、②、③、④所
- 质量为600g的物块A放入水中,静止后有的体积露出水面,则物块A的体积是 cm3;如果在物块A
- 有人认为人类实际上是一架缓慢氧化着的高级机器,人体在生命活动过程中需要不断补充燃料,按照这种观点,你认为人们摄入下列物质
- 阅读下面的文字,完成后面问题。 清兵卫与葫芦 (日)志贺直哉 这是一个叫清兵卫的孩子跟葫芦的故事。自从发生了这件事以后,
- 如图为某大洲矿产资源分布示意图,据图回答问题。【小题1】该大洲的石油资源主要分布在A.东部沿海和西部沿海B.西部沿海和北
- 阅读下面的消息,回答问题。(4分) 万里挑一定“芳名” 2009年9月22日,经过一个月热闹的征名活动,新乡市人民公园动
- 《西藏民主改革50年》白皮书回顾了西藏实行民主改革50年的历史进程和巨变。当前的西藏经济发展、社会进步、文化繁荣、民生改
- 例葡萄糖在毛霉细胞质内分解至丙酮酸的过程中,下列叙述正确的是 A.在线粒体中进行的无氧呼吸 B.需在有氧条件下进
- 2008年9月28日,在太空遨游两天多的“神舟七号”飞船返回舱成功着陆,中国“神舟七号”载人航天任务圆满完成。这反映出的



