配合物的成键情况 知识点题库
-
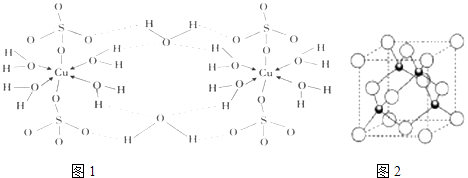
(1) 科学家通过X射线推测胆矾结构示意图如图1所示,
①写出基态Cu原子的核外电子排布式;金属铜采用下列(填字母代号)堆积方式
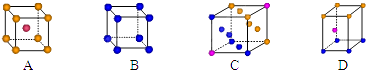
②胆矾中含有的微粒间作用力有(填字母代号).
a.离子键 b.极性键 c.金属键 d.配位键 e.氢键 f.非极性键
③铜离子形成胆矾中配离子的离子方程式为:;
-
(2) 合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac﹣表示CH3COO﹣),其反应是:[Cu(NH3)2]Ac+CO+NH3⇌[Cu(NH3)3]Ac.CO[醋酸碳基三氨合铜(Ⅰ)]△H<0
①C、N、O三种元素的第一电离能由小到大的顺序为
②氨分子中N原子的杂化方式为
-
(3) 铜的化合物种类也很多,其常见价台为+1,+2价.如CuO、Cu2O、CuH等,如图2是同的一种氯化铜的晶胞结构,则它的化学式是.
-
(1) 镍元素基态原子的电子排布式为,3d能级上的未成对的电子数为.
-
(2) 硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液.
①在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为,提供孤电子对的成键原子是.
②氨的沸点(“高于”或“低于”)膦(PH3),原因是;氨是分子(填“极性”或“非极性”),中心原子的轨道杂化类型为.
-
(3) 单质铜及镍都是由键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是
-
(4) Ni(CO)4分解为Ni和CO可制得高纯度的Ni粉,这个反应中形成的化学键是.
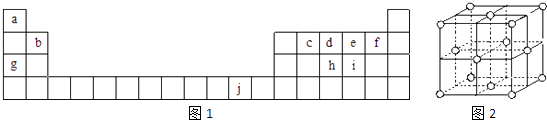
用化学用语回答下列问题:
-
(1) 写出元素f的基态原子核外电子排布式.
-
(2) 在c6a6分子中,元素c为杂化,该分子是分子(填“极性”或“非极性”).
-
(3) ci2分子的电子式为,ci2与ce2比较,沸点较高的是(写分子式).
-
(4) 第一电离能:hi;电负性:gb(填“>”、“<”或“=”).
-
(5) 下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 .A . j位于元素周期表中第四周期、ⅠB族,属于ds区元素 B . d的基态原子中,2p能级为半充满,属于p区元素 C . 最外层电子排布式为4s1 , 一定属于ⅠA族 D . 最外层电子排布式为ns2np1 , 该元素可能是ⅢA族或ⅢB族
-
(6) 将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是,写出蓝色沉淀溶解在氨水中的离子方程式.
-
(7) j的金属晶体的晶胞如图2所示,则一个晶胞中j原子的个数是个.
-
(1) 配制FeSO4溶液时,需加入稀硫酸,其目的是
-
(2) 写出CoCl2与氯水反应的化学方程式
-
(3) Co2+和Fe3+均可与KSCN溶液发生相似的反应,向CoCl2溶液中加入KSCN溶液,生成某种蓝色离子,该离子中钴元素的质量分数约为20%。则该离子的化学式为。
-
(4) 碳酸镍可用于电镀、陶瓷器着色等。镍矿渣中镍元素的主要存在形式是Ni(OH)2和NiS,从镍矿渣出发制备碳酸镍的反应如下:
先向镍矿渣中加入稀硫酸和NaClO3浸取出Ni2+ , 反应的离子方程式有①②NiS+ ClO3-+H+-Ni2++S+Cl-+H2O(未配平),此反应中还原产物与氧化产物的物质的量比为。再加入Na2CO3溶液沉镍,即制得碳酸镍,检验Ni2+是否沉淀完全的方法
-
(1) 准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过方法区分晶体、准晶体和非晶体。
-
(2) 基态Cu原子最高能层符号,Cu位于周期表区;新制备的Cu(OH)2可将丙醛(CH3CH2CHO)氧化成丙酸,而自身还原成Cu2O,Cu2O中Cu元素的化合价为。1mol丙醛分子中含有的σ键的数目为,丙酸的沸点明显高于丙醛,其主要原因是。
-
(3) 已知:
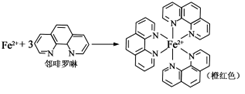
①Fe2+与邻啡罗啉形成的配合物(形成过程如图)中,配位体为,配位原子数为。
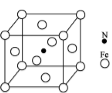
②铁能与氮形成一种磁性材料,其晶胞结构如图,则该磁性材料的化学式为。
③尿素(H2NCONH2)可用于制有机铁肥,主要代表有[Fe(H2NCONH2)6](NO3)3[三硝酸六尿素合铁(Ⅲ)]。尿素分子中C、N原子的杂化方式分别是、;与NO3-互为等电子体的一种化合物是(写化学式)。
-
(4) Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为,列式表示Al单质的密度g•cm﹣3(不必计算出结果)。
-
(1) 铜或铜盐的焰色反应为绿色,该光谱是(填“吸收光谱”或“发射光谱”)。
-
(2) 基态Cu原子中,核外电子占据的最低能层符号是,其价电子层的电子排布式为,Cu与Ag均属于IB族,熔点:CuAg (填“>”或“<”)。
-
(3) [Cu(NH3)4]SO4 中阴离子的立体构型是;中心原子的轨道杂化类型为,[Cu(NH3)4]SO4 中Cu2+与NH3之间形成的化学键称为。
-
(4) 用Cu作催化剂可以氧化乙醇生成乙醛,乙醛再被氧化成乙酸,等物质的量的乙醛与乙酸中σ键的数目比为。
-
(5) 氯、铜两种元素的电负性如表: CuCl属于(填“共价”或“离子”)化合物。
元素
Cl
Cu
电负性
3.2
1.9
-
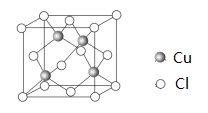
(6) Cu 与Cl 形成某种化合物的晶胞如图所示,该晶体的密度为ρ g·cm-3 , 晶胞边长为a cm,则阿伏加德罗常数为(用含ρ、a的代数式表示)。
-
(1) 铬元素在元素周期表的位置,基态Cu原子的核外电子排布式为 。
-
(2) 形成铬锆铜合金的元素中,其基态原子未成对电子数最多的元素是。
-
(3) 配合物[Cr(NH3)4(H2O)2]Cl3中的配位数是 ,1 mol配合物中所含σ键的数目为。
-
(4) 下表是Fe与Cu的部分电离能数据,解释I2(Cu)大于I2(Fe)的主要原因是。
元素
Fe
Cu
第一电离能I1 (kJ/mol)
759
746
第二电离能I2 (kJ/mol)
1 561
1 958
-
(5) 硫酸铜(CuSO4)是一种重要的工业原料,写出其阴离子
 的空间构型,与其互为等电子体的分子为。
的空间构型,与其互为等电子体的分子为。
-
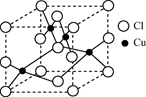
(6) 铜与氯形成的晶胞如下图所示,写出该晶胞的化学式。
-
(1) 水分子中氧原子在基态时核外电子排布式为
-
(2) 写出与H2O分子互为等电子体的微粒(填2种)。
-
(3) 水分子在特定条件下容易得到一个H+ , 形成水合氢离子(H3O+)。
下列对上述过程的描述不合理的是______
A . 氧原子的杂化类型发生了改变 B . 微粒的形状发生了改变 C . 微粒的化学性质发生了改变 D . 微粒中的键角发生了改变 -
(4) 下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。
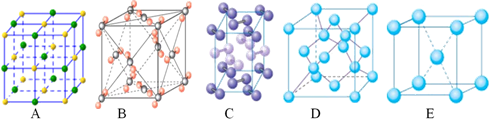
与冰的晶体类型相同的是(请用相应的编号填写)
-
(5) 将白色的无水CuSO4溶解于水中,溶液呈蓝色,是因为生成了一种呈蓝
色的配合离子。请写出生成此配合离子的离子方程式:。
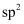 和
和  两种杂化方式
两种杂化方式
-
(1) 肼(N2H4)能与硫酸反应生成N2H6SO4 , N2H6SO4化合物类型与硫酸铵相同,则N2H6SO4内微粒间作用力不存在(填序号)。
a.离子键
b.共价键
c.配位键
d.范德华力
-
(2) ①胆矾CuSO4·5H2O可写成[Cu( H2O)4]SO4·H2O,其结构示意图如图:
胆矾中含有的粒子间作用力是 ( 填序号)。
A.离子键
B.极性键
C.配位键
D.非极性键
②已知CN-与N2互为等电子体,1 mol CN-中π键的数目为。
-
(3) 光化学烟雾中的过氧乙酰硝酸酯( CH3COOONO2 , 简称“PAN")是一种极强的催泪剂,1 mol PAN中含σ键数目为。
-
(1) Mn基态原子的价电子排布式,Ni位于周期表中 区。
-
(2) 根据价电子对互斥理论推测SeO
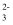 离子的空间构型为 ,SeO2分子中心原子杂化轨道类型是。
离子的空间构型为 ,SeO2分子中心原子杂化轨道类型是。
-
(3) 化合物[Co(NH3)6]Cl3中存在____ 。A . 离子键 B . σ键 C . π键 D . 配位键
-
(4) 一种铜的溴化物的晶胞结构如图所示。
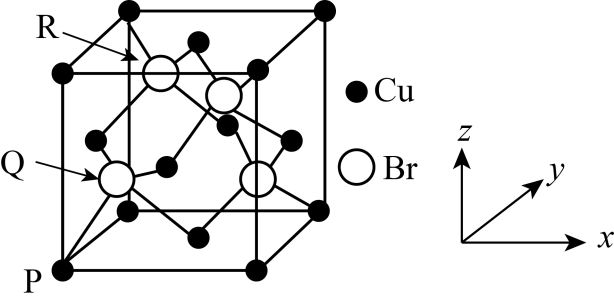
①该溴化物的化学式为 。
②原子坐标参数表示晶体内部各原子的相对位置。上图中各原子坐标参数P为(0,0,0),Q为 (
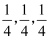 ),
),则R原子的坐标参数为。
③已知该溴化物密度为ρg·cm-3 , Cu原子半径为xpm,Br原子半径为ypm,阿伏加德罗常数为NA , 则该晶胞中原子空间利用率为。(列出计算式)
选项 | 事实 | 解释 |
A | 分别向K3[Fe(CN)6]溶液和Fe(SCN)3溶液中滴加等浓度的氢氧化钠溶液,只有Fe(SCN)3溶液中有黄色沉淀生成 | CN-对Fe3+的配位能力比SCN-更强,溶液中没有Fe3+ |
B | 向碘的四氯化碳溶液中加入适量浓KI溶液,振荡试管,溶液紫色变浅 | c(I-)增大,I2+I- |
C | 向酸式滴定管中加入蒸馏水,打开活塞让水缓缓流下,可看到水呈直线状垂直流入烧杯中。若用头发摩擦过的气球靠近,水流会向一侧偏转 | 水分子中含有极性键,会受到带电物体的吸引 |
D | 向盛有AgCl沉淀的试管中滴入足量1mol/L氨水,振荡,溶液变澄清 | AgCl+2NH3=[Ag(NH3)2]Cl,NH3的N接受电子对 |
-
(1) 基态Fe原子的简化电子排布式为。
-
(2) 因生产金属铁的工艺和温度等因素不同,产生的铁单质的晶体结构、密度和性质均不同。
①用实验测定铁晶体,测得A、B两种晶胞,其晶胞结构如图:
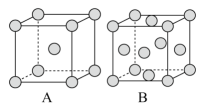
②A、B两种晶胞中含有的铁原子个数比为。
③在A晶胞中,每个铁原子周围与它最近且相等距离的铁原子有个。
-
(3) 常温下,铁不易和水反应,而当撕开暖贴(内有透气的无纺布袋,袋内装有铁粉、活性炭、无机盐、水、吸水性树脂等)的密封外包装时,即可快速均匀发热。利用所学知识解释暖贴发热的原因:。
-
(4) 工业盐酸因含有[FeCl4]-而呈亮黄色,在高浓度Cl-的条件下[FeCl4]-才是稳定存在的。
①[FeCl4]-的中心离子是,配体是;其中的化学键称为。
②取4mL工业盐酸于试管中,逐滴滴加AgNO3饱和溶液,至过量,预计观察到的现象有,由此可知在高浓度Cl-的条件下[FeCl4]-才是稳定存在的。
-
(1) 水体中过量的
 是一种重要污染物,可利用纳米铁粉将其除去。
是一种重要污染物,可利用纳米铁粉将其除去。①基态铁原子核外电子排布式:;铁元素在元素周期表中的位置为,属于区元素。
②相同条件下,向含有
 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图1所示,产生该差异的可能原因为。
的去除速率差异如图1所示,产生该差异的可能原因为。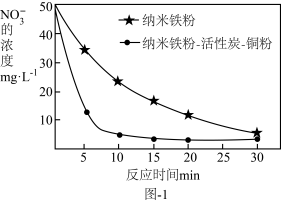
-
(2) 铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图2所示。储氢时,
 分子位于晶胞体心和棱的中心位置。
分子位于晶胞体心和棱的中心位置。①该晶胞中
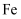 的配位数是。
的配位数是。②该合金储满氢后所得晶体的化学式是。
-
(3) 在生产中,常用
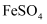 处理
处理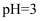 的含
的含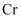 (
(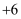 价)废水得到
价)废水得到 和
和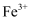 。
。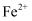 易被氧化为
易被氧化为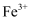 , 请利用核外电子排布的相关原理解释其原因:。
, 请利用核外电子排布的相关原理解释其原因:。
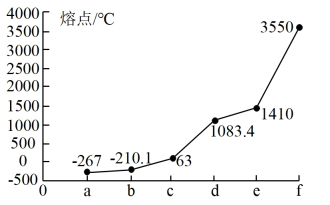
回答下列问题:
-
(1) 图中d单质对应元素基态原子的电子排布式为。
-
(2) 单质a、f对应的元素以原子个数比1∶1形成的分子(相同条件下对
 的相对密度为13)中所含
的相对密度为13)中所含 键和
键和 键的个数比为,其中f原子的杂化轨道类型为。
键的个数比为,其中f原子的杂化轨道类型为。
-
(3) a与b的元素形成的10电子中性分子X的空间构型为;将X溶于水后的溶液滴入到d的硫酸盐溶液中至过量,得到配合物的化学式为,其中d离子的配位数为。
-
(4) e、f单质对应元素的简单气态氢化物的热稳定性(用相应的化学式表示)>,原因是。
-
(5) c与氧元素和碘元素形成的一种晶体是一种性能良好的光学材料,其晶胞为立方体,棱长为0.446nm,晶胞中c原子、氧原子和碘原子分别处于顶点、面心和体心位置,如图所示。该晶体的化学式为,与c原子紧邻的氧原子有个。该晶体中c原子与氧原子间的最短距离为nm。
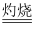 12KCN+Fe3C+2(CN)2↑+N2↑+C。下列说法错误的是( )
12KCN+Fe3C+2(CN)2↑+N2↑+C。下列说法错误的是( )
-
(1) 第四周期基态原子与基态Ni3+未成对电子数相同的元素有种。
-
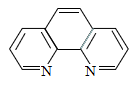
(2) 邻二氮菲(phen,结构如图)能通过N原子与Fe2+形成稳定的配合物[Fe(phen)3]2+ , 该配合物的特征颜色可用于测定Fe2+的浓度。[Fe(phen)3]2+中Fe2+的配位数为;实验表明,邻二氮菲检验Fe2+的适宜pH范围是2~9,其原因是。
-
(3) 草酸亚铁是生产磷酸铁锂动力电池的原料,可由草酸与硫酸亚铁铵反应制得。草酸与甲酸酸性相对强弱:草酸甲酸(填“>”“<”或“=”),其原因是。
-
(4) Fe3O4晶胞具有反尖晶石结构,氧离子和不同价态铁离子构成A、B两种结构,如图所示,其晶胞可以看作是由4个A型和4个B型小单元交替并置而成。
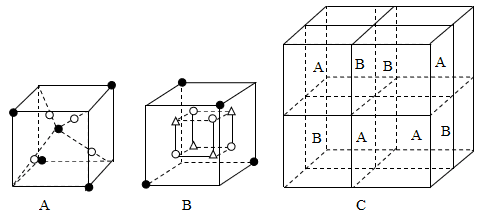
①Fe3+填充在O2-围成的空隙处(填“正四面体”或“正八面体”)。
②纳米材料的量子尺寸效应可以显著改变材料电磁性能,材料表面原子(或离子)占总原子(或离子)数的比例是重要的影响因素。假设某Fe3O4纳米颗粒恰好是一个Fe3O4晶胞,该颗粒表面离子与总离子数的最简整数比为。
- 下列物质中不能为人体生命活动提供能量的是
- 下列几种说法中正确的是:( )A.线圈中的磁通量变化越大,线圈中产生的感应电动势一定越大B.穿过线圈的磁通量越大,线
- 下列分子式只代表一种物质的是() A.C2H4Br2 B.C8
- 阅读《伤仲永》中文段,回答3—7题(26分)金溪平民方仲永,世隶耕。仲永生五年,未尝识书具,忽啼求之;父异焉,借旁近与之
- 国际上习惯用哪两条经线组成的经线圈作为东西半球的分界线:( ) A.0°经线和180°经线 B.20
- 下列关于生物工程的叙述中,不正确的是A.动物细胞培养可用于检测有毒物质 B.经诱导融合得到的杂种细胞,需经组织培养才能获
- 已知,求的值;
- 图中数码①②是两个城市的代码。读图完成下列小题。21.①②两城市都地处中纬度沿海地区,但气候类型不同,其主要原因是(
- 王安石变法中哪一措施与唐代的“庸”相似 A.青苗法 B.募役法 C.方田均税法
- 由Zn—Cu—H2SO4组成的原电池,工作一段时间后,锌片的质量减少了6.5g。求:(1)原电池的_______极生成氢
- 由于国内经济的回暖,2009年福建省城乡居民收入增长分别比上年同比提高10.9%和10.1%,消费预期明显增强。这说明
- 物理学家法拉第在研究电磁学时,亲手做过许多实验.如图6-1-19所示的实验就是著名的电磁旋转实验,这种现象是:如果载流导
- 中国奴隶社会的土地制度是A.井田制 B.礼乐制 C.分封制 D
- 下列句子中,没有语病的一项是 A.以“城市,让生活更美好”为主题的上海世博会,让肤色不同、语言不同的人们在这样一个巨大的
- 如图所示的几何体的正视图是( )
- 云南省原保山地委书记杨善洲,在位时,他始终廉洁奉公,公而忘私;退休后,他尽心竭力为老百姓办实事;辞世前,他把自己20多年
- 对H2O的电离平衡不产生影响的粒子是 A.HCl B.13X3+ C.CH3CO
- _____ about the economic crisis that he decided to look for
- “我们的制度之所以被称为民主政治,是因为政权在全体公民手中,而不是在少数人手中。在解决私人争执的时候,每个人在法律上都是
- 阅读下面短文,然后按照要求写一篇150词左右的英语短文: Irealize I am holding an ap
 I
I 平衡向右移动
平衡向右移动


