纯碱工业(侯氏制碱法) 知识点
纯碱工业(侯氏制碱法) 知识点题库
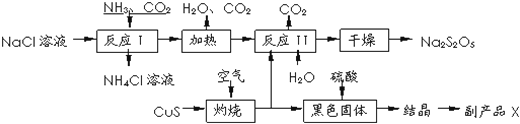
已知:反应Ⅱ包含2NaHSO3⇌Na2S2O5+H2O等多步反应.
(1)反应I的化学方程式为: .
(2)“灼烧”时发生反应的化学方程式: .
(3)已知Na2S2O5与稀硫酸反应放出SO2 , 其离子方程式为: .
(4)反应I时应先通的气体为 副产品X的化学式是 .生产中可循环利用的物质为 (填化学式)
(5)为了减少产品Na2S2O5中杂质含量,需控制反应Ⅱ中气体与固体的物质的量之比约为 .检验产品中含有碳酸钠杂质所需试剂是 (填编号)
①酸性高锰酸钾 ②品红溶液 ③澄清石灰水
④饱和碳酸氢钠溶液 ⑤NaOH ⑥稀硫酸.
2NaHCO3═Na2CO3+CO2↑+H2O↑ ②
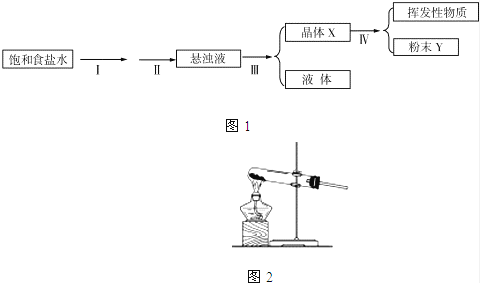
(1)操作Ⅰ、Ⅱ可否颠倒?答: (填“能”或“不能”);操作Ⅲ的名称是 .
(2)写出向晶体X的水溶液中滴加NaOH溶液时发生反应的离子方程式: .
(3)在实验室反应②可在如图2装置中进行,该装置可进行多个化学反应,如实验室制取少量氧气也可利用该装置,请再写出一种利用该装置制取的常见气体的名称.答: .
-
(1) (一)实验原理:向饱和食盐水中通入足量氨气和过量二氧化碳,析出溶解度较小的碳酸氢钠.写出相关离子方程式.
-
(2)
(二)实验装置:所需实验药品和装置如图所示:
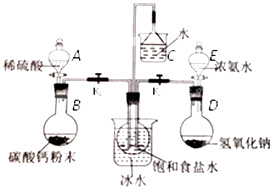
(三)实验步骤:
组装好装置,然后应该进行的操作是.
-
(3) 中间的烧瓶中加入20mL饱和食盐水,并将其浸入冰水中;D中加入足量氢氧化钠固体,E中加入足量浓氨水;B中加入足量碳酸钙粉末,A中加入足量稀硫酸于(可分多次加入).仪器A的名称是,选择用稀硫酸而不用稀盐酸的好处是.
-
(4) 先打开(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶.大约20分钟左右时,观察到饱和食盐水上方有现象时,再打开(填K1或K2),将装置A或E中的试剂慢慢加入圆底烧瓶,大约5分钟即有浑浊出现,约15分钟出现大量白色固体.
-
(5) (四)纯碱制备:
上述实验结束后,欲得到纯碱,将固体过滤、洗涤后,还需进行的操作是 (不加任何其它试剂,装置任选),反应的化学方程式为 ;若将上述操作产生的气体全部通过浓硫酸,再通过足量的过氧化钠,过氧化钠增重0.28g,则制得的纯碱质量为 g.
①Al2O3  NaAlO2(aq)
NaAlO2(aq)  Al(OH)3
Al(OH)3
②S  SO3
SO3  H2SO4
H2SO4
③饱和NaCl(aq) 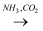 NaHCO3
NaHCO3  Na2CO3
Na2CO3
④Fe2O3 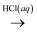 FeCl3(aq)
FeCl3(aq)  无水FeCl3
无水FeCl3
⑤MgCl2(aq) 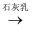 Mg(OH)2
Mg(OH)2  MgO
MgO
 通入氨的
通入氨的 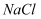 饱和溶液中,使溶解度较小的
饱和溶液中,使溶解度较小的 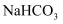 从溶液中析出
C . 可用
从溶液中析出
C . 可用  在加热条件下还原
在加热条件下还原 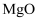 制备金属镁
D . 焦炭和石英砂制粗硅,说明单质C的氧化性比单质Si强
制备金属镁
D . 焦炭和石英砂制粗硅,说明单质C的氧化性比单质Si强
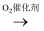 NO
NO 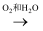 HNO3
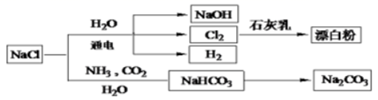
B . NaCl(aq)
HNO3
B . NaCl(aq)  Cl2
Cl2 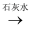 漂白粉
C . MgCl2(aq)
漂白粉
C . MgCl2(aq)  无水MgCl2
无水MgCl2  Mg
D . 饱和NaCl(aq)
Mg
D . 饱和NaCl(aq) 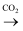 NaHCO3
NaHCO3  Na2CO3
Na2CO3
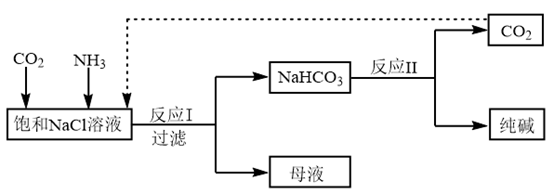
已知:常温常压下,1体积水能溶解1体积CO2;1体积水能溶解700体积NH3。下列有关说法错误的是( )

有关说法错误的是( )
[提出问题]能否在实验室模拟“侯氏制碱法”中制取NaHCO3的过程呢?
[实验验证]如图是该学习小组进行模拟实验时所用到的部分主要装置。已知浓氨水遇生石灰会产生大量的NH3。
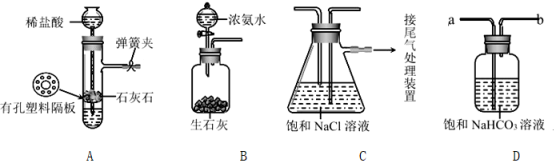
请回答下列问题:
-
(1) 检验装置A气密性的方法是:塞紧带长颈漏斗的橡胶塞,夹紧弹簧夹后,从漏斗注入一定量的水,使漏斗内的水面高于试管内的水面,停止加水后,若,说明装置不漏气。
-
(2) 实验室用石灰石(杂质既不溶于水也不与稀盐酸反应)和稀盐酸反应制取二氧化碳。反应的化学方程式为。
-
(3) 装置D是连接在装置A与装置C之间的气体净化装置,进气口是(填 “a”或“b”),装置D的作用是除去气体。
-
(4) 实验时先向饱和NaCl溶液中通入较多的NH3(溶液显碱性),再通入足量的CO2 , 其原因是(填标号)。
①使CO2更易被吸收②NH3比CO2更易制取③CO2的密度比NH3大
-
(5) 用的操作方法将生成的NaHCO3晶体从溶液中分离出来。[得出结论]利用“侯氏制碱法”在实验室可以制取NaHCO3。
-
(1) 一定温度下,往一定量饱和NaCl溶液中通入氨气达到饱和后,再不断通入CO2 , 一段时间后,出现沉淀,过滤得到NaHCO3晶体。该过程的化学方程式为:。
-
(2) 加热 NaHCO3的化学方程式为,实验室进行此操作的装置可以是图中的。
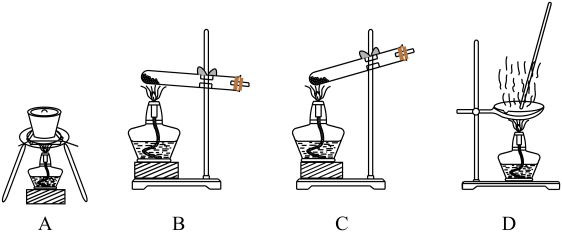
-
(3) 称取
 制得的碳酸钠样品,置于小烧杯中,加水溶解,向小烧杯中滴加足量氯化钙溶液充分反应(杂质不参加反应)。将反应混合物过滤、洗涤、干燥,得到质量为
制得的碳酸钠样品,置于小烧杯中,加水溶解,向小烧杯中滴加足量氯化钙溶液充分反应(杂质不参加反应)。将反应混合物过滤、洗涤、干燥,得到质量为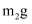 的沉淀。则该样品中碳酸钠的质量分数为(用
的沉淀。则该样品中碳酸钠的质量分数为(用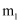 ,
, 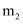 的计算式表示)。
的计算式表示)。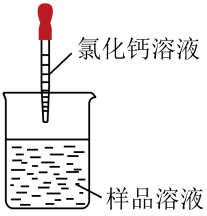
- 下列与免疫有关的叙述中,正确的是 A.效应B细胞能发生“染色质→染色体→染色质”的变化 B.利用效应细胞
- 函数的对称轴方程为x=______________.
- 下列过程没有体现生物膜信息传递功能的是 A.蔗糖溶液使洋葱表皮细胞发生质壁分离 B.抗原刺激引发记忆细胞增殖分化 C.胰
- 往纯水中加入下列物质,能使水的电离平衡发生移动的是( ) A.蔗糖 B.NaOH
- .既可以用来鉴别乙烯和甲烷,又可用来除去甲烷中混有的乙烯的方法是 A.通入足量的溴的四氯化碳溶液中 B.与足量的液溴反应
- 在下列文段的序号处填入恰当的标点符号。 在中国的文学作品中,常常可以看到这种“人生不再”的感觉。中国的诗人和学者,在欢娱
- 晚清时期,有人提议:“议院者,公议政事之院也。集全思,广众益,用人行政,一秉至公,法诚良,意诚美矣”“昏暴之君无所施其虐
- 读我国西北部分地区略图及材料,回答下列问题。(14分) 材料一 丁地区年日照时数为3 000~3 200小时,10℃以
- 常温下,下列各组离子在指定溶液中一定能大量共存的是( ) A.c(H+)/c(OH-)=1×1014的溶液:Na+、K+
- 要得到函数的导函数的图象,只需将的图象( ) A、向右平移个单位,再把各点的纵坐标伸长到原来的2倍(横坐标不
- 我国现阶段实行按劳分配为主体,多种分配方式并存的分配制度。实行这种分配制度的根本原因是 A.我国实行公有制为主体,多种所
- 王兵同学利用索尼HK1数码相机连拍功能(查阅资料得知此相机每秒连拍10张),记录下跳水比赛中小将陈若琳和王鑫在10 m跳
- 人体细胞有丝分裂时,形成的四分体个数是
- ( I )在一个容积固定不变的密闭容器中进行反应: 2X(g) + Y(g) 2Z(g),已知将2molX和1molY
- 1933年美国国会通过的《全国工业复兴法》规定:“工人有权组织起来,可选派代表与雇主进行谈判、签订集体合同。雇主不得以工
- —_______ John this week? —Yes. —Where _______ him? —In the l
- 10年来,我国铁路里程数突破10万公里,固定资产投资累计超过4.5万亿元。我国铁路技术达到世界先进水平,中国成为拥有世界
- 下列操作中,可以鉴别空气、氧气和二氧化碳三瓶气体的是 A. 观察气体颜色 B. 闻气体的气味 C. 插
- 在△ABC中,M是BC的中点,AM=1,点P在AM上且满足=2,则·(+)等于() A.-
- 下列各组中,没有“结构混乱”语病的一项是 A.适度的自我评价,实际上是把心理之船停泊在一个平静的“码头”;而超越个人实际



