蔗糖与淀粉的性质实验 知识点题库
-
(1) 各步加入的试剂的化学式:A ,B ,C
-
(2) 加入A溶液而不加入B溶液是否可以 ,其理由是
-
(3) 如何验证淀粉是否水解完全
-
(1) 属于烃类的是;
-
(2) 能与乙醇发生酯化反应的是;
-
(3) 植物通过光合作用直接生成的有机物是;
-
(4) 肉、蛋、奶等富含;
-
(5) 能作为制造肥皂的原料是;
-
(6) 棉花、甘蔗渣的主要成分是。
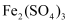 溶液
D . 稀硫酸
溶液
D . 稀硫酸
| 实验 | 结论 | |
| A | 甲烷与氯气在光照下反应后的混合气体能使湿润的蓝色石蕊试纸变红 | 生成的一氯甲烷具有酸性 |
| B | 向淀粉水解的产物中直接加入新制的氢氧化铜悬浊液,并加热煮沸,没有出现砖红色沉淀 | 水解的产物无还原性 |
| C | 室温下,向浓度为0.2 mol/L的BaCl2溶液中通入CO2气体,出现白色沉淀 | CO2与BaCl2反应生成BaCO3沉淀 |
| D | 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
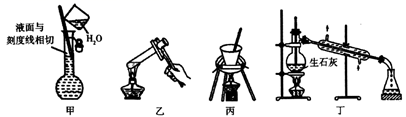
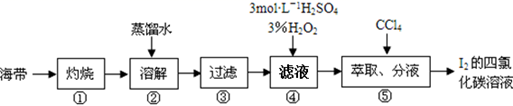
|
选项 |
实验操作 |
现象 |
结论 |
|
A |
向NaCl粉末中加入适量酒精,充分振荡形成无色透明液体,用激光笔照射 |
出现一条光亮通路 |
形成的分散系是胶体 |
|
B |
向2支分别盛有5mL0.1mo1∙L-1、1.0mo1.L-1NaHSO3溶液的试管中同时加入2mL5%H2O2溶液 |
均有气泡产生且1.0mo1∙L-1NaHSO3溶液产生气泡快 |
浓度大的NaHSO3溶液反应速率快 |
|
C |
取4mL淀粉溶液,加入5mL稀硫酸,加热5min后,再加入少量新制的Cu(OH)2 , 加热至沸腾 |
没有出现砖红色沉淀 |
淀粉未水解 |
|
D |
将Mg片和AL片用导线相连后,同时插入NaOH溶液中 |
Mg片上产生气泡 |
Al的金属性比Mg强 |
-
(1) 单质碘可与氢气反应生成碘化氢。将物质的量比为2:1的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g)⇌2HI(g),反应经过5分钟测得碘化氢的浓度为0.1mol•L-1 , 碘蒸气的浓度为0.05mol•L-1。
①前5分钟平均反应速率v(H2)=,H2的初始浓度是。
②下列能说明反应已达平衡状态的是(填序号)。
a.氢气的生成速率等于碘化氢的消耗速率
b.单位时间内断裂的H-H键数目与断裂的H–I键数目相等
c.c(H2):c(I2):c(HI)=1:1:2
d.2v(I2)正=v(HI)逆
e.反应混合体系的颜色不再发生变化
-
(2) 某小组同学在室温下进行“碘钟实验”:将浓度均为0.01mol•L-1的H2O2、H2SO4、KI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为:H2O2+2
 +2H+=
+2H+=  +2H2O,反应分两步进行:
+2H2O,反应分两步进行:反应A:…...
反应B:I2+2
 =2I-+
=2I-+ 
①反应A的离子方程式是。对于总反应,I-的作用是。
②为探究溶液变蓝快慢的影响因素,进行实验Ⅰ、Ⅱ。(溶液浓度均为0.01mol•L-1)
H2O2溶液
H2SO4溶液
Na2S2O3溶液
KI溶液(含淀粉)
H2O
实验Ⅰ
5
4
8
3
0
实验Ⅱ
5
2
x
Y
z
溶液从混合时的无色变为蓝色的时间:实验I是30min、实验II是40min。实验II中,x、y、z所对应的数值分别是;对比实验I、II、可得出的实验结论是。
|
实验操作 |
现象 |
结论 |
|
|
A |
溶液中加入适量盐酸,产生无色气体, 将气体通入澄清石灰水 |
澄清石灰水变浑浊 |
该溶液中一定含有CO32- |
|
B |
分别向鸡蛋清水溶液中加入饱和硫酸铵 溶液和硫酸铜溶液 |
均产生沉淀 |
蛋白质遇盐溶液发生 变性,失去生理活性 |
|
C |
溶液中加入 Ba(NO3)2 溶液,观察现象, 再加入足量稀硝酸酸化的 AgNO3 溶液 |
加入 Ba(NO3)2 溶液时无明 显现象,加入 AgNO3 溶液后,有白色沉淀产生 |
溶液中一定含有 Clˉ |
|
D |
淀粉溶液中加入稀硫酸,一段时间后加入 2mL10%CuSO4 溶液,再滴加 5 滴 5%NaOH 溶液,加热 |
未观察到砖红色沉淀出现 |
淀粉还没有水解 |
目的 | 方案设计 | 现象和结论 | |
A | 检验溶液中是否含有 | 取少量该溶液于试管中,先滴加 | 若沉淀不溶解,则说明溶液中含有 |
B | 探究淀粉水解程度 | 在试管中加入2mL淀粉溶液和适量稀硫酸,加热 | 若溶液中没有出现砖红色沉淀,则说明淀粉未水解 |
C | 验证乙醇脱水生成乙烯 | 向无水乙醇中加入浓硫酸,加热至170℃,将产生的气体通入溴水中 | 若溴水褪色,则有乙烯生成 |
D | 比较金属铝和氧化铝熔点的高低 | 用坩埚夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热 | 铝箔熔化但不滴落,说明金属铝的熔点比氧化铝低 |
-
(1) 检验葡萄汁含葡萄糖的方法是:向其中加碱调至碱性,再加入新制备的Cu(OH)2 , 加热,其现象是。
-
(2) 葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式。
C6H12O6(葡萄糖)
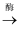 2+2C2H5OH
2+2C2H5OH -
(3) 葡萄酒密封储存过程中生成了有香味的酯,酯也可以通过化学实验来制备。实验室用右图所示装置制备乙酸乙酯:
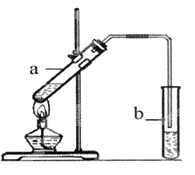
①试管a中生成乙酸乙酯的化学方程式是 。
②实验开始时,试管b中的导管不伸入液面下的原因是。
③若分离出试管b中生成的乙酸乙酯,需要用到的仪器是(填序号)。
a. 漏斗 b. 分液漏斗 c. 长颈漏斗
-
(4) 某有机物的结构简式为HOOC—CH=CHOH。验证该有机物中含有-COOH官能团常采用的方法是,产生的现象为。
 HNO3
B . CH3CH3
HNO3
B . CH3CH3 CH2BrCH2Br
C . Fe
CH2BrCH2Br
C . Fe Fe(NO3)3 (aq)
D . 淀粉(aq)
Fe(NO3)3 (aq)
D . 淀粉(aq)  C6H12O6(葡萄糖)
C6H12O6(葡萄糖)
- 18.对下面这段文字提供的信息进行筛选、整合,给“创造”下定义,不超过30字。 作为人的一种活动,创造包括思维活动和行为
- 某小组在实验室里制取CO2和O2时,用到了下列装置,请回答有关问题:(1)如图中仪器①、②的名称:①② (2)实验时能用
- 黑火药是我国历史上的四大发明之一,它的成分是硝酸钾、炭粉和硫粉的混合物,点火爆炸后的产物是二氧化碳、硫化钾和氮气。在该反
- 在一次数学活动中,黑板上画着如图所示的图形,活动前老师在准备的四张纸片上分别写有如下四个等式中的一个等式: ①
- 下列分子中的中心原子杂化轨道的类型相同的是A.CO2 SO2 B. C2H4 C2H2 C. B
- 如图是空气中氧气含量的测定装置。试回答: (1)盛在燃烧匙中的物质常用________ ,颜色为________,
- 2010年6月,《浙江省信息化促进条例(草案)》中有关立法禁止人肉搜索的规定引起了广泛争议,有专家指出:“总的说来,针对
- 如图,在空间四边形OABC中,OA=8,AB=6,AC=4,BC=5,∠OAC=45°,∠OAB=60°,求OA与BC的
- 与下图有关叙述中,不正确的是A.图一中abcde组成了一个完整的反射弧,a表示感受器 B.图一②的结构决定了神经元之间的
- 阅读下面的文字,完成16~21题(13分) 作为学者和诗人的闻一多先生,在30年代国立青岛大学的两年时间,我对他是有着深
- 减数第二次分裂的主要特征是() A.染色体自我复制 B.着丝点不分裂,同源染色体分开 C.着丝点分裂为两条染色单体分开
- 在“用电流表、电压表测电阻”的实验中,小李同学按图连接电路进行实验.所用电源为3节新干电池串联而成,且电压保持不变,滑动
- 人才是制约企业创新能力提高的重要因素。解决人才问题,“不拘一格是关键”这不仅仅指人才的不同类别、国家,还指使用人才的方法
- 读2012年1月29日我国华北地区气象干旱监测图(图10-12),判断旱情最严重的省级行政区包括( )A.鲁、苏、皖
- 综合性学习:2011年2月22日,利比亚安全形势发生了重大变化,如何让在利比亚的三万多中国滞留人员尽快撤离危险之地,他们
- 下列各组物质中,所含的分子数相同的是 ( ) A.10g H2和10g O2 B.5.6L N2和0.2
- 事物都有两面性,某气体在近地面空气中的浓度稍大时是一种污染物,而在高空中对人类有保护作用,该气体的同素异形体是(
- “夫天生一人,自有一人之用,不待取给于孔子而后足也,若必待取足于孔子,则千古以前无孔子,终不得为人乎?”明清之际最有可能
- (15分)某化学课外小组用下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
- 两极地区特殊的自然环境,为科学家进行科学研究提供了最为广阔的天然实验室。目前,我国在两极地区已经建成了四个科学考察站。分

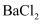 溶液,再加入稀盐酸
溶液,再加入稀盐酸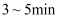 , 冷却后加入新制
, 冷却后加入新制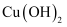 悬浊液加热煮沸
悬浊液加热煮沸


