乙醇的催化氧化实验 知识点题库
乙醇氧化制乙醛的实验装置如图所示(夹持仪器和加热仪器均未画出),下列叙述错误的是( )
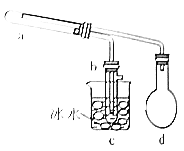
A . a中所盛的固体可以是CuO
B . d中乙醇可用沸水浴加热
C . c处具支试管b中有无色液体产生
D . c处具支试管b可换成带塞的普通试管
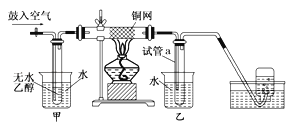
某实验小组用下列装置进行乙醇催化氧化的实验.
-
(1) 实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式 、 .在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该反应是 反应.
-
(2) 甲和乙两个水浴作用不相同.甲的作用是 ;乙的作用是
-
(3) 若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有
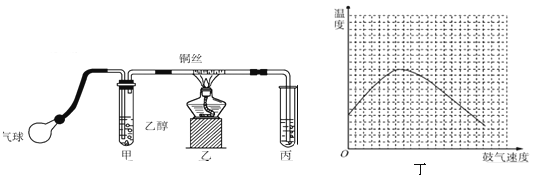
某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等固定装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.请填写下列空白:
-
(1) 检验乙醛的试剂是 (填字母).
A.银氨溶液 B.碳酸氢钠溶液 C.新制Cu(OH)2 D.氧化铜
-
(2) 乙醇发生催化氧化反应的化学方程式为:
-
(3) 实验时,常常将甲装置浸在70~80℃的水浴中,目的是 ,由于装置设计上的缺陷,实验进行时可能会
-
(4) 反应发生后,移去酒精灯,利用反应自身放出的热量可维持反 应继续进行.进一步研究表明,鼓气速度与反应体系的温度关系曲线如图丁所示.试解释鼓气速度过快,反应体系温度反而下降的原因 ,该实验中“鼓气速度”这一变量你认为可用 来估量.
-
(5) 该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确?
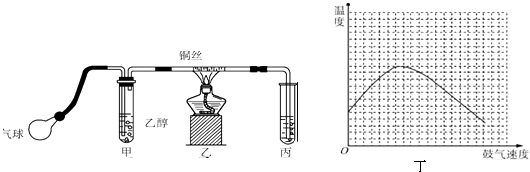
某课外活动小组利用如图所示的装置进行乙醇的催化氧化实验并制取乙醛(试管丙中用水吸收产物),图中铁架台等固定装置已略去.实验时,先加热玻璃管中的铜丝,约1min后鼓入空气.请填写下列空白:
-
(1) 检验乙醛的试剂是 (填字母).A . 银氨溶液 B . 碳酸氢钠溶液 C . 新制Cu(OH)2 D . 氧化铜
-
(2) 乙醇发生催化氧化反应的化学方程式为:.
-
(3) 实验时,常常将甲装置浸在70~80℃的水浴中,目的是,由于装置设计上的缺陷,实验进行时可能会.
-
(4) 反应发生后,移去酒精灯,利用反应自身放出的热量可维持反 应继续进行.进一步研究表明,鼓气速度与反应体系的温度关系曲线如图丁所示.试解释鼓气速度过快,反应体系温度反而下降的原因,该实验中“鼓气速度”这一变量你认为可用来估量.
-
(5) 该课外活动小组偶然发现向溴水中加入乙醛溶液,溴水褪色.该同学为解释上述现象,提出两种猜想:①溴水将乙醛氧化为乙酸;②溴水与乙醛发生加成反应.请你设计一个简单的实验,探究哪一种猜想正确?.
按下图装置,持续通入气体X,可看到a处有红色物质生成,b处变蓝,c处得到液体,则气体X可能是( )
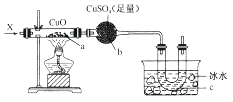
A . H2
B . CO和H2
C . NH3
D . CH3CH2OH(蒸气)
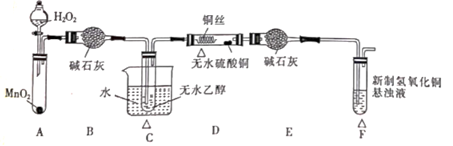
某化学课外活动小组设计了如图所示的装置(图中夹持装置未画出,“△”表示酒精灯热源)来研究乙醇催化氧化的实验。已知:无水乙醇的沸点为78℃,新制氢氧化铜悬浊液可用于验证乙醇催化氧化反应的氧化产物。
-
(1) 发生反应时,装置A中反应的还原剂是(填化学式,下同),D中反应的氧化剂是
-
(2) 装置B的作用是;装置C中热水的作用是
-
(3) 装置D中发生的氧化反应的化学方程式为
-
(4) 实验一段时间后,若撤掉装置D中的酒精灯,则反应(填“能”或“不能”)继续进行,原因是
分子中含有4个碳原子的饱和一元醇,发生氧化反应后能生成醛的种数与发生消去反应后能生成烯烃(要考虑顺反异构)的种数分别为( )
A . 2、3
B . 2、4
C . 3、3
D . 3、4
下列方程式不正确的是( )
A . 镁在二氧化碳中燃烧的化学方程式:2Mg+CO2  2MgO+C
B . 一水合氨在水中的电离方程式:NH3·H2O=NH
2MgO+C
B . 一水合氨在水中的电离方程式:NH3·H2O=NH  +OH-
C . 氯化铁水解的离子方程式:Fe3++3H2O
+OH-
C . 氯化铁水解的离子方程式:Fe3++3H2O  Fe(OH)3+3H+
D . 乙醇在铜催化下被氧化的化学方程式:2CH3CH2OH+O2
Fe(OH)3+3H+
D . 乙醇在铜催化下被氧化的化学方程式:2CH3CH2OH+O2  2CH3CHO+2H2O
2CH3CHO+2H2O
 2MgO+C
B . 一水合氨在水中的电离方程式:NH3·H2O=NH
2MgO+C
B . 一水合氨在水中的电离方程式:NH3·H2O=NH  +OH-
C . 氯化铁水解的离子方程式:Fe3++3H2O
+OH-
C . 氯化铁水解的离子方程式:Fe3++3H2O  Fe(OH)3+3H+
D . 乙醇在铜催化下被氧化的化学方程式:2CH3CH2OH+O2
Fe(OH)3+3H+
D . 乙醇在铜催化下被氧化的化学方程式:2CH3CH2OH+O2  2CH3CHO+2H2O
2CH3CHO+2H2O
把一端弯成螺旋状的铜丝放在酒精灯火焰上加热,看到铜丝表面生成黑色的(填化学式),再迅速把铜丝插入盛有乙醇的试管里,看到铜丝表面,反复多次,试管内有气味的生成,其反应的化学方程式为,反应中乙醇被。
下面四个反应中,反应类型与其它三个不同的是( )
A . CH3CH2OH+CH3COOH 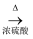 CH3COOCH2CH3+H2O
B . CH3CH2Br+NaOH
CH3COOCH2CH3+H2O
B . CH3CH2Br+NaOH  CH3CH2OH+NaBr
C . C6H5OH+3Br2 ⟶
CH3CH2OH+NaBr
C . C6H5OH+3Br2 ⟶ 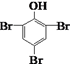 +3HBr
D . 2CH3CH2OH+O2
+3HBr
D . 2CH3CH2OH+O2  2CH3CHO+2H2O
2CH3CHO+2H2O
 CH3COOCH2CH3+H2O
B . CH3CH2Br+NaOH
CH3COOCH2CH3+H2O
B . CH3CH2Br+NaOH  CH3CH2OH+NaBr
C . C6H5OH+3Br2 ⟶
CH3CH2OH+NaBr
C . C6H5OH+3Br2 ⟶ 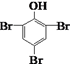 +3HBr
D . 2CH3CH2OH+O2
+3HBr
D . 2CH3CH2OH+O2  2CH3CHO+2H2O
2CH3CHO+2H2O
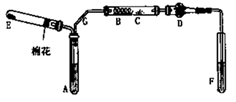
如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出)。图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液。
-
(1) 为使A中乙醇平稳地汽化成乙醇蒸气,常采用的方法是。
-
(2) 若E中的固体为纯净物,则E的化学式是。
-
(3) 写出B处发生反应的化学方程式
-
(4) 加热F处的混合液的实验现象是。
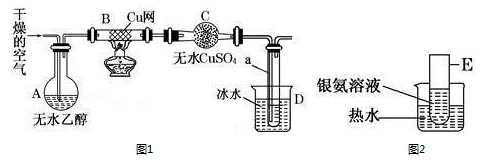
某化学兴趣小组,设计了如图1所示的实验装置(部分夹持装置未画出),来做乙醇催化氧化的实验,并验证其产物。请填写下列空白:

-
(1) 在A处不断鼓入空气的情况下,熄灭B处的酒精灯,反应仍能继续进行,说明乙醇的催化氧化反应是反应;(填“放热”或“吸热”)
-
(2) 装置D使用冰水进行冷却的目的是;
-
(3) 反应开始一段时间,C中观察到的现象是;
-
(4) 为检测产物,取出试管a中部分液体,加入银氨溶液,水浴加热,可观察到E试管有银镜产生,说明乙醇的催化氧化产物中存在;(填官能团名称)
-
(5) 写出E处反应的化学方程式:。
-
(6) 若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有。要除去该物质,可先在混合液中加入碳酸氢钠溶液,再通过(填实验操作名称)即可分离主要产物。
下图所示为某化学兴趣小组设计的乙醇催化氧化及其产物检验的实验装置(图中加热仪器、铁架台、铁夹等均未画出)。
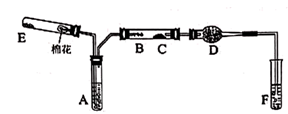
图中:A为无水乙醇(沸点为78℃),B为绕成螺旋状的细铜丝或银丝,C为无水 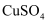 粉末,D为碱石灰,F为新制的碱性
粉末,D为碱石灰,F为新制的碱性 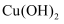 悬浊液。
悬浊液。
-
(1) 在上述装置中,实验时需要加热的仪器从左到右依次为(填仪器或某部位的代号)、、、(可以填满,也可以不填满);
-
(2) 为使A中乙醇平稳气化成乙醇蒸气,常采用的方法是;
-
(3) 检验乙醇氧化产物时F中的实验现象是;
-
(4) E处是一种纯净物,其反应方程式为;
-
(5) 写出乙醇发生催化氧化成乙醛的化学方程式。
请按要求填空:
-
(1) 苯酚与溴水生成白色沉淀的反应类型是。
-
(2) 填写有机物的结构简式:1-氯丁烷
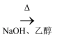
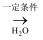 2-丁醇。
2-丁醇。
-
(3) 写出乙醇催化氧化生成乙醛的反应方程式。
-
(4) 涤纶的结构简式为
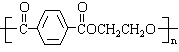 ,写出其单体的结构简式。
,写出其单体的结构简式。
-
(5) 某链烃C6H12的所有碳原子共平面,则其结构简式为。
乙醇是醇类物质的代表,下列乙醇的性质也是所有醇都具有的是( )
A . 能与羧酸发生酯化反应
B . 能与水互溶
C . 和浓硫酸在加热作用下发生消去反应
D . 在 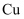 或
或 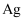 作催化剂及加热条件下发生氧化反应
作催化剂及加热条件下发生氧化反应
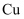 或
或 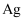 作催化剂及加热条件下发生氧化反应
作催化剂及加热条件下发生氧化反应
下列反应能使有机物官能团数目增加的是( )
A . 乙烯与HBr发生加成反应
B . 苯发生硝化反应
C . 乙烯合成聚乙烯
D . 乙醇催化氧化生成乙醛
在探究乙醇的有关实验中,得出的结论正确的是( )
选项 | 实验步骤及现象 | 实验结论 |
A | 在酒精试样中加入少量CuSO4·5H2O,搅拌,试管底部有蓝色晶体 | 酒精试样中一定含有水 |
B | 在乙醇燃烧火焰上方罩一冷的干燥烧杯,内壁有水珠出现,另罩一内壁涂有澄清石灰水的烧杯,内壁出现白色沉淀 | 乙醇由C、H、O三种元素组成 |
C | 将灼热后表面变黑的螺旋状铜丝伸入约50℃的乙醇中,铜丝能保持红热一段时间 | 乙醇催化氧化反应是放热反应 |
D | 在0.01mol金属钠中加入过量的乙醇充分反应,收集到标准状况下气体112mL | 乙醇分子中有1个氢原子与氧原子相连,其余与碳原子相连 |
A . A
B . B
C . C
D . D
下列设计的实验装置或方案不能达到相应实验目的的是( )
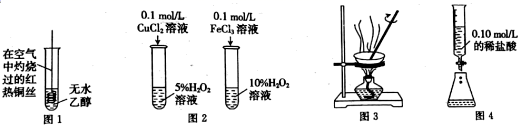
A . 利用图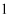 装置探究乙醇的还原性
B . 利用图
装置探究乙醇的还原性
B . 利用图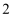 装置比较
装置比较 的催化效果好于
的催化效果好于 C . 利用图
C . 利用图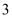 装置从
装置从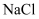 溶液中提取
溶液中提取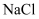 晶体
D . 利用图
晶体
D . 利用图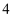 装置量取
装置量取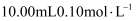 的稀盐酸
的稀盐酸
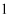 装置探究乙醇的还原性
B . 利用图
装置探究乙醇的还原性
B . 利用图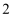 装置比较
装置比较 的催化效果好于
的催化效果好于 C . 利用图
C . 利用图 装置从
装置从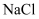 溶液中提取
溶液中提取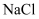 晶体
D . 利用图
晶体
D . 利用图 装置量取
装置量取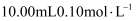 的稀盐酸
的稀盐酸
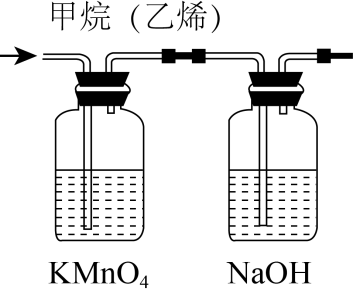
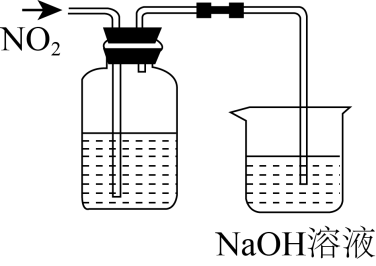
用下列实验装置不能达到相关实验目的的是( )
A | B | C | D | |
实验装置 |
|
|
|
|
实验目的 | 探究 | 除去甲烷中的乙烯 | 收集 | 将乙醇氧化为乙醛 |
A . A
B . B
C . C
D . D
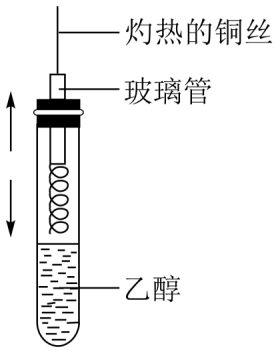
已知乙醛的沸点为20.8℃。实验室可用如图所示装置完成乙醇到乙醛的转化,下列叙述正确的是( )
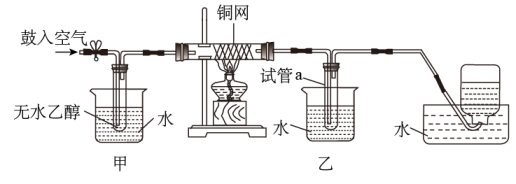
A . 集气瓶中收集到气体的主要成分是O2
B . 甲烧杯中盛装热水,乙烧杯中盛装冷水
C . 试管a中收集到的液体仅为乙醛
D . 反应结束后铜网变黑
最近更新
- 分解因式: .
- A geography teacher hung amap of the world’s river distribut
- (二)小石潭记(12分)柳宗元从小丘西行百二十步,隔篁竹,闻水声,如鸣珮环,心乐之。伐竹取道,下见小潭,水尤清冽。全石以
- 如图6所示是凝固图像,其中表示非晶体凝固的图像是 ;表示晶体凝固过程的是 段,物质处于
- 已知函数=当2<a<3<b<4时,函数的零点 .
- 噬菌体侵染细菌的实验可以证明 A.DNA是主要的遗传物质 B.噬菌体的遗传物质是DNA而不是蛋白质 C.所有生物的遗传物
- 大型音乐舞蹈史诗《复兴之路》2010年3月28日晚在国家大剧院举行闭幕演出。中共中央政治局常委李长春发贺信表示祝贺。回答
- — $1,500, but that’s my last offer. — OK. It’s a ____. A.
- As a poet, Hai Zi usedto write many romantic poems ______ pe
- 某强酸性溶液中可能存在NO3-、I-、Cl-、Fe3+中的一种或几种。向该溶液中加入溴水后,溴被还原,由此可推断该溶液中
- 据《左传》鲁宣公十五年记载“民不肯尽力于公田”。下列对引文中所说“公田”特点的叙述不正确是 A.土地归国家所有
- 为预防金属制品锈蚀,下列措施或做法不当的是 A.将使用后的菜刀洗净擦干 B.在铁制门窗表面喷涂油漆
- Most students make a study plan________ the beginning of the
- 依次填入下列各句横线处的词语,最恰当的一组是 ①剑南风景区的万竿碧竹,郁郁葱葱,生机勃勃。那壮观的景色令他久久不能
- The garbage _______ (短信) on cell phones are pollutingthe te
- 孔孟学说主要讨论的是( ) A.人与人的关系 B.人与自然的关系 C.国与国的关系 D.夷夏关系
- (1)上述实验结果的归纳,正确的有 (填实验序号)。 (2)实验①在染色之后,用吸水纸吸去染液,
- 关于催化剂的说法正确的是() A.催化剂只能加快反应速率 B.催化剂在反应前后质量和性质不变 C.不使用催化剂,反应就不
- 某同学的午餐是米饭、牛排、煎蛋、鱼汤,他需要补充的营养成分是( ) A.维生素 B.糖类 C.脂肪 D.蛋白
- 近代人诗言:“轮船电报开平矿,创自商人尽商股……总办商董举自官,不依商律自商 举,……不闻岁举查账员,股息多少任所予。…

 与
与 的反应
的反应 气体
气体


