常见化学电源的种类及其工作原理 知识点题库
高功率Ni/MH(M表示储氢合金)电池已经用于混合动力汽车。总反应方程式如下:
下列叙述不正确的是( )
A . 该电池放电时的正极和充电时的阴极均发生还原反应
B . 放电时负极反应为:MH+OH--e- = M+H2O
C . 充电时阳极反应为:NiOOH+H2O+e- = Ni(OH)2+OH-
D . 放电时每转移1mol电子,正极有1molNiOOH被还原
氢氧燃料电池用于航天飞船,电极反应产生的水,经冷凝后可作为航天员的饮用水,其电极反应如下:①2H2+4OH﹣-4e﹣=4H2O,②O2+2H2O+4e﹣=4OH﹣ 当得到1.8L饮用水时,电池内转移的电子数约为( )
A . 1.8mol
B . 3.6mol
C . 100mol
D . 200mol
如图为铅蓄电池的示意图.下列说法正确的是( )
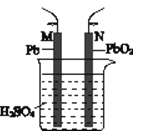
A . 放电时,N为负极,其电极反应式为:PbO2+SO42﹣+4H++2e﹣=PbSO4+2H2O
B . 放电时,c(H2SO4)不变,两极的质量增加
C . 充电时,阳极反应式为:PbSO4+2e﹣=Pb+SO42﹣
D . 充电时,若N连电源正极,则该极生成PbO2
下列叙述中正确的是( )
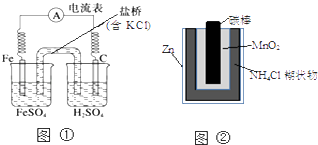
A . 图①中正极附近溶液pH降低
B . 图②正极反应是2MnO2(s)+H2O(l)+2e﹣=Mn2O3(s)+2OH﹣(aq)
C . 图①中电子由Fe流向石墨,盐桥中的Cl﹣移向FeSO4溶液
D . Zn﹣MnO2干电池自放电腐蚀主要是由MnO2的氧化作用引起的
氢氧燃料电池是一种新能源.如图为氢氧燃料电池示意图.下列说法不正确的是( )
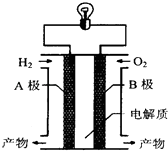
A . 该装置能将化学能转化为电能
B . A极是正极,B极是负极
C . 电子由A极通过导线流向B极
D . 产物为无污染的水,属于环境友好电池
碱性电池具有容量大、放电电流大的特点,因而得到广泛使用,锌﹣锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s)下列说法错误的是( )
A . 电池工作时,锌失去电子
B . 电池正极的电极反应式为:2MnO2(s)+H2O(l)+2e﹣═Mn2O3(s)+2OH﹣(aq)
C . 电池工作时,电子由正极通过外电路流向负极
D . 外电路中每通过0.1mol电子,锌的质量理论上减小6.5g
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为:3Zn+2K2FeO4+8H2O  3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A . 放电时负极反应为:Zn﹣2e+2OH=Zn(OH)2
B . 充电时阳极反应为:Fe(OH)3﹣3e+5OH﹣=FeO42﹣+4H2O
C . 放电时每转移3mol电子,正极有1molK2FeO4被氧化
D . 放电时正极附近溶液的碱性增强
Li﹣CuO二次电池的比能量高、工作温度宽,性能优异,广泛应用于军事和空间领域.
-
(1) Li﹣CuO电池中,金属锂做极.
-
(2) 比能量是指消耗单位质量的电极所释放的电量,用来衡量电池的优劣.比较Li、Na、Al分别作为电极时比能量的大小:.
-
(3) 通过如下过程制备CuO
Cu
 CuSO4溶液
CuSO4溶液  Cu2(OH)2CO3沉淀
Cu2(OH)2CO3沉淀  CuO
CuO①过程Ⅰ,H2O2的作用是.
②过程Ⅱ产生Cu2(OH)2CO3的离子方程式是.
③过程Ⅱ,将CuSO4溶液加到Na2CO3溶液中,研究二者不同物质的量之比与产品纯度的关系(用测定铜元素的百分含量来表征产品的纯度),结果如下:
已知:Cu2(OH)2CO3中铜元素的百分含量为57.7%.
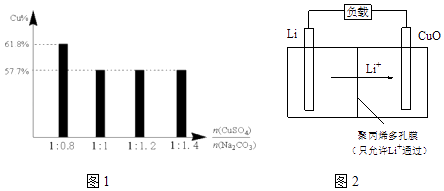
二者比值为1:0.8时,产品中可能含有的杂质是,产生该杂质的原因是.
④过程Ⅲ反应的化学方程式是.
-
(4) Li﹣CuO二次电池以含Li+的有机溶液为电解质溶液,其工作原理示意如图2.放电时,正极的电极反应式是.
水钴矿中除SiO2外,还有9.24% CoO、2.78% Fe2O3、0.96% MgO、0.084%CaO。 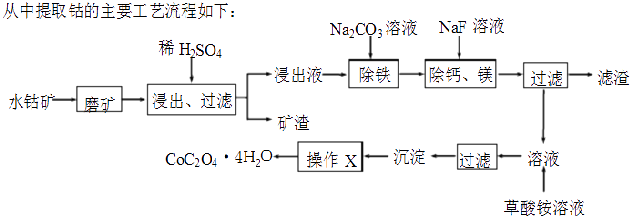



-
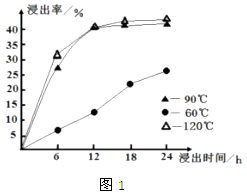
(1) 在一定浓度的
 溶液中,钴的浸出率随时间、温度的变化如图1所示
溶液中,钴的浸出率随时间、温度的变化如图1所示  考虑生产成本和效率,最佳的浸出时间为小时,最佳的浸出温度为
考虑生产成本和效率,最佳的浸出时间为小时,最佳的浸出温度为 
-
(2) 请配平下列除铁的化学方程式:
_ _Fe2(SO4)3+H2O +Na2CO3 =Na2Fe6(SO4)4(OH)12↓+Na2SO4 +CO2↑
-
(3) “除钙、镁”的原理反应为:
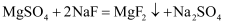 ;
; 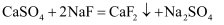 已知
已知  ,加入过量NaF溶液反应完全后过滤,则滤液中
,加入过量NaF溶液反应完全后过滤,则滤液中  .
.
-
(4) “沉淀”中含杂质离子主要有
 、
、 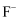 、和;“操作X”包括和。
、和;“操作X”包括和。
-
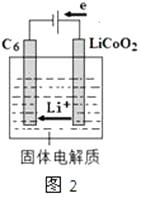
(5) 某锂离子电池正极是
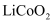 ,含
,含 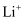 导电固体为电解质
导电固体为电解质  充电时,
充电时, 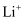 还原为Li,并以原子形式嵌入电池负极材料碳
还原为Li,并以原子形式嵌入电池负极材料碳  中
中  如图2所示
如图2所示 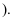 电池反应为
电池反应为 
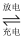
 ,写出该电池放电时的正极反应式 .
,写出该电池放电时的正极反应式 .
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O=Fe(OH)2+2Ni(OH)2 , 下列有关该电池的说法正确的是( )
A . 电池的电解液为碱性溶液,正极发生氧化反应
B . 电池放电时,负极反应为Fe+2OH--2e-= Fe(OH)2
C . 电池充电过程中,阴极附近溶液的pH降低
D . 电池充电时,阳极反应为2Ni(OH)2+2OH-- 2e-= Ni2O3+3H2O
某太阳能电池的工作原理如图所示。下列说法正确的是( )
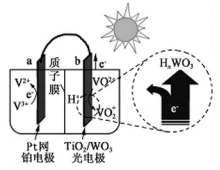
A . 硅太阳能电池供电原理与该电池相同
B . 光照时, H+由a极区经质子交换膜向b极区迁移
C . 光照时,b极的电极反应式为 VO2+-e-+H2O=VO2++2H+
D . 夜间无光照时,a极的电极反应式为V3++e-=V2+
硼氢化物NaBH4(B元素的化合价为+3价)燃料电池(DBFC), 由于具有效率高、产物清洁无污染和燃料易于储存和运输等优点,被认为是一种很有发展潜力的燃料电池。其工作原理如下图所示,下列说法正确的是( )
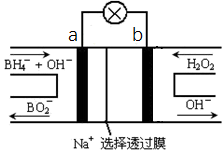
A . 电池的负极反应为BH4-+2H2O-8e-=BO2-+8H+
B . 放电时,每转移2mol电子,理论上需要消耗9.5gNaBH4
C . 电池放电时Na+从b极区移向a极区
D . 电极a采用MnO2 , MnO2既作电极材料又有催化作用
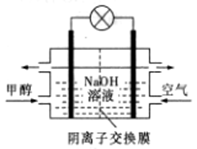
煤的液化可以合成甲醇。下列有关说法正确的是( )
①“气化”:C(s)+2H2O(g)=CO2(g)+2H2(g)ΔH1=+90.1kJ·mol-1
②催化液化I:CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H2=-49.0kJ·mol-1
③催化液化Ⅱ:CO2(g)+2H2(g)=CH3OH(g)+  O2(g)△H3=akJ·mol
O2(g)△H3=akJ·mol
A . 催化液化I的反应在高温下更容易自发进行
B . C(s)+H2O(g)+H2(g)=CH3OH(g)△H=+41.1kJ·mol-1
C . △H2>△H3
D . 如图所示为甲醇燃料电池的工作原理示意图,负极的电极反应为CH3OH-6e-+6OH-=CO2↑+5H2O
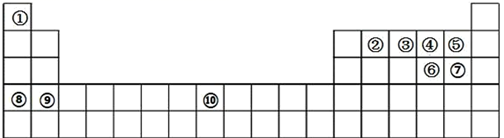
下图所示是元素周期表的轮廓图,根据元素①~⑩在周期表中的位置,按题目要求回答问题:
-
(1) 元素①、②能形成 16 电子的分子,该分子的电子式为, 元素①、③能形成 10 电子的分子,请用电子式表示该物质的形成过程;
-
(2) 元素④、⑤、⑥形成的简单氢化物的热稳定性从小到大顺序为(用化学式表示);
-
(3) 将过量的元素⑩单质加入到元素③最高价氧化物水化物的稀溶液中,发生反应的离子反应方程式为;
-
(4) 铅元素在元素周期表中的位置为,铅酸蓄电池是典型的二次电池,在生活中有广泛的应用,其放电时正极的电极反应式为,放电一段时间后,正极质量增加 6.4g,则这段时间,转移电子物质的量为mol。
下列有关电池的说法错误的是( )
A . 手机用的锂离子电池属于二次电池
B . 锌锰干电池中锌电极是负极
C . 甲醇燃料电池可把化学能转化为电能
D . 汽车所用的铅蓄电池可以无限次的反复放电、充电
人造地球卫星上使用的一种高能电池(银锌蓄电池),其电池的电极反应式为:Zn+2OH--2e- =ZnO+H2O,Ag2O+H2O+2e- =2Ag+2OH-。据此判断氧化银是( )
A . 正极,被还原
B . 负极,被氧化
C . 正极,被氧化
D . 负极,被还原
自古以来,化学与人类生产、生活密切相关,下列有关说法错误的是( )
A . 杜康用高粱酿酒的原理,是通过蒸馏法将高粱中的乙醇分离出来
B . 制造新版人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质
C . “深海勇士”号潜水艇使用的锂离子电池是一种二次电池
D . 唐代诗人刘禹锡的《浪淘沙》中“美人首饰侯王印,尽是沙中浪底来”不涉及氧化还原反应
化学电源在日常生活和高科技领域中都有广泛应用。下列说法错误的是( )
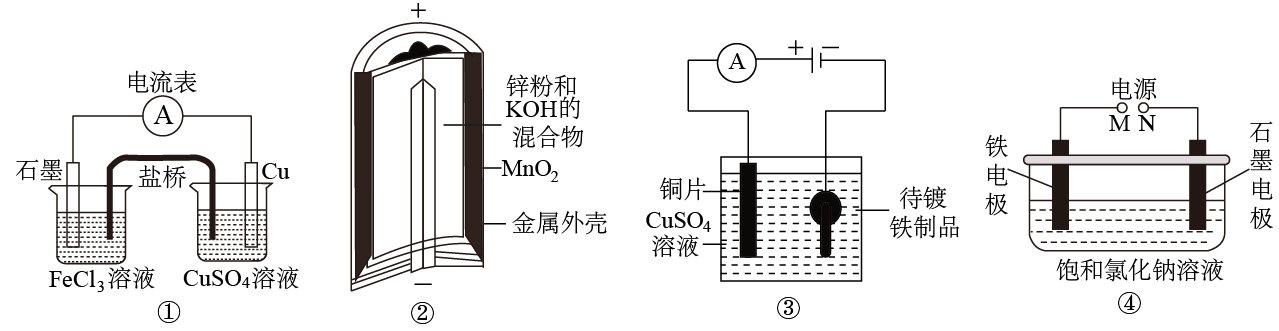
A . ①中,电子由Cu电极通过电流表流向石墨电极
B . ②中,干电池正极电极反应式为: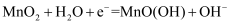 C . ③中,Cu2+移向待镀铁制品且溶液中Cu2+的浓度降低
D . ④中,为了保护铁电极不受腐蚀,M应接电源的负极
C . ③中,Cu2+移向待镀铁制品且溶液中Cu2+的浓度降低
D . ④中,为了保护铁电极不受腐蚀,M应接电源的负极
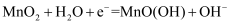 C . ③中,Cu2+移向待镀铁制品且溶液中Cu2+的浓度降低
D . ④中,为了保护铁电极不受腐蚀,M应接电源的负极
C . ③中,Cu2+移向待镀铁制品且溶液中Cu2+的浓度降低
D . ④中,为了保护铁电极不受腐蚀,M应接电源的负极
氮元素的单质及其化合物是化学研究的热点。回答下列问题:
-
(1) 肼(N2H4 , 常温下为液态)是火箭的传统燃料之一,某N2H4-O2原电池的工作原理如图甲。
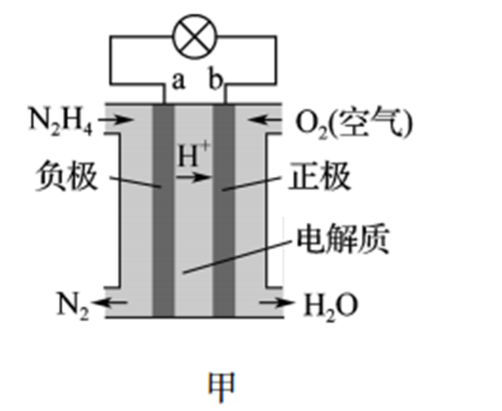
①a极的电极反应式为。
②该电池工作时,若有2 mol电子流经外电路,则被还原的O2体积为L(标准状况下)。
-
(2) 一定温度时,在体积为2 L的恒容反应器中发生反应:
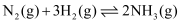 , A、B物质的量随时间的变化曲线如图乙所示。
, A、B物质的量随时间的变化曲线如图乙所示。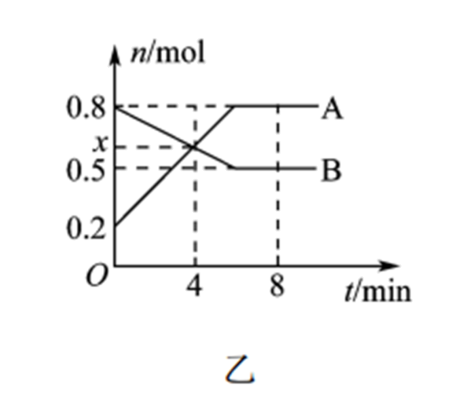
①A为(填化学式)。
②4 min时,v正(填“>”“<”或“=”) v逆。
③
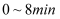 内该反应的平均反应速率v(H2)=(保留两位有效数字)
内该反应的平均反应速率v(H2)=(保留两位有效数字) 。
。④
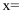 ,反应进行4 min时,N2的转化率为
,反应进行4 min时,N2的转化率为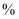 。
。
根据氧化还原反应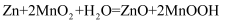 , 设计原电池,下列有关说法中正确的是( )
, 设计原电池,下列有关说法中正确的是( )
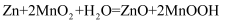 , 设计原电池,下列有关说法中正确的是( )
, 设计原电池,下列有关说法中正确的是( )
A . 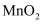 在电池的正极发生氧化反应
B . 电流方向是从锌极流出并经过用电器流向二氧化锰电极
C . Zn极上发生的电极反应为
在电池的正极发生氧化反应
B . 电流方向是从锌极流出并经过用电器流向二氧化锰电极
C . Zn极上发生的电极反应为 D . 电解质溶液可能是稀硫酸
D . 电解质溶液可能是稀硫酸
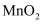 在电池的正极发生氧化反应
B . 电流方向是从锌极流出并经过用电器流向二氧化锰电极
C . Zn极上发生的电极反应为
在电池的正极发生氧化反应
B . 电流方向是从锌极流出并经过用电器流向二氧化锰电极
C . Zn极上发生的电极反应为 D . 电解质溶液可能是稀硫酸
D . 电解质溶液可能是稀硫酸
最近更新
- 一台电动机的输出功率是10KW,这表明电动机工作时A.每秒钟能消耗10KW的电能B.每秒钟对外做10KW的功C.每秒钟对
- 托盘天平是物理实验中常用的实验测量仪器。在使用前调节天平时,要将游码移动到 (1) ,若此时观察到如图所示的现象,这
- 下面这些对北京人一天生活的描述,正确的是( ) A.一个北京人在原始森林中用弓箭射死了一头野兽 B.大家很高兴,马上
- 图1-29中为一“滤速器”装置示意图。a、b为水平放置的平行金属板,一束具有各种不同速率的电子沿水平方向经小孔O进入a、
- 如图,⊙O是外接圆,,BD为⊙的直径,BD=2,连结CD,求BC的长
- 根据下列反应判断有关物质还原性由强到弱的顺序是① H2SO3+I2+H2O=2HI+H2SO4 ② 2
- 某一密闭绝热容器中盛有饱和Ca(OH)2溶液,当加入少量CaO粉末,下列说法正确的是( )①有晶体析出 ②c[C
- 据统计,截止到5月31日上海世博会累计入园人数803.27万人.803.27万这个数字(保留两位有效数字)用科学记数法表
- 如图,闭合线圈上方有一竖直放置的条形磁铁,磁铁的N 极朝下。当磁铁向下运动时(但未插入线圈内部)( )A.线圈
- . The door is not ______ for theelephant to pass. A. w
- 某市政府规定,“凡是市政府发布或经市政府同意以部门名义印发的涉及经济社会发展和人民群众切身利益的重要文件,均需进行解读”
- 用红果番茄(RR)作父本,黄果番茄(rr)作母本进行杂交,正确的是 ①所结番茄全为黄果,遗传方式为细胞质遗传 ②杂交种子
- 1960年,法国总统戴高乐听到法国首先成功试验原子弹的消息后高呼:“法国万岁!从今天早上起,她更加强大了,更加骄傲了……
- 如图所示,A、B两物体的质量分别为mA、mB,用劲度系数为k的轻弹簧相连。开始时,A、B都处于静止状态。现对A施加一个竖
- 人生的舞台 孙道荣 ①头发理好了。镜子里的我,显得精神多了。我满意地朝理发师点点头。 ②我准备站起来,理发师却示意我再等
- 反应mA(固)+nB(气) eC(气)+fD(气),反应过程中,当 其它条件不变时,C的百分含量(C%)与温
- 反应C(s)+H2O(g)CO(g)+H2(g)在一体积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是_
- 图为光合作用暗反应阶段的示意图.RuBP羧化酶能催化CO2+C5(即RuBP)→2C3.为测定RuBP羧化酶的活性,某学
- .已知等腰三角形的一条边等于4,另一条边等于9,那么这个三角形的第三边是_______
- (06年浙江卷文)抛物线的准线方程是( ) (A) (B) (C)



