常见能量的转化及运用 知识点题库
下列有关能量转换的说法错误的是( )
A . 煤燃烧是化学能转化为热能的过程
B . 化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C . 动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D . 植物通过光合作用将CO2转化为葡萄糖是太阳能转变成化学能的过程
下列设备工作时,将化学能转化为热能的是( )
A | B | C | D |
|
|
|
|
硅太阳能电池 | 锂离子电池 | 太阳能集热器 | 燃气灶 |
A . A
B . B
C . C
D . D
化学家认为石油、煤作为能源使用时,燃烧了“未来的原始材料”.下列观点正确的是( )
A . 大力提倡开发化石燃料作为能源
B . 研发新型催化剂,提高石油和煤中各组分的燃烧热
C . 化石燃料属于可再生能源,不影响可持续发展
D . 人类应尽可能开发新能源,取代化石能源
下列电池工作时能量转化形式与其它三个不同的是( )
|
|
|
|
A.锌锰碱性电池 | B.硅太阳能电池 | C.氢燃料电池 | D.银锌纽扣电池 |
A . A
B . B
C . C
D . D
H2在O2中燃烧生成气态H2O的反应是一个放热反应,在反应过程中( )
A . 核能转化成热能
B . 化学能转化成热能
C . 生成物的总能量等于反应物的总能量
D . 生成物的总能量大于反应物的总能量
分析下图,不能得出的结论是( )
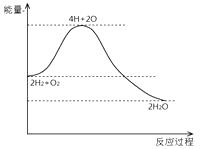

A . H2与O2反应是放热反应
B . 断开化学键要放出能量
C . 化学反应伴随着物质变化和能量变化
D . 2mol H2和1mol O2具有的总能量高于2mol H2O 的总能量
下列说法错误的是( )
A . 化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能
B . 光—热转化是目前技术最成熟、成本最低廉、应用最广泛的利用太阳能形式
C . 氢气之所以被称为“绿色能源”是因为它燃烧的产物不会污染环境
D . 人类利用的能源都是通过化学反应获得的
2SO2(g)+O2(g)  2SO3(g) △H =-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO3+SO3(快);4VO2+O2→2V2O5(慢)( )
2SO3(g) △H =-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO3+SO3(快);4VO2+O2→2V2O5(慢)( )
 2SO3(g) △H =-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO3+SO3(快);4VO2+O2→2V2O5(慢)( )
2SO3(g) △H =-198kJ/mol,在V2O5存在时,该反应机理为:V2O5+SO2→2VO3+SO3(快);4VO2+O2→2V2O5(慢)( )
A . 反应速率主要取决于V2O5的质量
B . VO2是该反应的催化剂
C . 该反应逆反应的活化能大于198kJ/mol
D . 升高温度,该反应的△H增大
下列说法正确的是( )
A . 需要加热的反应一定是吸热反应
B . 放热反应X(s)=Y(s),则X比Y稳定
C . 硫蒸气和硫固体分别完全燃烧,后者放出的热量更多
D . 在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定不同
下列说法错误的是( )
A . 化学能可以转变成为热能、电能等
B . 化学反应必然伴随发生能量变化
C . 化学反应中的能量变化主要是由化学键的变化引起的
D . 化学反应中能量变化的多少与反应物的质量无关
一种钌(Ru)基配合物光敏染料敏化太阳能电池的原理及电池中发生的主要反应如图所示。下列说法正确的是( )
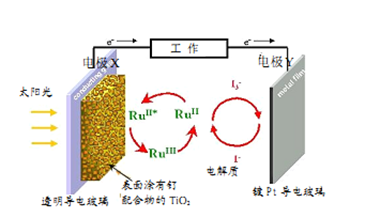
A . 镀铂导电玻璃的作用是传递I-
B . 电池工作时,光能转变为电能,X为电池的正极
C . 电池的电解质溶液中I-和I3-的浓度均不断减小
D . 电解质溶液中发生反应2Ru3++3I-═2Ru2++I3-
下列依据热化学方程式得出的结论正确的是( )
A . 已知2SO2(g)+O2(g)  2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 若C(石墨,s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C . 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 , 则20.0 g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量
D . 已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2 , 则ΔH1>ΔH2
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 若C(石墨,s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C . 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 , 则20.0 g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量
D . 已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2 , 则ΔH1>ΔH2
 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 若C(石墨,s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C . 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 , 则20.0 g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量
D . 已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2 , 则ΔH1>ΔH2
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B . 若C(石墨,s)=C(金刚石,s) ΔH>0,则石墨比金刚石稳定
C . 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1 , 则20.0 g NaOH固体与稀盐酸完全中和,放出28.7 kJ的热量
D . 已知2C(s)+2O2(g)=2CO2(g) ΔH1;2C(s)+O2(g)=2CO(g) ΔH2 , 则ΔH1>ΔH2
有关电解原理的说法正确的是( )
①电解是把电能转变成化学能 ②电解是把化学能转变成电能 ③电解质溶液导电是化学变化,金属导电是物理变化④不能自发进行的氧化还原反应,通过电解的原理可以实现⑤任何溶液被电解时,必然导致氧化还原反应的发生
A . ①②③④
B . ②③⑤
C . ③④
D . ①③④⑤
已知某反应A(g)+B(g)=C(g)+D(g),过程中的能量变化如图所示,下列说法中正确是( )
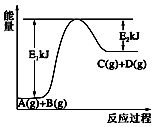
A . A的能量一定低于C
B . 反应物断键吸收的总能量大于产物新键形成放出的总能量
C . 化学反应中的能量变化都表现为热量的变化
D . 1mol气体A和1mol气体B反应生成1mol气体C和1molD
与如图图像有关的叙述,正确的是( )
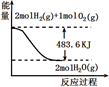
A . H2O(g)的能量低于H2(g)和O2(g)的能量之和
B . 表示的热化学方程式为:H2(g)+  O2(g)=H2O(g)+241.8kJ
C . 表示1molH2(g)完全燃烧生成水蒸气吸收241.8kJ热量
D . 表示2molH2(g)所具有的能量一定比2mol气态水所具有的能量多483.6kJ
O2(g)=H2O(g)+241.8kJ
C . 表示1molH2(g)完全燃烧生成水蒸气吸收241.8kJ热量
D . 表示2molH2(g)所具有的能量一定比2mol气态水所具有的能量多483.6kJ
 O2(g)=H2O(g)+241.8kJ
C . 表示1molH2(g)完全燃烧生成水蒸气吸收241.8kJ热量
D . 表示2molH2(g)所具有的能量一定比2mol气态水所具有的能量多483.6kJ
O2(g)=H2O(g)+241.8kJ
C . 表示1molH2(g)完全燃烧生成水蒸气吸收241.8kJ热量
D . 表示2molH2(g)所具有的能量一定比2mol气态水所具有的能量多483.6kJ
能源是现代社会发展的主要支柱,下列属于二次能源的是( )
A . 太阳能
B . 水力
C . 潮汐能
D . 电力
电能是一种清洁能源,下列发电厂在生产过程中,将化学能转化为电能的是( )

A . 水力发电厂
B . 火力发电厂
C . 潮汐发电厂
D . 风力发电厂
我国中科院天津工业生物所利用光伏发电,将电解水获得的H2与CO2反应合成甲醇,再由甲醇经若干醇促反应合成淀粉,首次在实验室实现二氧化碳到淀粉的从头合成,相关论文在国际学术期刊《自然》上发表。回答下列问题:
-
(1) 该研究成果中涉及的能量转换形式为
-
(2) 已知:在一定温度和压强下,由最稳定单质生成1mol化合物的焓变称为该物质的摩尔生成焓。某些化合物的摩尔生成焓如表所示。
化合物
CO2(g)
CH3OH(g)
H2O(g)
摩尔生成焓/(kJ·mol-1)
-395
-200
-242
反应Ⅰ:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)△H1
CH3OH(g)+H2O(g)△H1反应Ⅱ:CO2(g)+H2(g)
 CO(g)+H2O(g)△H2
CO(g)+H2O(g)△H2①反应Ⅰ的焓变△H1=kJ·mol-1。
②保持温度T不变,在一刚性密闭容器中,充入一定量的CO2及H2 , 起始及达平衡时,容器内各气体物质的量如表所示。
CO2
H2
CH3OH
CO
H2O
起始量/mol
4.0
8.0
0
0
0
平衡量/mol
n1
3.0
已知起始时总压强为1.5pkPa,平衡时体系总压强为pkPa,则表中n1=,反应I的平衡常数Kp=。(无需带单位,用含p的式子表示)。
-
(3) 取物质的量浓度为amol·L-1的甲醇,选择不同的工程酶组块作为催化剂反应10h,测得实验数据如表所示。
实验序号
温度(K)
不同工程酶的组块
淀粉(g/L)
1
T1
无
0.21
2
T1
agp-M1
0.38
3
T2
agp-M2
1.82
4
T2
agp-M3
1.24
①最佳的反应条件为
②已知温度升高,反应生成的淀粉量先增加后急剧减少,其可能的原因是。
③实验4可用淀粉的质量浓度表示反应速率为g·L-1·h-1 , 淀粉的产率为(用含a的代数式表示)。
为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。回答下列问题:
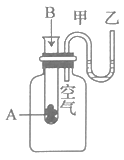
-
(1) 该反应为(填“放热”或“吸热”)反应。
-
(2) 反应物A和B的总能量比生成物C和D的总能量(填“高”或低”)。
-
(3) 该反应过程中,物质中的能通过化学反应转化成能释放出来。
-
(4) 该反应过程中,反应物化学键断裂吸收的能量(填“高”或“低”)于生成物化学键形成放出的能量。
-
(5) 下列反应符合题中实验现象的是____(填标号)。A . 2Al+6HCl=2AlCl3+3H2↑ B . 2Na+2H2O=2NaOH+H2↑ C . NaOH+HCl=NaCl+H2O D . Na2O2+2CO2=2Na2CO3+O2
北京冬奥会彰显了我国的科技实力。下列有关说法错误的是( )
A . 开幕式“演出服”用到的新型材料石墨烯,既能导热又能导电
B . 吉祥物“冰墩墩”的毛绒材质主要是聚酯纤维,其属于合成纤维
C . 速滑馆“冰丝带”采取CO2跨临界直冷制冰,利用了CO2的化学性质
D . 场馆大面积使用的“碲化镉”发电玻璃,可将光能高效转化为电能
最近更新
- 如图,足球图片正中的黑色正五边形的内角和是()A.180° B.360° C.
- 中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末同时生成氯化钠。该成果发表在世
- 交通是否更顺畅,环境是否更美好……日前,作出“十大突出问题”整改承诺的武汉市政府14个部门的“一把手”,接受了市民代表团
- 读图某区域等压线形势图,完成问题。 在
- 甲溶液PH是1,乙溶液PH是2,甲溶液与乙溶液的氢离子浓度之比为 A.10﹕1 B.1﹕10 C.2﹕1
- 下列国家中地跨亚欧两洲的是 A.① B.② C.③ D.④
- 将下列各组物质分别置于烧杯中,加适量水,振荡,可得无色透明溶液的一组是() A.AgNO3、BaCl2、HCl(过量)
- a、b两球位于同一竖直线上的不同位置,a比b高h,如图所示,将a、b 两球分别以v1、v2的速度沿同一水平方向抛出,不计
- 下列应用与中和反应原理无关的是( ) A.用浓硫酸干燥湿润的氧气 B.用熟石灰改良酸性土壤 C.服用含氢氧化铝的药物
- 渔夫的妻子桑娜毫不犹豫地收养了邻居西蒙的孩子。(缩句) _______________________________
- 下列关于我国封建专制主义中央集权制度的认识正确的是( ) ①它的产生是中国封建自然经济发展的必然结果 ②封建专制主义的
- The cold and icy land that isthe Eskimo's home is a danger
- 下列对“联合国的成立是人类历史上一件具有划时代意义的大事”理解正确的是 ①联合国是世界上第一个宣布以维护世界和平为宗旨的
- 读漫画《艰难的出路》,艰难的出路解决伊拉克问题的出路似乎并不难找,关键在于高傲的山姆大叔肯不肯低下“高贵的头”。(图中英
- 马克思主义诞生的标志是 A.宪章运动的出现 B.《宣言》
- 我国女药学家、诺贝尔奖获得者屠呦呦发现的青蒿素(化学式为C15H22O5)是一种用于治疗疟疾的药物.下列有关青蒿素的说法
- 改革开放30年我国保险业保持30%以上的年平均增长速度,是国民经济中发展最快也是最具活力的朝阳行业之一。以下对保险认识正
- 随着“绿色青奥会”的理念逐渐深入人心,空气质量日益受到人们的关注。下列物质中,未计入监测空气污染指数项目的是(
- (08年北师大附中月考)函数y = x3 + ax + b在区间(-1,1)上为减函数,在(1,+∞)上为增函数,则(
- We call Sam Smith . A. Mr. Sam B. Mr. Smith C











