元素周期律和元素周期表的综合应用 知识点题库
短周期元素R、T、Q、W在元素周期表中的相对位置如右下图所示,其中T所处的周期序数与族序数相等。下列推断不正确的是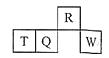
A . 最简单气态氢化物的热稳定性:R>Q
B . 最高价氧化物对应水化物的酸性:Q<W
C . 原子半径:T>Q>R
D . 含T的盐溶液一定显示酸性
短周期元素X、Y、Z在元素周期表中的位置如图所示,其中Y元素原子的最外层电子数是电子层数的两倍.回答下列问题:
X | ||
Y | Z |
-
(1) Z元素在元素周期表中的位置是.
-
(2) 下列能证明Y元素与Z元素的得电子能力强弱的是 . (填序号)A . 氢化物水溶液的酸性 B . 最高价氧化物对应的水化物的酸性 C . 气态氢化物的稳定性 D . 与金属化合时每个原子得电子的多少
-
(3) 比较Y和Z简单离子半径大小(用离子符号表示)
-
(4) X元素的某种气态氢化物分子中含有10个电子.该物质在加热条件下能够将CuO还原为Cu,同时生成一种气体,该气体是空气中的成分之一.则反应的化学方程式为.若反应中有6.02×1022个电子发生转移,则有 g的CuO参加反应.
表为周期表的一部分,其中的字母代表对应的元素,请针对这些元素回答下列问题.

请回答下列问题:
-
(1) 元素I的元素符号;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的周期族.
-
(2) 表中元素第一电离能最小的是(填元素符号,下同),电负性最大的是,化学性质最稳定的是.
-
(3) 表中元素处于d区的是(填元素符号).
-
(4) 请举出F的金属性比C强的实验事实:,并用原子结构理论解释其原因:
短周期元素W、X、Y、Z在元素周期表中的位置如图所示.下列说法中,正确的是( )
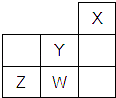
A . Y的原子半径在同周期主族元素中最大
B . W的非金属性比Z的弱
C . Z的气态氢化物的稳定性在同主族元素中最强
D . W的最高价氧化物对应的水化物是强酸
短周期元素W、X、Y、Z的原子序数依次增大,W的一种核素在考古时常用来鉴定一些文物的年代,X2-和Y3+具有相同的电子层结构,Z原子的最外层电子数是其电子层数的2倍。下列相关说法错误的是( )
A . 简单氢化物的稳定性:W<X
B . 单核阴离子还原性:Z>X
C . 电解Y的熔融氧化物可制备Y单质
D . WZ2分子中只存在共价键
原子序数依次增大的短周期元素a、b、c、d,它们的最外层电子数分别依次为6、7、1、3。a、b、c、d形成的简单离子与氖原子电子层结构相同。下列叙述错误的是( )
A . d的最高价氧化物对应水化物可溶于c的最高价氧化物对应的水化物的溶液
B . a和c形成的离子化合物中可能含有共价键
C . 四种元素离子半径:c>d>a>b
D . c是短周期元素中金属性最强的元素,b是短周期元素中非金属性最强的元素
下列是元素周期表的一部分,A、B、C、D、E、F、G、X分别代表一种元素,其中X在周期表中的位置没有标出,请回答下列有关问题。
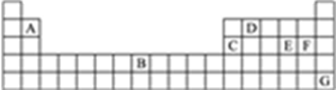
-
(1) X在A元素附近,与F能形成化学式为XF的离子化合物,X单质的密度小于水,有两种重要的氧化物。X在周期表中的位置是第周期第族;X单质与其相邻元素的单质形成的合金主要用途是。
-
(2) A、C具有相似的化学性质,请写出A和X的最高价氧化物对应的水化物之间反应的离子方程式。
-
(3) B与水蒸气在高温下反应的化学方程式是。
-
(4) E的一种氧化物通入F的水溶液中可以得到两种物质,写出反应的离子方程式:。
-
(5) 有同学判断G是一种稀有气体,由此判断不存在G的化合物。该说法是否正确:。
W、X、Y、Z为短周期元素,W的原子中只1个电子,X2-和Y-的电子层结构相同,Z与X同族。下列叙述错误的是( )
A . Y的原子半径是这些元素中最大的
B . Z与W形成的化合物的溶液呈弱酸性
C . W与其他三种元素形成的二元化合物中其化合价均为+1
D . X与其他三种元素均可形成至少两种二元化合物
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
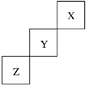
A . X、Y、Z三种元素中,X的非金属性最强
B . X单质的熔点比Z的低
C . Y的最高正化合价为+7价
D . Y的氢化物的稳定性比Z的氢化物弱
寻找室温超导材料一直是科学家们竞相追求的目标,
CaFeAsF 、LaH10、H2S等均是近年来的研究热点。回答下列问题:
-
(1) 基态As原子价层电子的电子排布图(轨道表达式)为,基态La原子价电子排布为5d16s2 , 成为阳离子时首先失去轨道电子。
-
(2) CaFeAsF中,电负性最高的元素是。
-
(3) Ca与Fe位于同周期且最外层电子构型相同,Ca的熔点和沸点均比Fe的低,这是因为。
-
(4) H2S的的空间构型为,写出一种与H2S互为等电子体的分子的化学式。
-
(5) 含砷化合物(以
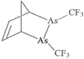 )中碳原子杂化方式是, 每个分子中含σ键和π键个数比为。
)中碳原子杂化方式是, 每个分子中含σ键和π键个数比为。
-
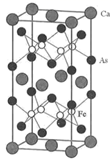
(6) Ca、Fe、As构成的超导材料的晶胞结构如图所示,边长为apm,高为cpm,则紧邻的Ca原子之间的距离为 pm,该晶体的密度为 g•cm-3。
下列叙述正确的是( )
A . 第二周期主族元素原子半径从左到右依次减小
B . 第三周期元素的氯化物所属晶体类型相同
C . 短周期第IA族与VIIA族元素构成的物质均含离子键
D . 元素周期表中位于金属与非金属分界线附近的元素属于过渡元素
化合物 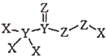 是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力,可用于目前新冠病毒疫情下的生活消毒。其中X、Y、Z为原子序数依次增大的短周期元素。下列叙述正确的是( )
是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力,可用于目前新冠病毒疫情下的生活消毒。其中X、Y、Z为原子序数依次增大的短周期元素。下列叙述正确的是( )
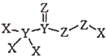 是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力,可用于目前新冠病毒疫情下的生活消毒。其中X、Y、Z为原子序数依次增大的短周期元素。下列叙述正确的是( )
是一种高效消毒剂,其蒸汽和溶液都具有很强的杀菌能力,可用于目前新冠病毒疫情下的生活消毒。其中X、Y、Z为原子序数依次增大的短周期元素。下列叙述正确的是( )
A . 原子半径:Z>Y>X
B . Z的第一电离能比同周期相邻元素都大
C . 1mol该化合物分子中含有的非极性键数目为2NA
D . 该化合物中X、Y、Z都满足8电子稳定结构
如图所示是一种麻醉剂的分子结构式。其中,X的原子核内只有1个质子;元素Y、Z、W原子序数依次增大,且均位于X的下一周期;元素E的原子比W原子多8个电子。下列说法错误的是( )
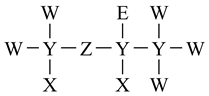
A .  是一种强酸
B .
是一种强酸
B .  中,Z的化合价为
中,Z的化合价为 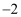 价
C . 原子半径:
价
C . 原子半径: 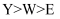 D . 非金属性:
D . 非金属性: 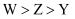
 是一种强酸
B .
是一种强酸
B .  中,Z的化合价为
中,Z的化合价为  价
C . 原子半径:
价
C . 原子半径:  D . 非金属性:
D . 非金属性: 
下列有关碱金属元素的性质判断正确的是( )
A . Li与 反应最剧烈
B . 从Li到Cs,其单质熔沸点逐渐升高
C . 钾与氧气反应可生成多种氧化物
D . 从Li到Cs最高价氧化物对应的水化物的碱性逐渐减弱
反应最剧烈
B . 从Li到Cs,其单质熔沸点逐渐升高
C . 钾与氧气反应可生成多种氧化物
D . 从Li到Cs最高价氧化物对应的水化物的碱性逐渐减弱
 反应最剧烈
B . 从Li到Cs,其单质熔沸点逐渐升高
C . 钾与氧气反应可生成多种氧化物
D . 从Li到Cs最高价氧化物对应的水化物的碱性逐渐减弱
反应最剧烈
B . 从Li到Cs,其单质熔沸点逐渐升高
C . 钾与氧气反应可生成多种氧化物
D . 从Li到Cs最高价氧化物对应的水化物的碱性逐渐减弱
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X同主族,Y原子的最外层电子数等于X原子的电子总数。Z原子的电子总数等于W、X、Y原子的电子数之和,Z的最高价氧化物对应水化物的化学式为HnZO2n+2。W、X、Y三种元素组成的一种化合物的结构如图所示。下列说法正确的是( )
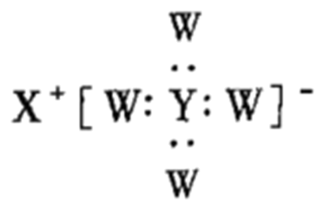
A . W没有负化合价
B . Z的单质通入SO2的水溶液中,漂白效果更好
C . X在短周期元素中金属性最强
D . Y的最高价氧化物对应的水化物属于两性化合物
A、B、C、D、E、F、G是短周期中原子序数依次增大的主族元素,A、B元素最高正价与最低负价之和均为0,D、F是同主族元素且F元素原子序数是D元素原子序数的2倍,E元素原子半径是短周期中最大的。下列说法正确的是( )
A . B,C,D三者的简单气态氢化物的热稳定性:B>C>D
B . 简单离子的半径:E>D>C
C . 简单气态氢化物的还原性:G>F
D . B,D与A均可形成含非极性键的二元化合物
短周期主族元素W、X、Y、Z的原子序数依次增大,且原子序数成等差数列,Z原子的最外层电子数等于其电子层数。短周期中,Y的最高价氧化物对应的水化物的碱性最强。下列说法错误的是( )
A . 原子半径:Y>Z>W>X
B . X的简单氢化物对应的酸属于强酸
C . 简单氢化物的稳定性:X>W
D . 工业上通常采用电解法制备Y、Z的单质
短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者Y原子最外层电子数的3倍。下列说法正确的是( )
A . X的氢化物溶于水显酸性
B . Y的氧化物是共价化合物
C . 其离子半径大小:Z>Y>X
D . X和Z的最高价氧化物对应的水化物都是强酸
X、Y、Z、W为原子序数依次增大的短周期主族元素,Y、W同族,常温下Z的单质遇Y的最高价氧化物对应水化物的浓溶液会发生钝化反应,由X、Y、Z三种原子构成的一种特殊离子化合物如图所示,下列说法正确的是( )
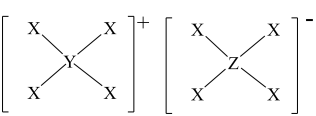
A . 在元素周期表中,111号元素与Z元素同族
B . Y的非金属性比W的强,所以单质的还原性:Y>W
C . X、Y形成的二元化合物只含有极性共价键
D . X、Z、Y、W四种元素的简单离子半径依次增大
W、X、Y均为短周期元素,它们可以形成离子化合物 、W和Y两种元素的单质可以生成
、W和Y两种元素的单质可以生成 和
和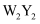 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水,下列说法正确的是( )
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水,下列说法正确的是( )
 、W和Y两种元素的单质可以生成
、W和Y两种元素的单质可以生成 和
和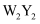 两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水,下列说法正确的是( )
两种化合物,X元素的氢化物和它的某种氧化物反应,可以生成固态单质和水,下列说法正确的是( )
A . 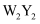 与水反应,生成的化合物中存在极性键和非极性键
B . 同周期元素中,X的最高价氧化物的水化物酸性最强
C . 同主族元素中,Y的简单氢化物沸点最低
D . W、X、Y的简单离子半径由大到小顺序是
与水反应,生成的化合物中存在极性键和非极性键
B . 同周期元素中,X的最高价氧化物的水化物酸性最强
C . 同主族元素中,Y的简单氢化物沸点最低
D . W、X、Y的简单离子半径由大到小顺序是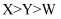
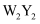 与水反应,生成的化合物中存在极性键和非极性键
B . 同周期元素中,X的最高价氧化物的水化物酸性最强
C . 同主族元素中,Y的简单氢化物沸点最低
D . W、X、Y的简单离子半径由大到小顺序是
与水反应,生成的化合物中存在极性键和非极性键
B . 同周期元素中,X的最高价氧化物的水化物酸性最强
C . 同主族元素中,Y的简单氢化物沸点最低
D . W、X、Y的简单离子半径由大到小顺序是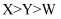
最近更新
- 季风水田区的水稻种植业的特点有() A.单位面积产量高而且商品率高 B.主要以大农场为单位生产 C.机械化水平低 D.科
- .现代化是人类孜孜以求的目标。历史学家认为,欧洲近代早期的文艺复兴、宗教改革、科技革命与启蒙运动极大地促进了现代化进程。
- 函数y=中自变量x的取值范围是( ) A.x>1 B. x≥1
- 印度最容易发生的自然灾害是 A.火山 B.地震
- 14.—You forgot your purse when you went out. —Good heavens,
- NA表示阿伏加德罗常数的值,下列说法不正确的是 ( ) A.标准状况下,22
- 小红按某种规律写出4个方程:①;②;③;④.按此规律,第五个方程的两个根为( ) A.-2、3 B.2、-3
- 建筑、装饰、装修等材料会散发甲醒、苯等有害气体而导致室内空气污染.成为头号“健康杀手”。此现象表明分子在承不停息地做无规
- 根据要求默写。(8分)(1)气蒸云梦泽, 。(2) ?烟波江上使人愁。(
- Sometimes the _______ between the reality and the dream is s
- 某溶液中,只可能含有下列离子中的几种:阳离子 K+、Mg2、Fe3+、Al3+ 阴离子 、、现每次取100.00mL溶液
- 关于内环境与稳态的叙述,正确的是( ) A、内环境主要由血液、组织液和淋巴组成 B、内环境中多余的H+
- 下列关于交叉互换与染色体易位的区别的叙述中不正确的是A.图甲是交叉互换,图乙是染色体易位 B.交叉互换发生于同源染色体之
- 太阳能丰富,有“日光城”之称的城市是( ) A.漠河 B.海口
- 若用 NA表示阿伏加德罗常数的值,下列叙述不正确的是( ) A.在0.1 mol NaHSO4晶体中阳离子与阴
- The wild flowers looked like a soft orange blanket__________
- If you don’t work hard for most of the year and then work ha
- 2009年7月16日,教育部、国家民委印发的《全国中小学民族团结教育工作部署视频会议纪要》指出,我国将把民族团结教育纳入
- 下图中四位同学正在讨论某一化学方程式表示的意义,他们描述的化学方程式是()。A.C+O2CO2 B.2CO+O22CO2
- I used tobelieve courtesy was a thing of the past. Very seld



