铵盐 知识点题库
-
(1) NH4Al(SO4)2可作净水剂,其理由是 (用必要的化学用语和相关文字说明).
-
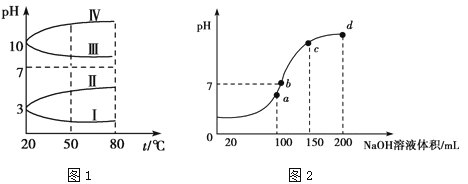
(2) 如图1是0.1mol•L﹣1的几种电解质溶液的pH随温度变化的曲线.
①其中符合NH4Al(SO4)2的曲线是 (填写序号),导致pH随温度变化的原因是
②25℃时,0.1mol•L﹣1 NH4Al(SO4)2中2c(SO42﹣)﹣c(NH4+)﹣3c(Al3+)= (近似值).
-
(3)
室温时,向100mL0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图2所示:
试分析图中a、b、c、d四个点,水的电离程度最大的是 点;在b点,溶液中各离子浓度由大到小的排列顺序是
 NH3↑+H2O
D . 除去NaCl固体中混有的NH4HCO3固体可以采用加热的方法
NH3↑+H2O
D . 除去NaCl固体中混有的NH4HCO3固体可以采用加热的方法
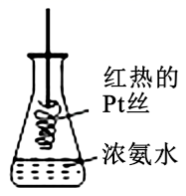
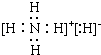 B . NH4H固体投入少量水中,有两种气体产生
C . NH4H中的H﹣离子半径比锂离子半径大
D . NH4H溶于水后,形成的溶液呈酸性
B . NH4H固体投入少量水中,有两种气体产生
C . NH4H中的H﹣离子半径比锂离子半径大
D . NH4H溶于水后,形成的溶液呈酸性
①Na2SiO3 ②Al(OH)3 ③NH4HCO3 ④Al2O3 ⑤NaHSO4
| 选项 | 实验操作和现象 | 结论 |
| A | 强酸性溶液X中加入Ba(NO3)2溶液,静置后再加入KSCN溶液,先生成白色沉淀,后溶液变红 | 溶液X中一定含有 |
| B | 检验HCl气体中是否含有Cl2 , 将气体通入品红溶液中,品红溶液褪色,加热后溶液不恢复成红色 | HCl气体中含有Cl2 |
| C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色 | Fe3+的还原性比I2强 |
| D | 加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结 | NH4Cl固体易升华 |
| 实验 | 现象 | 结论 | |
| A. | 向2mL0.1mol/LFeCl3的溶液中加足量铁粉,振荡,加1滴KSCN溶液 | 黄色逐渐消失,加KSCN溶液颜色不变 | 还原性:Fe>Fe2+ |
| B. | 将金属钠在燃烧匙中点燃,迅速伸入集满CO2的集气瓶 | 集气瓶中产生大量白烟,瓶内有黑色颗粒产生 | CO2具有氧化性 |
| C. | 加热盛有少量NH4HCO3固体的试管,并在试管口放置湿润的红色石蕊试纸 | 石蕊试纸变蓝 | NH4HCO3显碱性 |
| D. | 将SO2通入酸性KMnO4溶液 | 紫色溶液褪色 | SO2具有还原性 |
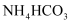 固体,观察到固体逐渐减少,试管口有液滴产生,说明
固体,观察到固体逐渐减少,试管口有液滴产生,说明 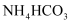 受热不稳定
C . 将红热的铂丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气红热体,说明氨气的氧化产物为
受热不稳定
C . 将红热的铂丝伸入如图所示的锥形瓶中,瓶口出现少量红棕色气红热体,说明氨气的氧化产物为  D . 如图红热的铂丝在反应过程中继续保持红热,说明该反应放热
D . 如图红热的铂丝在反应过程中继续保持红热,说明该反应放热
性质 | 用途 | |
A |
| 漂白纸浆 |
B |
| 化肥 |
C |
| 制冷剂 |
D |
| 刻蚀玻璃 |
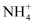 废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分)的流程如图所示。
废水和工业废气(主要含N2、CO2、SO2、NO、CO,不考虑其他成分)的流程如图所示。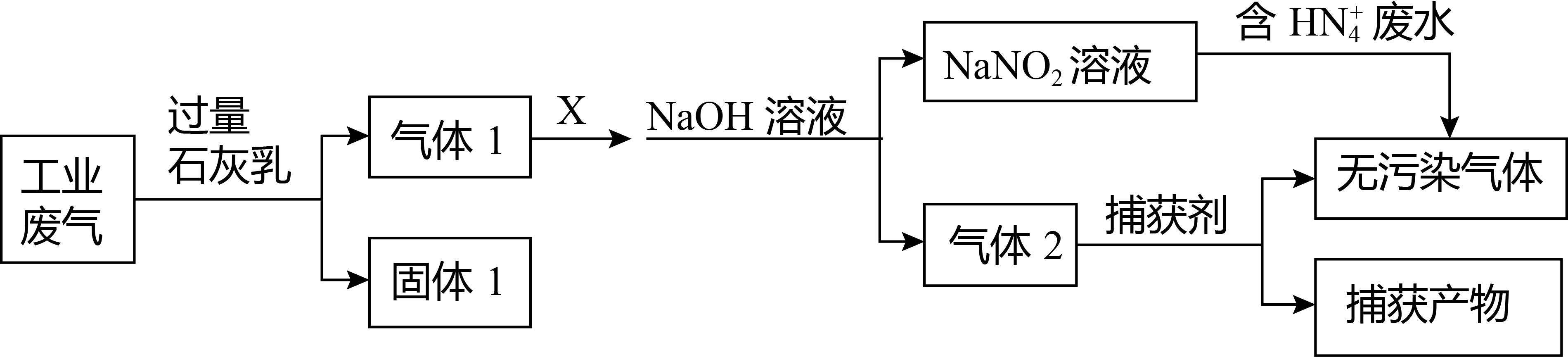
已知: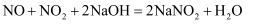
-
(1) 固体1的主要成分是。
-
(2) 流程中,试剂X的作用是(填“氧化剂”或“还原剂”) 。
-
(3) 捕获剂捕获的气体主要是。
-
(4) NaNO2溶液处理含
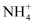 废水的离子方程式为。
废水的离子方程式为。
-
(5) 处理含
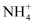 废水的另一种方法如图所示。
废水的另一种方法如图所示。
①过程a中需升温至30℃,产生大量气体,过程b产生大量无毒气体,达到了逐步降低溶液中
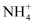 含量的目的。这两种气体分别是、。
含量的目的。这两种气体分别是、。②过程c中,余氯的主要成分是NaClO,NaClO的含量是7.45mg/L,则处理10 m3含余氯废水,理论上需要0.5mol·L-1 Na2SO3溶液L。
- C......
- 下列氧化还原反应中,水作为氧化剂的是( ) A.CO+H2OCO2+H2 B.Cl2
- 名著阅读。(任选一题作答) (1)《西游记》中,孙悟空炼就“火眼金睛”的情节充满了神奇色彩,请简述这个故事情节。 (2)
- 如图甲所示,一列简谐横波以1m/s的速度由A向B传播,质点A、B间的水平距离x=3m。若t=0时质点A刚从平衡位置开始向
- 近代民主思想与近代早期的“君权至上”思想相比 A.两者在各自的历史条件下都具有进步作用 B.后者没有历史进步意义 C.前
- HOW TO BOOK Bookingopens for Becket Shorts on 8 September Bo
- 下列关于电解质的叙述正确的是 A.溶于水能导电的化合物一定是电解质 B.熔融状态能导电的物质一定是电解质 C.易溶于水的
- Why______ you do everything as if you have towin? A. mus
- Professor Haley told me that he__________by many of his stud
- “人肉搜索”第一案一审落槌。一审判决认定:北飞的候鸟网站、大旗网披露当事人个人信息,导致网民进行“人肉搜索”,影响了原告
- 白头叶猴是我国的一种珍稀动物,保护白头叶猴最有效的方法是 A.消灭白头叶猴的所有天敌 B.为白头叶猴提供更多的肉食 C.
- 乒乓球比赛中,运动员打出“上弦球”,足球运动员踢出“香蕉球”,他们都是通过控制力的______、______、_____
- 图甲和图乙是两类细胞的亚显微结构模式图,图丙表示生物膜的亚显微结构图,请据图回答:(1)图甲细胞属于细胞,判断的理由是_
- NASA is moving ahead with plans to put a long-armed Lander o
- 下列诗句中与漫画哲学寓意相近的是 ①若非一身寒彻骨,哪得梅花扑鼻香 ②千淘万漉虽辛苦,吹尽狂沙始到金 ③不识庐山真面
- (08年合肥168中学联考)如图所示,一轻质杆一端用铰链固定在竖直墙面上,另一端固定一个定滑轮.一轻质细软绳一端系一个重
- “冬季下雨;夏季干燥”是哪种气候的主要特征 ( ) A.亚热带季风气候B.温带季风气候 C.地中海
- 实验室有一瓶存放时间过长的氢氧化钠,其中一部分已转化成为了碳酸钠。现需用该药品配制氢氧化钠溶液。取50克该药品,溶于20
- Lastyear, a special kind of glove came out. It was invented
- 如图是某化学反应的微观模型,“”“”分别表示不同元素的原子,下列各项中对图示模型理解正确的是()A.该反应属于分解反应
 和Fe3+
和Fe3+ 具有漂白性
具有漂白性 受热易分解
受热易分解 易溶于水
易溶于水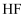 具有弱酸性
具有弱酸性


