常见的生活环境的污染及治理 知识点题库
下列说法不正确的是 ( )
A . 从性质的角度分类,SO2属于酸性氧化物
B . 从对大气及环境影响的角度,SO2是一种大气污染物
C . 从在水中是否发生电离的角度,SO2属于电解质
D . 从元素化合价的角度分类,SO2即可作氧化剂又可作还原剂
下列有关环境污染的说法正确的是( )
A . 燃煤时加入适量石灰石,可减少废气SO2的排放量
B . 空气中臭氧的含量越高,对人体健康越有利
C . pH在5.6﹣7之间的降水通常称为酸雨
D . 含磷洗涤剂易于被细菌分解,故不会导致水体污染
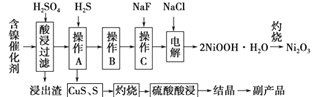
为回收利用废镍催化剂(主要成分为NiO,另含Fe2O3、CaO、CuO、BaO等),科研人员研制了一种回收镍的新工艺.工艺流程如图:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
开始沉淀的pH | 1.5 | 6.5 | 7.7 |
沉淀完全的pH | 3.7 | 9.7 | 9.2 |
已知常温下:①有关氢氧化物开始沉淀和沉淀完全
的pH如右表 ②Cu2O+2H+=Cu+Cu2++H2O
③常温时,Ksp(CaF2)=2.7×10﹣11
回答下列问题:
-
(1) 写出酸浸时Fe2O3和硫酸反应的化学方程式
-
(2) 浸出渣主要成分为CaSO4•2H2O和 两种物质.
-
(3) 操作B是除去滤液中的铁元素,某同学设计了如下方案:向操作A所得的滤液中加入NaOH溶液,调节溶液pH在3.7~7.7范围内,静置,过滤.请对该实验方案进行评价 (若原方案正确,请说明理由;若原方案错误,请加以改正).
-
(4) 流程中的“副产品”为 (填化学式).在空气中灼烧CuS可以得到铜的氧化物,向Cu、Cu2O、CuO组成的混合物中加入1L 0.6mol•L﹣1HNO3溶液恰好使混合物溶解,同时收集到2240mLNO气体(标准状况),若该混合物中含0.1molCu,与稀硫酸充分反应至少消耗 mol H2SO4 .
-
(5) 操作C是为了除去溶液中的Ca2+ , 若控制溶液中F﹣浓度为3×10﹣3mol•L﹣1 , 则溶液中
 =
=
-
(6) 电解产生2NiOOH•H2O的原理分两步:
①碱性条件下,Cl﹣在阳极被氧化为ClO﹣ , 则阳极的电极反应式为
②Ni2+被ClO﹣氧化产生2NiOOH•H2O沉淀.则该步反应的离子方程式为
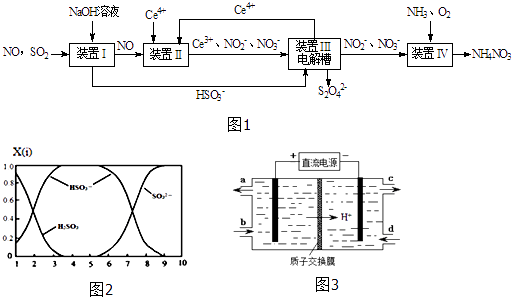
雾霾含有大量的污染物SO2、NO.工业上变“废”为宝,吸收工业尾气SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如图1(Ce为铈元素):
-
(1) 装置Ⅰ中的主要离子方程式为.
-
(2) 含硫各微粒(H2SO3、HSO3﹣和SO32﹣)存在于SO2与NaOH溶液反应后的溶液中,它们的物质的量分数X(i)与溶液pH的关系如图2所示.
①若是0.1mol NaOH反应后的溶液,测得溶液的pH=8时,溶液中个离子由大到小的顺序是.
②向pH=5的NaHSO3溶液中滴加一定浓度的CaCl2溶液,溶液中出现浑浊,pH降为2,用化学平衡移动原理解释溶液pH降低的原因:.
-
(3) 写出装置Ⅱ中,酸性条件下的离子方程式.
-
(4) 装置Ⅲ还可以使Ce4+再生,其原理如图3所示.
①生成Ce4+从电解槽的(填字母序号)口流出.
②写出与阴极的反应式.
-
(5) 已知进入装置Ⅳ的溶液中,NO2﹣的浓度为a g•L﹣1 , 要使1m3该溶液中的NO2﹣完全转化为NH4NO3 , 需至少向装置Ⅳ中通入标准状况下的O2L.(用含a代数式表示,计算结果保留整数)
某化学实验室产生的废液中含有Fe3+、Cu2+、Ag+三种金属离子,实验室设计了方案对废液进行以下三步处理,并回收金属.

请回答:
-
(1) 步骤①中得到的沉淀含有的金属单质有.
-
(2) 步骤②是将Fe2+转化为Fe3+ , 还可以选用的试剂是 .A . Fe粉 B . NaOH溶液 C . 新制氯水 D . 稀硫酸
-
(3) 步骤③中加入氨水生成红褐色沉淀的离子方程式为.
下列气体中,不会造成空气污染的是( )
A . NO2
B . NO
C . SO2
D . N2
生活环境逐渐恶化,人们日益重视环境问题,下列做法或说法正确的是( )
A . 推广使用无磷洗衣粉,以减少水体富营养化
B . PM2.5是指大气中直径接近于2.5μm(1m=106μm=109nm)的颗粒物,也称可吸入颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体
C . 为提高农作物产量大量使用农药和化肥
D . 对农作物秸秆进行焚烧还田,以增加土壤肥力
空气污染已成为人类社会面临的重大威胁.下列气体中,不会造成空气污染的是( )
A . NO2
B . Cl2
C . N2
D . SO2
某雨水样品刚采集时测得pH值为4.82,放在烧杯中经2小时后,再次测得pH值为4.68.以下叙述正确的是( )
A . 雨水样品酸度逐渐减小
B . 雨水样品酸度没变化
C . 雨水样品继续吸收空气中的CO2
D . 雨水样品中的H2SO3逐渐被空气中的氧气氧化成H2SO4
节能减排对发展经济,保护环境有重要意义.下列措施不能减少二氧化碳排放的是( )
A . 利用太阳能制氢
B . 推广使用煤液化技术
C . 举行“地球一小时”熄灯活动
D . 关停小火电企业
学好化学能使我们更好地认识各种现象,更轻松、合理地解决实际问题.请回答下列问题:
-
(1) 家里炒菜时油锅着火,最好的灭火方法是;
-
(2) 随着化石燃料使用量的迅猛增长,二氧化碳的排放量迅速增加,温室效应带来的负面影响日益显现,为了解决这一问题,我们应该;(一条建议即可)
-
(3) 2008年5月12日我国汶川发生特大地震灾害,救援人员发放净水片解决饮水问题.高铁酸钠是一种新型净水剂.高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3x+5H2O,试写出物质x的化学式.
下列说法不正确的是( )
A . 干冰可用于人工降雨
B . 过氧化钠常用作航天员的供氧剂
C . 乘车严禁携带易燃、易爆等危险品
D . 大量开采、使用可燃冰不会对环境造成影响
下列叙述中正确的是( )
A . 竹炭的结构疏松多孔,具有除异味和杀菌作用
B . 燃料的脱硫脱氮、SO2的回收利用和NOx的催化转化都是减少酸雨产生的措施
C . 纳米铁粉可以高效地去除被污染水体中的Pb2+、Cu2+、Cd2+、Hg2+等重金属离子,其本质是纳米铁粉对重金属离子较强的物理吸附
D . 利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
下列说法正确的是( )
A . 绿色食品就是指颜色为绿色的食品
B . 白色污染是指白色的废弃物的污染
C . 有机食品是指含有有机物的食品
D . 食盐加碘实质是在食盐中加入KIO3
“绿色化学”是指从技术、经济上设计可行的化学反应,尽可能减少对环境的副作用。下面化学反应不符合绿色化学理念的是( )
A . 消除硫酸厂尾气排放:SO2 + 2NH3 + H2O = (NH4)2SO3
B . 治理汽车尾气中NO和CO,可利用催化装置将NO与CO转化成CO2和N2
C . 制Cu(NO3)2:Cu + 4HNO3(浓) = Cu(NO3)2 + 2NO2↑+ 2H2O
D . 制CuSO4:2Cu + O2 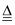 2CuO CuO + H2SO4 = CuSO4 + H2O
2CuO CuO + H2SO4 = CuSO4 + H2O
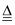 2CuO CuO + H2SO4 = CuSO4 + H2O
2CuO CuO + H2SO4 = CuSO4 + H2O
下列有关物质应用的说法错误的是( )
A . 氯气用于制备漂白粉
B . 单质硅用于制造光导纤维
C . 用明矾净化水
D . 燃煤时加入石灰石减少SO2排放
化学与生活密切相关,下列说法正确的是( )
A . 酒精浓度越大,对新冠肺炎病毒的杀菌消毒效果越好
B . 废旧电池属于有害垃圾,不可随意丢弃,需专门回收
C . “祝触号”火星车使用的铝基碳化硅复合材料属于有机高分子材料
D . 尽量使用含12C的产品,减少使用含13C或14C的产品,有利于实现碳中和
2022北京冬奥会是我国提出“2030碳达峰、2060碳中和”目标后的首个世界级体育盛会,冬奥会承诺碳排放将全部中和。下列技术中不能促进碳中和的是( )
A . 在火力发电中,对烟尘采用脱硫除尘处理减少空气污染
B . 张北风电、太阳能发电实现绿色用电
C . “平原用电、山地用氢”的原则,在各赛区推广电动汽车、氢燃料电池汽车
D . 中科院首次实现了从二氧化碳到淀粉的从头全合成
化学与环境密切相关,下列有关说法错误的是( )
A . NO2、NO含氮氧化物是光化学烟雾的主要污染物
B . 使用绿色工艺、开发绿色产品,从源头上消除污染
C . 加大农药和化肥的生产和使用量,以提高粮食的产量
D . 大气中CO2含量的增加会导致温室效应加剧
2022年北京冬奥会通过科技助力,体现环保理念。下列说法错误的是( )
A . 全部餐具均由可降解聚乳酸生物新材料制作,有效减少白色污染
B . 全部场馆采用光伏、风能产生100%绿色电力,实现零碳排放
C . 冬奥火炬“飞扬”采用氢气作燃料,氢气燃烧将热能转化为化学能
D . 国家速滑馆使用的二氧化碳跨临界直冷制冰系统,与传统制冷剂氟利昂相比更环保
最近更新
- 短周期元素W、X、Y、Z的原子序数依次递增,a、b、c、d、e、f是由这些元素组成的化合物,d为离子化合物,其结构中还含
- 一个单摆的摆球运动到最大位置时,正好遇到空中竖直下落的雨滴,雨滴均匀附着在摆球的表面,下列说法正确的是( ) A.
- 语文实践活动。(9分) 【活动一】阅读下面一则消息,然后回答问题。(7分) 记者日前获悉,为了让渔农村尽快跟上城市发
- 常温下,在25 mL 0.1 mol/L NaOH溶液中逐滴加入mL O.2 mol/L CH3COO溶液,有关混合溶液
- 下列各组词语中加点字读音完全正确的一项是 A.慰藉(jiè
- 设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )A.25℃时,pH=3的1.0LNaHSO3溶液中,含Na
- Jane is a great dancer, and _______ above the others with he
- 下列各组物质的无色溶液,不用其它试剂即可鉴别的是①KOH Na2SO4 AlCl3 ②NaHCO3
- 下面关于与异性同学交往的说法,你认为正确的是 A. 现在的主要任务是学习,不能与异性交往 B. 异性交往
- What does ATM _____? Automatic Teller Machine? A. stand for
- 下图为我国某集中团块式城市现状及规划范围图,据此完成 28~30题。 28. 该城市的布局模式不利于A.节约用地
- Most children like to watch TV. It’s veryinteresting. By wat
- 第Ⅱ卷 第四部分:书面部分(共两节,满分35分) 一.对话填空(满分10分) Tom: I’m (76) w______
- 地壳中含量最多的金属元素是 A.氧 B.硅 C.铝 D.铁
- Would you mind ________ the window,please? It’s so cold.
- There has been some progress insaving _______ wildlife in Ch
- 阅读理解,阅读下列短文,从各题A、B、C、D中选出能回答所提问题或完成所给句子的最佳答案。 Mr. Whitehad a
- 在图4-13中,若两物体的重力分别为GA=20 N,GB=40 N,A、B间动摩擦因数μ1=0.2,B与地面间动摩擦因数
- He drive us to the station, but we preferred to walk
- 经过一月的学习,你已经初步掌握实验室制取气体的有关知识,请结合图示回答问题: (1)写出图1中标号仪器的名称:①;②.



