探究卤素单质间的置换反应 知识点题库
某研究性学习小组设计了一组实验来探究元素周期律.甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种非金属元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律.图2中,A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红色石蕊试纸.(已知常温下浓盐酸与高锰酸钾能反应生成氯气)
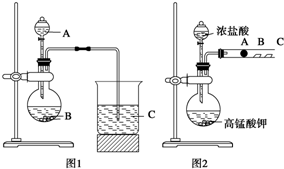
(1)甲同学实验中选用的物质化学式为:A ,B , C ;
(2)写出甲同学的实验中C处反应的离子方程式为 ,乙同学的实验中圆底烧瓶中发生反应的化学方程式为 ,B处的实验现象为 .
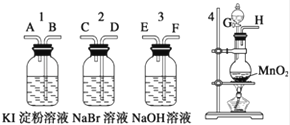
为了比较卤素单质的氧化性强弱,可在实验室先制取Cl2 , 并将Cl2依次通入NaBr溶液和淀粉KI溶液中.有如图所示的仪器(橡胶塞均为双孔)及药品,试回答:
(1)若所制气体从左向右流向时,上述仪器接口的连接顺序为H接 、 接 、 接 .
(2)装置3的作用是 ,反应的离子方程式为 .
(3)装置1中产生的现象是 ,反应的化学方程式为 .
(4)通过本实验可得到的结论是 .
为验证卤素单质氧化性的相对强弱,某小组用图所示装置进行实验(夹持仪器已略去,气密性已检验).
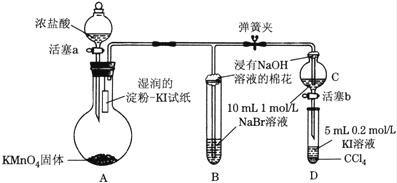
实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸.
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹.
Ⅲ.当B中溶液由黄色变为棕红色时,关闭活塞a.
Ⅳ…
(1)验证氯气的氧化性强于碘的实验现象是 .
(2)B中溶液发生反应的离子方程式是 .
(3)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是 .
(4)过程Ⅲ实验的目的是 .
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下随着核电荷数的增加, 的增多, 逐渐增大, 逐渐减弱,得电子能力逐渐减弱.
(1)提出问题:Fe3+、Br2谁的氧化性更强?
(2)猜想:
①甲同学认为氧化性:Fe3+>Br2 , 故上述实验现象不是发生化学反应所致.则溶液呈黄色是含 (填化学式,下同)所致.
②乙同学认为氧化性:Br2>Fe3+ , 故上述实验现象是发生化学反应所致,则溶液呈黄色是含 所致.
(3)设计实验并验证:
丙同学为验证乙同学的观点,选用下列某些试剂设计出两种方案进行实验,并通过观察实验现象,证明了乙同学的观点确实是正确的.供选用的试剂:
a.酚酞试液 b.四氯化碳 c.无水酒精 d.硫氰化钾溶液
请你在下列表格中写出丙同学选用的试剂及实验中观察到的现象.(试剂填序号)
选用试剂 | 实 验 现 象 | |
方案1 |
|
|
方案2 |
|
|
(4)应用与拓展:
①在足量的稀氯化亚铁溶液中,加入1~2滴溴水,溶液呈黄色所发生的离子反应方程式为 .
②在100mL FeBr2溶液中通入2.24LCl2(标准状况),溶液中有1/3的Br﹣被氧化成单质Br2 , 则原FeBr2溶液中FeBr2的物质的量浓度为 .
③若选用淀粉﹣碘化钾溶液验证上述猜想,是否可行? (填“是”或“否”),理由是 .
实验名称:ⅦA单质氧化性强弱比较
实验药品:NaBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸
实验设计:
实验步骤 | 实验结论 |
①氯水+1mLCCl4 , 振荡、静置, 观察四氯化碳层颜色 | 氧化性从强到弱的 顺序: Cl2>Br2>I2 |
②NaBr溶液+氯水+1mLCCl4 , 振荡、静置,观察四氯化碳层颜色 | |
③KI溶液+氯水+1mLCCl4 , 振荡、静置,观察四氯化碳层颜色 |
试回答:
(1)完成该实验所用到得实验仪器是 .
(2)CCl4在实验中所起的作用是 .
(3)该同学的实验设计不足之处是 ,改进的办法是 .
已知:①溴水为溴的水溶液,溴水为橙黄色,溴蒸气为红棕色,均有毒
②氯水为氯气的水溶液。
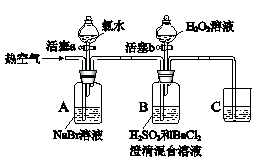
实验记录如下:
实验操作 | 实验现象 | |
Ⅰ | 打开活塞a,滴加氯水,关闭活塞a | A中溶液变为橙黄色 |
Ⅱ | 吹入热空气 | A中橙黄色明显变浅;B中有气泡,产生大量白色沉淀,混合液颜色无明显变化 |
Ⅲ | 停止吹入空气,打开活塞b,逐滴加入H2O2溶液 | 开始时颜色无明显变化;继续滴加H2O2溶液,一段时间后,混合液逐渐变成橙黄色 |
请回答下列问题:
-
(1) A中反应的离子方程式是。
-
(2) 实验操作II吹入热空气的目的是。
-
(3) 装置C的作用是。
-
(4) 实验操作III,混合液逐渐变成橙黄色,其对应的离子方程式是。
-
(5) 由操作I得出的结论是,由操作III得出的结论是。
-
(6) 实验反思:实验操作III,开始时颜色无明显变化的原因是(写出一条即可):。
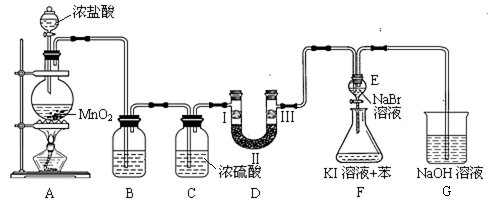
-
(1) 装置 B 中饱和食盐水的作用是。
-
(2) 装置 D 的作用是验证氯气是否具有漂白性,为此 D 中Ⅰ、Ⅱ、Ⅲ 处依次放入物质的组合应是(填字母编号)。
编号
Ⅰ
Ⅱ
Ⅲ
a
干燥的有色布条
碱石灰
湿润的有色布条
b
干燥的有色布条
无水氯化钙
湿润的有色布条
c
湿润的有色布条
碱石灰
干燥的有色布条
d
湿润的有色布条
无水氯化钙
干燥的有色布条
-
(3) 设计装置 F 的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开 E 中活塞,将装置 E 中少量溶液加入装置 F 中,振荡,观察到的现象是 ,该现象(填“能”或“不能”)说明溴单质的氧化性强于碘单质,原因是。
-
(4) 实验室也可以用高锰酸钾和浓盐酸反应来制备氯气,反应的化学方程式为:
2KMnO4 + 16HCl(浓) = 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O
①在化学方程式上用双线桥法标出该反应中电子转移的方向和数目 。
②在该反应中,氧化剂是。
③上述反应中,有126. 4 g 的 KMnO4 参加反应,若将生成的氯气全部通入足量的石灰乳中,理论上可得到次氯酸钙多少克?
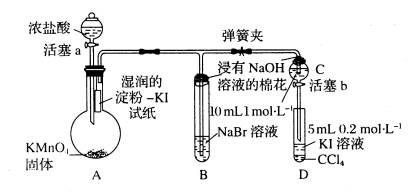
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为红棕色时,关闭活塞a。
IV.……
-
(1) A中产生黄绿色气体的化学反应方程式是。
-
(2) 验证氯气的氧化性强于碘的实验现象是。
-
(3) B中溶液发生反应的离子方程式是。
-
(4) 为验证溴的氧化性强于碘,过程Ⅳ的操作是,现象是。
-
(5) 过程III实验的目的是。
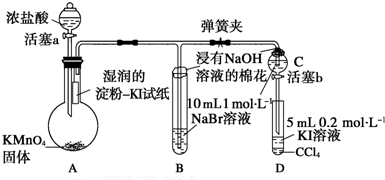
实验过程:
Ⅰ. 打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ. 当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ. 当B中溶液由黄色变为棕红色时,关闭活塞a。
Ⅳ.……
-
(1) A中产生黄绿色气体,其电子式是。
-
(2) 验证氯气的氧化性强于碘的实验现象是。
-
(3) B中溶液发生反应的离子方程式是。
-
(4) 为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是。
-
(5) 过程Ⅲ实验的目的是。
-
(6) 氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下,得电子能力逐渐减弱。
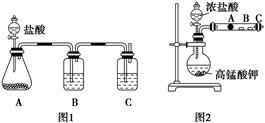
甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成碳族元素中C与Si的非金属性强弱比较的实验研究;
乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
-
(1) 甲同学设计实验的依据是强酸制弱酸,请回答下列问题
A中锥形瓶装入的是碳酸钙固体,A中发生的离子方程式为:,
B应放入的物质是,其作用为;
C中是Na2SiO3溶液该反应的离子方程式为。
-
(2) 乙同学的实验原理是强氧化剂生成弱氧化剂。
如果A处的棉花由白色变成棕色,则A处的离子方程式为B处的现象是 。
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 酸性:HCl>H2S | 非金属性:Cl>S |
| B | 铁表面镀锌可以增强其抗腐蚀性 | 构成原电池且铁作负极 |
| C | Na在Cl2中燃烧的生成物含离子键 | NaCl固体可导电 |
| D | 向NaI溶液中滴入少量氯水和苯,振荡、静置,溶液上层呈紫红色 | I-还原性强于Cl- |
-
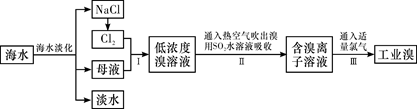
(1) 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序正确的是__________。A . NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸 B . BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸 C . NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸 D . Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
-
(2) 步骤Ⅰ中已获得Br2 , 步骤Ⅱ中又将Br2还原为Br- , 其目的是。写出步骤Ⅱ中发生反应的离子方程式:。
-
(3) 制备钠单质的方法之一是将熔融NaCl进行电解,写出电解化学方程式:。
-
(4) 已知某溶液中Cl-、Br-、I-的物质的量之比为2∶3∶4,现欲使溶液中的Cl-、Br-、I-的物质的量之比变成4∶3∶2,那么要通入Cl2的物质的量是原溶液中I-的物质的量的_____。(填选项)A .
 B .
B .  C .
C . 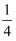 D .
D . 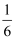
-
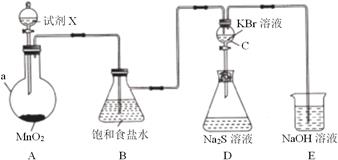
(1) 仪器a的名称是。试剂X 是。
-
(2) 写出装置A中发生反应的化学方程式。
-
(3) 装置E中NaOH溶液的作用是。
-
(4) 反应一段时间后,观察到装置C中溶液变为橙黄色,说明非金属性:ClBr( 填“>"或"<")。
-
(5) 打开装置C中的活塞,将装置C中的溶液逐渐滴人装置D中,振荡。观察到的现象是,写出可能发生反应的离子方程式:(写一个即可),根据此现象不一定能说明溴的非金属性比硫强,原因是。
下列说法错误的是( )
-
(1) I.将钠、镁各2 g分别投入盛足量冷水的烧杯中,实验结果:与冷水剧烈反应;另取镁、铝各2 g 分别投入足量0.05 mol/L盐酸中,与盐酸反应最剧烈。
-
(2) 向Na2SiO3溶液中通入CO2出现胶状沉淀,可证明元素得电子能力>,反应的离子方程式为。
实验结论:随原子序数增大,同周期元素失电子能力依次(填“增强”或“减弱”,下同),得电子能力依次。
-
(3) II.利用如图装置可验证同主族元素非金属性的变化规律。
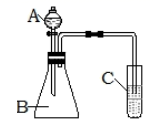
仪器A的名称为。
-
(4) 若要证明非金属性:Cl>Br,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加KBr溶液和CCl4.反应一段时间后,将C振荡、静置,观察到C中现象是。此装置存在的不足之处是。
选项 | 实验 | 现象 | 结论 |
A | 向 | 产生白色沉淀,且有无色气体生成 | 溶液中 |
B | 检验某无色溶液中是否含有 | 溶液变黄色且试管上部产生红棕色气体 | 该溶液中含有 |
C | 将铜粉放入稀硫酸溶液中并不断通入 | 铜粉快速溶解,溶液变为蓝色 | 形成 |
D | 向某钾盐中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为 |
- 下列各组物质中,前者属于单质、后者属于氧化物的是 A.氢气 大理石 B.生
- 解析:已知中,,. 故选D.
- 66.How many (德国人)are going to visit their town next
- 如图所示,质量为4 kg的物体静止于水平面上,物体与水平面间的动摩擦因数为0.5,物体受到大小为20N,与水平方向成37
- 工具的改进是促进中国古代农业发展的重要条件。与图一相比,图二工具的进步之处在于 ()图一图二 A.合理利用水资源
- 关于质点做简谐运动,下列说法中正确的是( ) A.在某一时刻,它的速度和回复力的方向相同,与位移的方向相反 B.在
- 下列说法正确的是 ( )A.物质的量可理解为物质的质量 B.物质的量是国际单位制中的一个物理量C.物质的
- 下列实验现象的描述中,正确的是 A.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体熔化溅落下来 B.木炭在氧气中剧烈
- 汶川地震过后,一些不法分子蠢蠢欲动,抢劫、盗窃等案件在废墟累累的灾区中时有发生。地震发生后,公安部紧急抽调公安特警333
- 下列叙述正确的是A.元素的单质可由氧化或还原含该元素的化合物来制得B.得电子越多的氧化剂,其氧化性就越强C.阳离子只能得
- 市场销售的“84”消毒液,其商品标识上有如下叙述,其有效成分可能是() ①本品为无色液体,呈碱性 ②使用时加水稀释 ③可
- ⑴计算 ⑵化简,并计算当时代数式的值.
- 如图是生态系统中碳循环示意图,“→”表示碳的流动方向,下列说法正确的是A.图中A是生产者,B.D.E是消费者,C是分解者
- 设A={x|<0},B={x|x2+ax+b≤0},A∩B=, A∪B={x|-5<x≤2. 求实数a,b的值.
- 阅读下面的文字,完成1-4题。 烟花三月下扬州 熊召政 ①扬州古称广陵,人们又叫它维扬。清代之前,扬州因靠着大运河,一向
- .史学家陈寅恪认为:“华夏民族之文化,历数千年之演进,造极于赵宋之世。”宋代文化高度繁荣,在科技领域的表现有 A.发明造
- 在电解水制取H2和O2时,为了增强溶液的导电性,常加入一些电解质。下列物质中最合适的是 A.Na2SO4B.CuC12
- 如图13-7-8所示,边长为L的等边三角形三个顶点a、b、c处在匀强电场中,且电场线与a、b、c共平面.一个电子只在电场
- (2009上海卷)38.我国人民代表大会制度已经走过了55年的历程。这一制度,植根于中华民族赖以生存和发展的广阔沃土。产
- 自2012年7月份开始,我国合理调整城市居民生活用水价格,稳步推进阶梯式水价制度,推进农业水价综合改革,探索实行农民定额
 溶液中滴入
溶液中滴入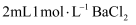 溶液
溶液 部分电离出
部分电离出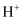 和
和 ,
,  与
与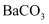 沉淀,促进了
沉淀,促进了 的电离,使
的电离,使
 , 取少量该溶液于试管中,加稀盐酸酸化,再加入
, 取少量该溶液于试管中,加稀盐酸酸化,再加入 溶液
溶液 , 再在溶液中滴加少量
, 再在溶液中滴加少量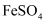 溶液
溶液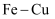 原电池,加快反应速率
原电池,加快反应速率 或
或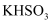 或者二者混合物
或者二者混合物


