海带成分中碘的检验 知识点题库
①通入足量Cl2 ②将海带焙烧成灰后加水搅拌 ③加CCl4振荡 ④用分液漏斗分液 ⑤过滤 合理的操作顺序是.
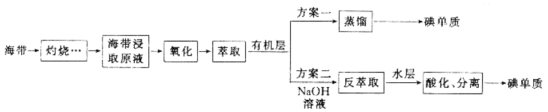
材料一:苏教版《化学1(必修)》工业上从海产品(海带)中获取碘的流程图如下:
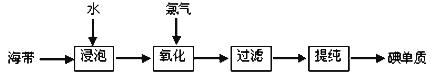
回答(1)~(3)三个小题:
-
(1) 上述生产流程的第一步是“浸泡”,它的实验目的是
-
(2) “氧化”这一操作中可供选用的试剂:Cl2、Br2、浓硫酸和H2O2(滴加稀硫酸),从无污染角度考虑,你认为选择的合适试剂是 ,反应中I﹣转化为I2的离子反应方程式为
-
(3)
上述的生产流程中,“提纯获得单质碘”一般认为经历两步,你认为应选择的实验装置分别是 (按操作的先后顺序填写);
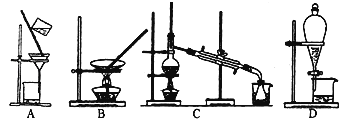
-
(4) 材料二:我国实际工业利用海带制取碘,采用的是离子交换法,其流程如下:
淡干海带→浸泡→浸泡液净化→上层清液→酸化→氧化→离子交换树脂吸附→解吸→碘析→精制→成品碘↓残渣(加热)→上层清液→返回
试回答(4)~(6)三个小题:
(4)实际工业生产中,酸化、氧化的方法是先加入硫酸酸化,使pH降低到2,然后加入次氯酸钠一类的氧化剂,使碘离子氧化.工业通常不用氯气氧化原因是: 写出该过程的离子方程式
-
(5) 有资料显示,为减少化学物质对环境的污染,工业可以采用电化学法制备,在 (填“阴极”或“阳极”)可以收集到碘单质.写出该极的电极方程式
-
(6) 上述的生产流程中离子交换树脂是用碱性树脂吸附,再用亚硫酸钠一类还原剂解吸,请问树脂吸附的碘元素状态是 (填写“游离态”或“化合态”).解吸后应加入 (填写下列编号:A.氧化剂、B.还原剂)可以实现碘析.
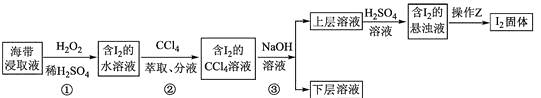
下列说法正确的是
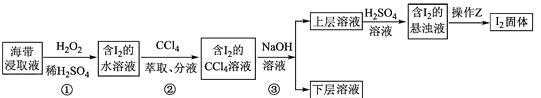
下列说法正确的是( )
实验(一) 碘含量的测定
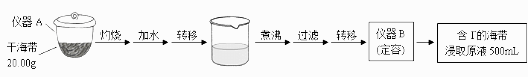
取0.0100 mol·Lˉ1的AgNO3标准溶液装入滴定管,取100.00 mL海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势(E)反映溶液中c(Iˉ)的变化,部分数据如下表:
V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
E/mV | -225 | -200 | -150 | -100 | 50.0 | 175 | 275 | 300 | 325 |
实验(二)碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:
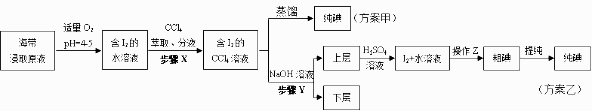
已知:3I2+6NaOH=5NaI+NaIO3+3H2O。
请回答:
-
(1) ①实验(一)中的仪器名称:仪器A,仪器B。
②该次滴定终点时用去AgNO3溶液的体积为mL,计算得海带中碘的百分含量为%。
-
(2) ①步骤X中,萃取后分液漏斗内观察到的现象是。
②下列有关步骤Y的说法,正确的是。
A.应控制NaOH溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.NaOH溶液可以由乙醇代替
③实验(二)中操作Z的名称是。
-
(3) 方案甲中采用蒸馏不合理,理由是。
-
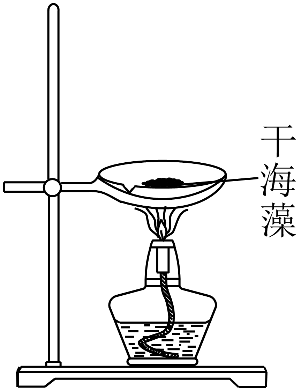
(1) 第1步:灼烧。操作是将足量海带灼烧成灰烬。该过程中将使用到的硅酸盐质实验仪器有________(填代号,限填3项)。A . 试管 B . 瓷坩埚 C . 坩埚钳 D . 铁三脚架 E . 泥三角 F . 酒精灯 G . 烧杯 H . 量筒
-
(2) 第2步:I-溶液的获取。主要操作为。
-
(3) 第3步:氧化。操作是依次加入合适的试剂。下列氧化剂最好选用(填代号),离子方程式为。
A.浓硫酸
B.新制氯水
C.KMnO4溶液
D.H2O2
-
(4) 第4步:碘单质的检验。操作是取少量第3步的溶液,滴加淀粉溶液,如果溶液显色,则证明海带中含碘。
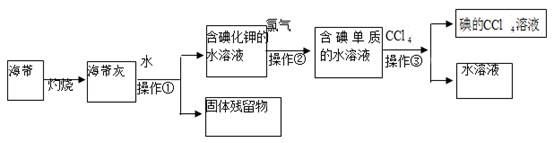
请回答下列问题:
-
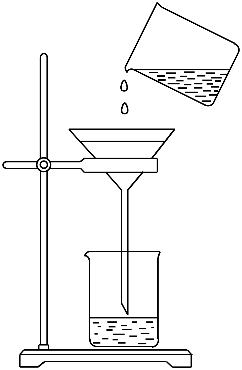
(1) 操作①的名称为、;
-
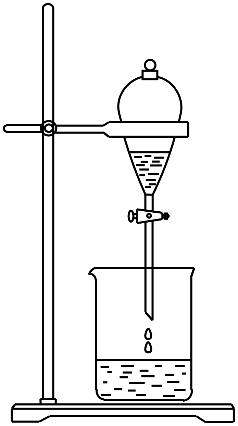
(2) 向含碘单质的水溶液中加入CCl4振荡、静置后,观察到的现象是;
-
(3) 操作③中,将含碘单质的水溶液与CCl4在分液漏斗中混合、振荡摇匀放在铁架台的铁圈上,分液漏斗的下端尖嘴处紧贴在承接的烧杯内壁上静置后,下面的操作步骤是。
-
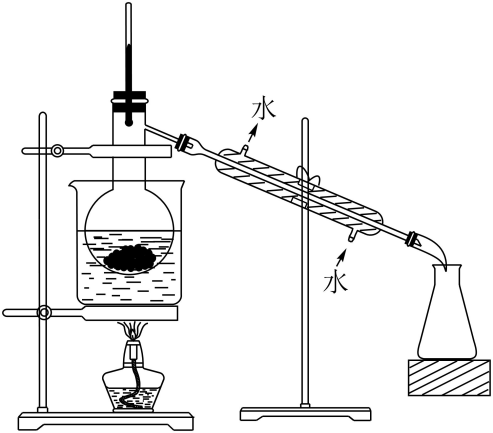
(4) 从含碘的有机溶剂中经过蒸馏可以提取碘和回收有机溶剂,该实验需要的主要玻璃仪器除酒精灯、烧杯、温度计、锥形瓶、牛角管外,还需要,实验中温度计水银球所处位置为。
-
(1) 验证“含
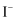 溶液”和“含
溶液”和“含  溶液”中含有的
溶液”中含有的 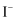 和
和  所需的试剂分别是和。
所需的试剂分别是和。
-
(2) 步骤④的反应中
 被还原为
被还原为  ,反应的离子方程式为;
,反应的离子方程式为;  、稀硫酸可用代替。
、稀硫酸可用代替。 a.
 b.
b.  c.
c.  、稀硫酸 d.
、稀硫酸 d. 
-
(3) 海带灰中含有的可溶性硫酸盐、碳酸盐等,在实验步骤(填序号)中实现与碘分离。
-
(4) 某同学制得的粗碘中含有少量
 ,对粗碘进行提纯的装置如图所示,采用的分离方法是;a、b为冷凝水进出口,其中(填“a”或“b”)接水龙头,最终能得到较多较高纯度的单质碘。
,对粗碘进行提纯的装置如图所示,采用的分离方法是;a、b为冷凝水进出口,其中(填“a”或“b”)接水龙头,最终能得到较多较高纯度的单质碘。
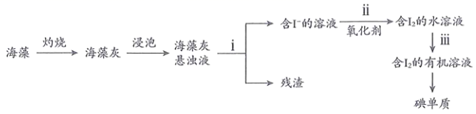
-
(1) 指出上述过程中有关实验操作的名称,步骤i:,步骤iii:。
-
(2) 步骤ii中可使用
 ,从原子结构角度说明理由:。
,从原子结构角度说明理由:。  过量时,可能无法获得
过量时,可能无法获得  ,原因是
,原因是  会被继续氧化为
会被继续氧化为  ,该反应的离子方程式为。
,该反应的离子方程式为。
-
(3) 当使用
 做氧化剂时,
做氧化剂时, 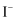 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。 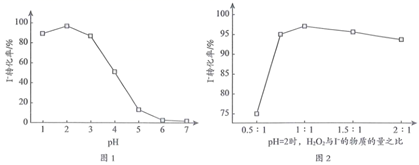
①图1中,
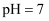 时
时 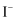 转化率几乎为0,结合离子方程式解释原因:。
转化率几乎为0,结合离子方程式解释原因:。②图2中,
 与
与 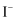 物质的量之比从0.5﹕1提高至1﹕1时,
物质的量之比从0.5﹕1提高至1﹕1时,  的转化率明显增大,可能的原因是(写出2条)。
的转化率明显增大,可能的原因是(写出2条)。
-
(1) Ⅰ.某同学依据反应
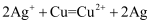 设计的原电池如图所示。
设计的原电池如图所示。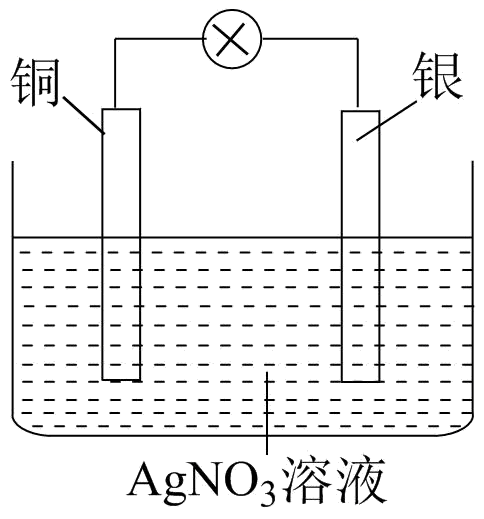
负极上发生的电极反应为。
-
(2) 溶液中
 流向(填“
流向(填“ ”或“
”或“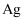 ”)电极。
”)电极。
-
(3) 当反应进行一段时间后取出电极材料,测得某一电极增重了5.4g,则反应中转移的电子数目是
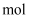 。
。
-
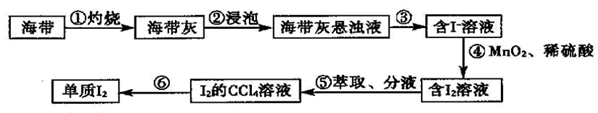
(4) Ⅱ.海带中含有非富的确元素,某化学研究性学习小组用如图流程从海带中提取碘:
步骤①灼烧海带时,除需要三脚架、泥三角、酒精灯外,还需要用到的实验仪器是____(填字母)。
A . 烧杯 B . 蒸发皿 C . 坩埚 D . 干燥器: -
(5) 步骤③、⑥的实验操作名称分别是、。步骤⑤中,除选择用苯来提取碘,还可选择的试剂是(填字母)。
A.酒精 B.醋酸 C.四氯化碳
 B . 配制0.1mol·L-1 NaCl溶液
B . 配制0.1mol·L-1 NaCl溶液 C . 制备时收集乙酸乙酯
C . 制备时收集乙酸乙酯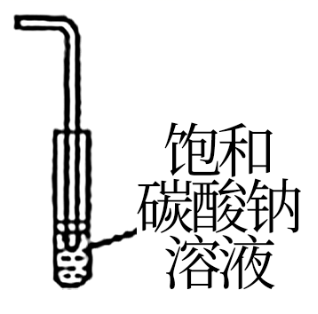 D . 灼烧海带变为灰烬
D . 灼烧海带变为灰烬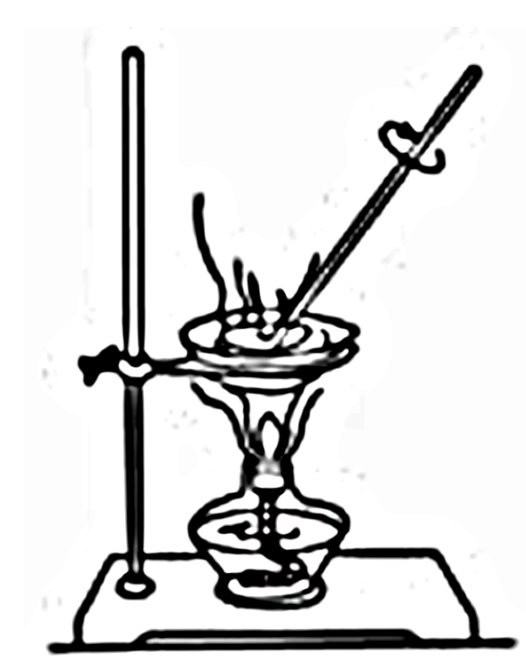
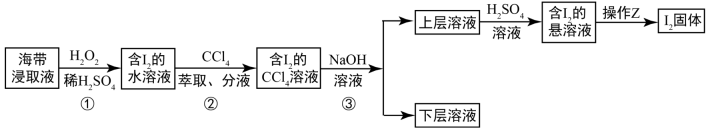
下列说法正确的是( )
![]()
|
|
|
|
A | B | C | D |
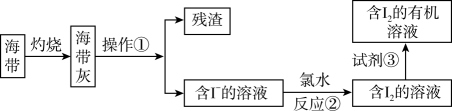
 D . 试剂③可以选用无水乙醇
D . 试剂③可以选用无水乙醇
 B . “氧化”时,试剂可选用O2、H2O2或Br2
C . 上述流程包括三个氧化还原反应和三种分离操作
D . “反萃取”时,反应的离子方程式为I2+2OH-=I-+IO
B . “氧化”时,试剂可选用O2、H2O2或Br2
C . 上述流程包括三个氧化还原反应和三种分离操作
D . “反萃取”时,反应的离子方程式为I2+2OH-=I-+IO +H2O
+H2O
 形式存在。在实验室中,从海带灰中提取碘的流程如下:
形式存在。在实验室中,从海带灰中提取碘的流程如下: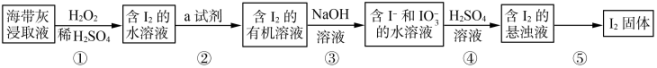
回答下列问题:
-
(1) 实验室灼烧海带的主要仪器有酒精灯、三脚架、泥三角、玻璃棒、等;
-
(2) 指出上述提取碘的过程中有关实验操作的名称:步骤②,步骤⑤;
-
(3) 写出步骤①中发生反应的离子方程式:;
-
(4) 步骤②中提取碘的过程中,可选择的有机试剂是____(填编号);A . 酒精 B . 醋酸 C . 四氯化碳 D . 苯
-
(5) 写出步骤④中发生反应的离子方程式:,在此反应中,每生成
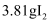 转移mol电子;
转移mol电子;
-
(6) 上述流程中,含
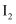 的水溶液经3步转化为含
的水溶液经3步转化为含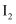 的悬浊液,主要目的是。
的悬浊液,主要目的是。
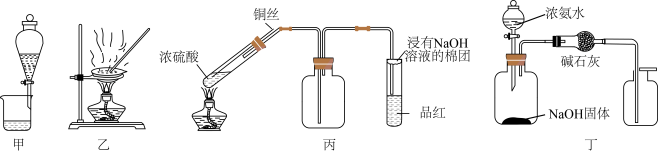

- ( ) A. B. C.i
- 观察图a和图b,根据盖斯定律,写出△H1、△H2、△H3、△H4、△H5和△H6的关系。图a:
- 下列词语中,字形全都正确的一项是 A.绣闼 暮蔼 鳏寡孤独 举案齐眉 B.祗候 忤逆 繁文
- 早期欧美资产阶级革命宣告新时代的到来。下列表述不正确的是 ( )A.英国通过革命确立起君主立宪制的资产阶级统治,
- 某人以1m/s的速度沿着平直的河堤行走,他在平静的河水中的倒影相对于河堤的速度是() A.1m/s
- 当氧化铜中混有少量木炭粉时,除去木炭粉的方法是 ( ). A.隔绝空气加热混
- 此题要求改正所给短文的错误。对标有题号的每一行做出判断: 如无错误,在该行右边横线上划一个勾(√);如有错误(每行只有一
- 新文化运动中,陈独秀发表文章说:“输入西洋式社会国家之基础,所谓平等人权之新信仰,对于此新社会、新国家、新信仰不可相容之
- 阅读下面两首诗,完成小题。 含山店梦觉作 [唐]韦庄 曾为流离惯别家,等闲挥袂客天涯。 灯前一觉江南梦,惆怅起来山月斜。
- 如图2-1-13所示,在PQ、QR区域是存在着磁感应强度大小相等、方向相反的匀强磁场,磁场方向均垂直于纸面,bc边与磁场
- 与“学而时习之,不亦说乎”的“说”意义和用法相同的一项是( ) A.说尽心中无限事B.而听细说,欲诛有功之人C.秦
- After 21 years of marriage, I started to go out with
- 如图1—63所示,某货船以20海里/时的速度将一批重要物资由A处运往正西方向的B处,经16小时到达,到达后立即卸货,此时
- 短文改错 Time flies! In four years our school will celebrate the
- IfI drive in this city myself, I’ll probably get lost as I h
- 较为保守的人士徒劳无益地抱怨说,没有什么是神圣的了,上帝自己也受到审查了,《圣经》被要求在理性的法庭上提交自己的证明材料
- With little knowledge about the area he succeeded ______ man
- 有些物理量的大小不易直接观测,但它变化时引起其他量的变化却容易直接观测。用易观测的量显示不易观测的量,是制作测量仪器的一
- N2O5是一种新型硝化剂,在一定温度下可发生以下反应: 2N2O5(g) 4NO2 (g)+ O2(g) ΔH &g
- —I don't know______ next.—Why not__ __ your teacher for advi