碳族元素简介 知识点题库
(1)密度最小的气体 ;
(2)天然气的主要成分 ;
(3)固体可用于冷藏食物和人工降雨的物质 ;
(4)实验室用于制取氧气的物质 ;
(5)俗名为烧碱的物质 ;
(6)用于治疗胃酸过多的药物
(1)CO2和SiO2都是非金属氧化物,分子中既有o键又有π键的是 .属于原子晶体的是 ,SiO2中原子轨道的杂化形式为 .
(2)碳和硅有关键键能如下表所示,简要分析解释下列有关事实:
①硅和碳都能形成系列氢化物,但硅烷在种类和数量上都远不如烷泾多,原因是
②SiH4的稳定性小于CH4 , 更易生成氧化物,原因是
化学键 | C﹣C | C﹣H | C﹣O | Si﹣Si | Si﹣H | Si﹣o |
键能(Kj/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
(1)铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为 周期第 族.
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为
(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为 :PbO2也可以通过石墨为电极,Pb (NO3)2和Cu(NO3)2的混合溶液为电解液电解制取.阳极发生的电极反应式
-
(1) I.碳元素广泛存在于自然界中,对人类生命和生活具有重要意义。含碳化合物在工业生产和国防建设中有广泛的应用。
碳元素原子核外有个未成对电子,最外层有种能量不同的电子。CH4 分子的空间构型为,是分子。(填“极性”或“非极性”)
-
(2) 碳和硅是同主族元素,下列能说明二者非金属性相对强弱的是(填编号)
a.CH4的稳定性比SiH4强 b.SiH4的沸点比CH4高
c.碳酸是强酸,硅酸是弱酸 d.碳原子半径比硅原子小
-
(3) II.氮化硅(Si3N4)是一种重要的陶瓷材料,可用石英与焦炭在800℃氮气气氛下合成:3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g) 该反应的平衡常数表达式K=。已知平衡常数:K(800℃)>K(850℃),则正反应是反应(填“放热”或“吸热”)
-
(4) 任写两种能提高二氧化硅转化率的措施、。
-
(5) 一定温度下,在2 L密闭容器内,充入一定量的反应物,5分钟时达到平衡,测得容器内气体增加了0.4mol,用CO表示该反应时间内的反应速率为。
 、Cl-、微生物、有机物等进行检测和分析
B . 化学科研工作者可从事特定功能新分子合成、节能环保物质转化工艺的研发等
C . 科技考古研究人员是靠文献记载、年历学和各种有纪年文字的遗物来断定文物的绝对年代
D . 测试工程师可通过化学检测仪或化学检测方法测出不锈钢中的某些组成元素及其含量来确定不锈钢的等级
、Cl-、微生物、有机物等进行检测和分析
B . 化学科研工作者可从事特定功能新分子合成、节能环保物质转化工艺的研发等
C . 科技考古研究人员是靠文献记载、年历学和各种有纪年文字的遗物来断定文物的绝对年代
D . 测试工程师可通过化学检测仪或化学检测方法测出不锈钢中的某些组成元素及其含量来确定不锈钢的等级
选项 | A | B | C | D |
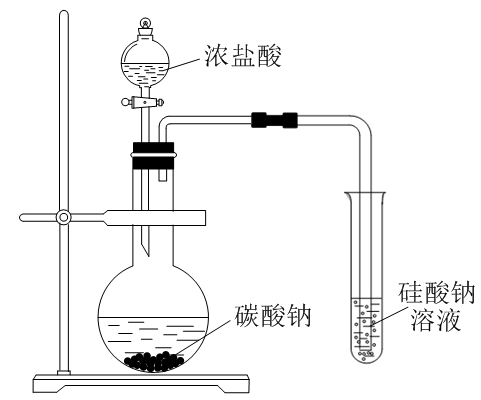
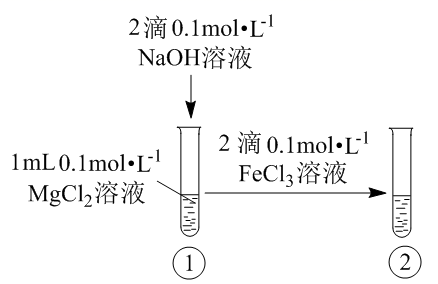
实验及现象 |
热水中烧瓶内气体颜色变深 |
试管中出现白色沉淀 |
①中产生白色沉淀②中产生红褐色沉淀 |
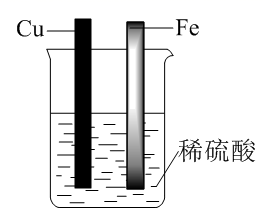
Cu上无气泡,Fe上有气泡 |
结论 | 2NO2(g) | 酸性:H2CO3>H2SiO3 | 溶解度:Mg(OH)2>Fe(OH)3 | 还原性:Fe>Cu |
-
(1) 已知金刚石的莫氏硬度为10,石墨的莫氏硬度为
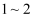 , 从晶体结构的角度解释金刚石硬度很大,石墨很软的原因。
, 从晶体结构的角度解释金刚石硬度很大,石墨很软的原因。
-
(2) 在相同温度时,酸性条件下
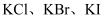 都能被
都能被 氧化,通过控制溶液中
氧化,通过控制溶液中 探究同浓度的
探究同浓度的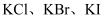 还原性强弱,预测同浓度的
还原性强弱,预测同浓度的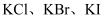 被
被 氧化需要的
氧化需要的 最小的是,试从离子结构角度解释
最小的是,试从离子结构角度解释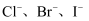 的还原性逐渐增强的原因。
的还原性逐渐增强的原因。
- 右图示某种农作物品种①和②培育出⑥的几种方法,有关说法正确的是 A. Ⅳ过程和Ⅴ过程都需要逐代自交的方式获得品种⑥ B.
- 下列关于植物激素的叙述,不正确的是 A.喷施赤霉素溶液或赤霉菌培养基滤液都能促进水稻生长 B.植物正常生长发育过程是多种
- 随着微电子制造技术的不断进步,电子元件的尺寸大幅度缩小,在芯片上某种电子元件大约只占0.0000007(平方毫米),这个
- 一束由红、蓝两单色光组成的光线从一平板玻璃砖的上表面以入射角射入,穿过玻璃砖自下表面射出。已知该玻璃对红光的折射率为。设
- 下列关于化学实验的“目的一操作一现象一结论”的描述正确的是( ) 实验过程 组别 实验目的 所加试剂 (或操作)
- 1.依次填入下列各句横线处的成语,最恰当的一组是 ( ) ①还有一种坏处,是一做教员,未免有顾忌;教授有教授
- 当m______时,方程(m-1)x2+2mx+m-3=0有两个实数根.
- 2005年10月19日,中国国务院新闻办公室发表了《中国的民主政治建设》白皮书。回答1~4题。 1、白皮书指出:到200
- Welcome to the Story County Family. It is a community servic
- 鼎被视为传国重器、国家和权力的象征,鼎又是旌功记绩的礼器。周代的国君或王公大臣在重大庆典或接受赏赐时都要铸鼎,以记载盛况
- 有一块表面被氧化成氧化钠的金属钠,质量为0.584 g,放入9.436 g水中,当反应结束时可生成氢气0.02 g。(1
- I have ____ orange._______ orange is green. A.an; The B
- 以下说法不正确的是( ) A. 1mol乙醇可以与足量的乙酸作用,生成1mol 乙酸乙酯,能证明乙醇分子有一个H原子
- ,he never seems able to do the work beautifully. A、Try
- 质量为m、电荷量为q的质点,在静电力作用下以恒定速率v沿圆弧从A点运动到B点,其速度方向改变的角度为θ(rad),AB弧
- 若2a-b=5,则多项式6a-3b的值是 。
- 如图所示,灯泡L标有“6V 6W”字样(灯泡电阻不受温度影响),滑动变阻器的最大阻值为12Ω,电源电压为6V保持不变。
- 18.下列各句中,没有语病的一句是( )(3分) A.国家正在加大交通基础设施建设,特别是中西部的交通基础设施,用
- 下图是我国近代民族资本主义工业发展趋势示意图,下列诗句比较恰当地反映了中国民族资本主义工业在B处的发展状况的是 A
- 下列说法错误的是( )A.Na2SO3与BaCl2溶液作用,有白色沉淀生成,加稀HNO3后沉淀消失B.将SO2气体
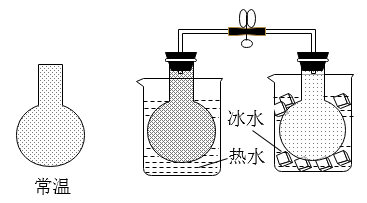
 N2O4(g)是放热反应
N2O4(g)是放热反应


