氢氧化铝的制取和性质探究 知识点题库
以氧化铝为原料制取氢氧化铝,最好的方法是( )
A . 将氧化铝溶于水
B . 将氧化铝先溶于盐酸中,之后滴加氨水
C . 将氧化铝溶于盐酸中,之后滴加氢氧化钠溶液
D . 将氧化铝溶于氢氧化钾溶液
将氢氧化钠溶液和氯化铝溶液等体积混合,得到的沉淀物中铝元素的质量与溶液中所含铝元 素的质量相等,则原氢氧化钠溶液和氯化铝溶液的物质的量浓度之比可能是( )
A . 3∶1
B . 4∶1
C . 3∶2
D . 7∶2
常温下,向下列溶液中通入CO2马上有沉淀产生的是( )
A . NaOH稀溶液
B . NaAlO2溶液
C . 饱和NaHCO3溶液
D . CaCl2溶液
已知A、B、D、E均为化学中的常见物质,它们之间的转化关系如图所示(部分产物略去),则下列有关物质的推断不正确的是( )
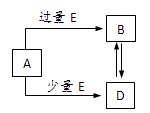
A . 若A是铁,则E可能为稀硝酸
B . 若A是CuO,E是碳,则B为CO
C . 若A是NaOH溶液,E是CO2 , 则B为NaHCO3
D . 若A是AlCl3溶液,E可能是氨水
欲将溶液中的Al3+沉淀完全,最合适的试剂是( )
A . NaOH溶液
B . 氨水
C . Na2SO4溶液
D . NaCl溶液
不能溶解新制氢氧化铝的溶液是()
A . 碳酸
B . 氢氧化钾
C . 盐酸
D . 硫酸
下列图像与选项对应的是( )
A . 氯化铝中滴加氢氧化钠溶液 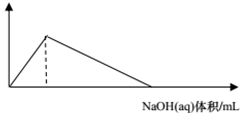 B . 氢氧化铝溶液中滴加硝酸钠
B . 氢氧化铝溶液中滴加硝酸钠 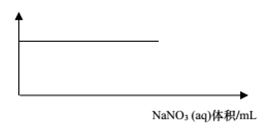 C . 氯化铝中滴加氨水
C . 氯化铝中滴加氨水 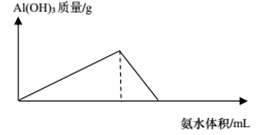 D . 氢氧化铝溶液中通入CO2
D . 氢氧化铝溶液中通入CO2 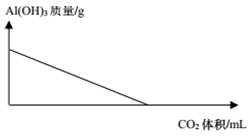
 B . 氢氧化铝溶液中滴加硝酸钠
B . 氢氧化铝溶液中滴加硝酸钠  C . 氯化铝中滴加氨水
C . 氯化铝中滴加氨水  D . 氢氧化铝溶液中通入CO2
D . 氢氧化铝溶液中通入CO2 
学习化学应明确“从生活中来,到生活中去”的道理,请回答下列问题:
-
(1) 漂粉精中有效成分的化学式为.
-
(2) “硅材料”是无机非金属材料的主角,其中广泛应用于光导纤维的材料是.
-
(3) 向浑浊的水中加入明矾KAl(SO4)2•12H2O后,水可得到净化.写出明矾在水中的电离方程式,往明矾溶液中逐滴加入Ba(OH)2溶液直至Al3+恰好沉淀完全,发生反应的离子方程式为.
-
(4) 饮用水中的NO3-对人类健康产生危害,为了降低饮用水中NO3-的浓度,可以在碱性条件下用铝粉将NO3-还原为N2 , 其化学方程式为:
10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.
请回答下列问题:
①在化学方程式上用单线桥标出该反应中电子转移的方向和数目:
②上述反应中若生成标况下3.36LN2 , 则转移的电子数目为.
某同学欲检验抗酸药中是否含有Al(OH)3 , 操作如下:取药剂3~4片研碎,向样品中加入过量的盐酸,过滤,得澄清溶液,向澄清溶液中滴加NaOH溶液,观察到有白色沉淀,继续加过量NaOH溶液,白色沉淀又溶解。你能得出该抗酸药中是否含有Al(OH)3?(填含或不含),请写出有关反应的化学方程式:
①
②
③
下图是工业上铝土矿(含有Al2O3和Fe2O3等)冶炼铝的工艺流程图:
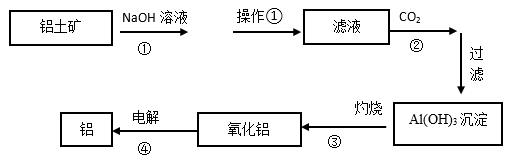
-
(1) 操作①的名称是:。操作①剩余的矿渣主要成分为:(填化学式)。
-
(2) 图中①为了提高NaOH和铝土矿的反应速率可采取哪些措施(写两条)。
-
(3) 图中①的离子方程式;图中③、④的化学反应方程式。
-
(4) 洗涤Al(OH)3沉淀的具体操作是: 。
有一镁、铝合金,用适量稀硫酸恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠的体积关系如图所示,则原合金中镁、铝物质的量比为( )
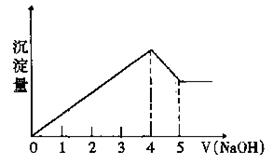
A . 2∶1
B . 4∶1
C . 1∶1
D . 1∶2
含Na2CO3、NaAlO2的混合溶液中逐滴加入150 mL 1mol·L−1HCl溶液,测得溶液中的某几种离子物质的量的变化如图所示,则下列说法错误的是( )
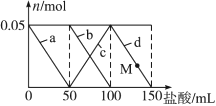
A . a曲线表示的离子方程式为:AlO2-+H++H2O=Al(OH)3↓
B . b和c曲线表示的离子反应是相同的
C . M点时,溶液中沉淀的质量为3.9g
D . 原混合溶液中的CO32-与AlO2-的物质的量之比为1∶2
下列操作中最终可以得到氢氧化铝的是( )
A . 氧化铝与水混合加热
B . 金属铝与水反应
C . 过量的烧碱溶液加入到氯化铝溶液中
D . 过量的氨气通入到氯化铝溶液中
从铝土矿(主要成分为Al2O3 , 还有少量杂质)中提取铝的工艺流程及步骤如下:
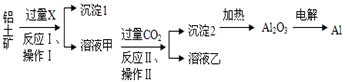
试回答下列问题:
-
(1) 试剂X为;
-
(2) 写出试剂X溶解Al2O3的化学方程式
-
(3) 操作Ⅰ、操作Ⅱ均为(填操作名称);
-
(4) 金属铝与氧化铁混合在高温下,会发生剧烈的反应,该反应的化学方程式为;
-
(5) 反应Ⅱ的离子方程式为;
-
(6) 电解熔融氧化铝制取金属铝,若有0.6 mol电子发生转移,理论上能得到金属铝的质量是g。
将1.0 mol/L盐酸逐滴滴入到100 mL含有NaOH、NaAlO2和Na2CO3的混合溶液中,反应过程如图所示。下列有关说法错误的是( )
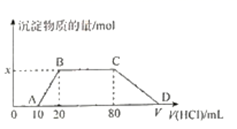
A . 混合液中NaOH的物质的量浓度为0.1 mol/L
B . x=0.01
C . BC段的反应过程离子方程式为:CO 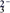 +H+ =HCO
+H+ =HCO 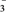 D . V=110
D . V=110
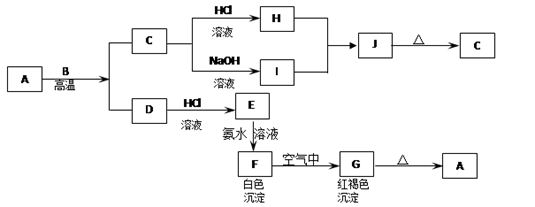
已知A是一种红棕色金属氧化物,B、D是常见的金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解。
-
(1) 写出下列物质的化学名称:A:I:J:G:
-
(2) 写出C→I的离子方程式:。
-
(3) 写出F→G实验现象:。
-
(4) 将一定量A和C混合物溶于100mL稀硫酸中,向反应后的溶液中缓慢加入NaOH溶液,加入NaOH溶液的体积与生成沉淀的质量关系如图所示,试回答:
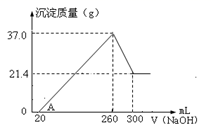
①混合物中含A的质量为;
②所用硫酸溶液物质的量浓度为。
既能与稀盐酸反应,又能与NaOH溶液反应的化合物是:( )
①NaHCO3 ②Al2O3 ③Al(OH)3 ④Al
A . 仅①②③
B . 仅①④
C . 仅②③④
D . ①②③④
甲、乙、丙、丁分别是Al2(SO4)3、FeCl3、NaOH、BaCl2四种物质中的一种。若将丁溶液滴入乙溶液中,发现有白色沉淀生成,继续滴加则沉淀消失,丁溶液滴入甲溶液时,无明显现象发生。据此可推断丙物质是( )
A . Al2(SO4)3
B . NaOH
C . BaCl2
D . FeCl3
下列两种方案制备氢氧化铝:
Ⅰ:2.7 g Al  X溶液
X溶液  氢氧化铝
氢氧化铝
Ⅱ:2.7 g Al  Y溶液
Y溶液  氢氧化铝
氢氧化铝
已知所用的稀盐酸和氢氧化钠溶液均为3 mol·L-1 , 如图是向X溶液与Y溶液中分别加入氢氧化钠溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系,下列说法正确的是( )
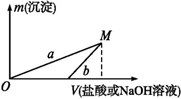
A . a曲线表示的是向Y溶液中加入稀盐酸
B . 方案Ⅱ比方案Ⅰ生成更多的气体
C . 在M点时,两方案所得溶液中溶质的物质的量浓度相同
D . M点以后,a、b两条曲线重合为一条
化学与人类生活密切相关。关于下列物质的使用不合理的是( )
A . 二氧化硫常用于食品增白
B . 碳酸氢钠常用于焙制糕点
C . 醋酸常用于除去水壶内的水垢
D . 氢氧化铝常用于治疗胃酸过多
最近更新
- 在a、b、c、d条件下,测得某植物种子萌发时CO2和O2体积变化的相对值如右表。若底物是葡萄糖,则下列叙述中正确的是(
- 竖直上抛一球,球又落回原处,已知空气阻力的大小正比于球的速度。 A.上升过程中克服重力做的功等于下降过程中重力做的功 B
- 下列四组蛋白质中,可以在人体同一个细胞中产生的是 A.胰高血糖素和胰蛋白酶 B.抗体和干扰素 C.溶菌酶和
- 某8种食品所含的热量值分别为:120,134,120,119,126,120,118,124,则这组数据的众数为
- 家庭电路中,通常用电能表测量的物理量是 A.电阻 B.电能
- 如图所示,质量为M的大圆环,用轻绳悬挂于天花板上,两个质量均为m的小环同时从等高处由静止滑下,当两小圆环滑至与圆心等高时
- 阅读下文,完成第1-5题。 公民是个普世的概念 (1)一个人,为什么要做公民?因为他或她,不能当臣民,也不能做“顺民”。
- It was easier to move about the fringe of the crowd. A. at
- 下列句子中加点的词语使用正确的一项是( ) A. 终于雨过天晴了!我们站在山崖边尽情欣赏着高山流水,心中有一种说不
- 2015年6月5日,上海交通大学机械与动力工程学院的一位硕士研究生在导师指导下,经过反复试验研究,成功利用人类的大脑意念
- 某人是双眼皮,其基因组成为Aa,那么他的父母的基因不可能是 A.AA与Aa B.Aa与Aa C.
- ⑴计算 ⑵化简,并计算当时代数式的值.
- The wild flowers looked like a soft orange blanket______
- 下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是① 过滤 ② 蒸发 ③ 溶解 ④ 向容
- 列宁说:“我们在夺取政权的时候便知道,不存在将资本主义制度具体改造成社会主义制度的现存方法。……我不知道哪位社会主义者处
- 我国家用照明电路的电压为 (1) 伏,各用电器之间是 (2) 连接的(选填“串联”或“并联”)。家庭每月的耗电量用
- 上等米每千克售价为x元,次等米每千克售价为y元,取上等米a千克和次等米b千克,混合后的大米每千克售价为( )A
- 10.17世纪40年代,伴随着明王朝的灭亡,清王朝建立起在全中国的统治。而同一时期的英国,也经历了一场不同含义的“革命”
- 下列关于哺乳动物受精和发育的叙述正确的是() A.雌性动物排卵后遇精子即完成受精 B.胚胎发育至囊胚时已经开始了细胞分化
- 如果电信企业没有推出这套手机媒体服务,就不会有人们对这套媒体的强烈向往,更不会产生强烈的消费欲望。这主要说明 A.消费反



