焰色反应 知识点题库
甲、乙、丙、丁、戊是中学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去).下列说法不正确的是( )
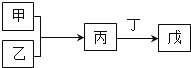
-
(1) 利用焰色反应的原理既可制作五彩缤纷的节日烟花,亦可定性鉴别某些金属盐。灼烧立德粉样品时,钡的焰色为__________(填标号)。A . 黄色 B . 红色 C . 紫色 D . 绿色
-
(2) 以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:
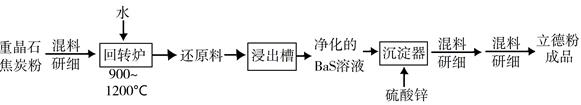
①在回转窑中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为。回转窑尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为。
②在潮湿空气中长期放置的“还原料”,会逸出臭鸡蛋气味的气体,且水溶性变差。其原因是“还原料”表面生成了难溶于水的(填化学式)。
③沉淀器中反应的离子方程式为。
-
(3) 成品中S2−的含量可以用“碘量法”测得。称取m g样品,置于碘量瓶中,移取25.00 mL 0.1000 mol·L−1的I2−KI溶液于其中,并加入乙酸溶液,密闭,置暗处反应5 min,有单质硫析出。以淀粉溶液为指示剂,过量的I2用0.1000 mol·L−1Na2S2O3溶液滴定,反应式为I2+2
 =2I−+
=2I−+  。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为,样品中S2−的含量为(写出表达式)。
。测定时消耗Na2S2O3溶液体积V mL。终点颜色变化为,样品中S2−的含量为(写出表达式)。
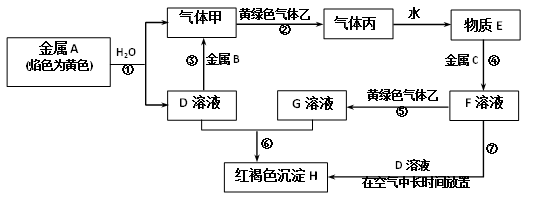
请根据以上信息完成下列各题:
-
(1) 写出下列物质的化学式:B、丙。
-
(2) 写出黄绿色气体乙的一种用途,反应过程⑦可能观察到的实验现象是。
-
(3) 写出反应①的化学方程式,并用单线桥法标出电子转移的方向和数目:。
-
(4) 反应③中的氧化剂是(写化学式,下同),反应④中的还原剂是。
-
(5) 写出反应⑤的离子方程式。
|
Ⅰ |
Ⅱ |
Ⅲ |
Ⅳ |
Ⅴ |
Ⅵ |
Ⅶ |
0 |
|
|
1 |
① |
② |
||||||
|
2 |
③ |
④ |
⑤ |
⑥ |
||||
|
3 |
⑦ |
⑧ |
⑨ |
⑩ |
-
(1) 能显+1价,还能显-1价的元素是(填元素符号):②的分子式是
-
(2) ⑥与⑦按原子个数比1:1形成化合物甲,其电子式为,向甲中滴加足量水时发生反应的化学方程式是
-
(3) ⑦、⑧、⑨三种元素最高价氧化物对应的水化物,碱性由强到弱的顺序排列为(填化学式);⑩的最高价氧化物对应的水化物的化学式为
-
(4) ①、⑤、⑥三种元素形成的一种常见盐的化学式为,其中含有的化学键为
-
(5) 高温灼烧由⑦与⑩形成的化合物时,火焰呈色。⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为
-
(6) 元素⑨的单质和⑦的最高价氧化物的水化物之间发生反应的离子方程式为
| 实验目的 | 实验操作 | |
| A | 焰色试验后为了除去铂丝上杂质 | 将铂丝用盐酸洗净后,在酒精灯外焰上灼烧至与原来的火焰颜色相同 |
| B | 除去Na2CO3固体中的NaHCO3 | 将固体加热至恒重 |
| C | 探究维生素C的还原性 | 向盛有2mL黄色氯化铁(FeCl3)溶液的试管中滴加浓的维生素C溶液,观察颜色变化 |
| D | 制备Fe(OH)3胶体 | 将饱和FeCl3溶液滴加到NaOH浓溶液中 |
 溶液中滴加少量稀盐酸,没有气泡或只有极少量气泡出现
D . 向
溶液中滴加少量稀盐酸,没有气泡或只有极少量气泡出现
D . 向  溶液中滴加足量的
溶液中滴加足量的 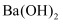 溶液,反应的离子方程式为:
溶液,反应的离子方程式为: 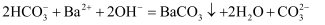
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 用铁丝蘸取某种粉末做焰色试验 | 火焰呈黄色 | 证明含有钠单质 |
| B | 将饱和氯化铁溶液滴入沸水中 | 产生某种红褐色液体 | 该红褐色液体为胶体 |
| C | 用红色激光笔照射雾 | 看到一条光亮的“通路” | 雾能产生丁达尔效应 |
| D | 加热碳酸氢钠溶液 | 产生能使澄清石灰水变浑浊的气体 | 碳酸氢钠热稳定性较差 |
选项 | 实验操作 | 实验现象 | 实验结论 |
| 向未知液中滴加氯水,再滴加 | 溶液呈红色 | 未知液中一定含有 |
| 取无色溶液做焰色试验 | 火焰为黄色 | 无色溶液中有 |
| 某少量无色无味气体通入澄清石灰水中 | 澄清石灰水变浑浊 | 该气体一定是 |
| 将银白色的金属钠放置在空气中 | 钠表面很快变暗 | 金属钠具有强氧化性 |
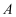 B .
B . 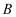 C .
C . 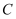 D .
D . 
已知:FeO是一种黑色粉末,不稳定,在空气中加热,可被氧化成Fe3O4 , 隔绝空气加热会歧化为Fe和Fe3O4。
-
(1) Ⅰ.FeCl3溶液的灼烧。
实验ⅰ:将一只白粉笔浸泡在FeCl3溶液中,用坩埚钳夹持粉笔于酒精灯上灼烧,很快观察到粉笔表面颜色的变化:黄色→红褐色→铁锈色→黑色。
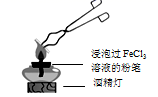
配制FeCl3溶液时,先将氯化铁晶体溶于较浓的盐酸中,再加水稀释到所需要的浓度。结合化学用语解释将氯化铁晶体溶于盐酸的目的。
-
(2) “黄色→红褐色→铁锈色→黑色”颜色变化中的“铁锈色”物质是。(填化学式)
-
(3) 针对“黑色”物质,小组成员提出猜想。
猜想1:酒精灼烧粉笔的产物;
猜想2:酒精还原“铁锈色”物质得到的产物。
通过实验排除了猜想①,实验操作和现象是。
-
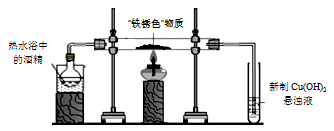
(4) Ⅱ.探究“黑色”物质的成分。
实验ⅱ:先用酒精蒸气排尽装置中的空气,再在“铁锈色”物质处加热,充分反应至“铁锈色”物质完全变成“黑色”物质。取下装有新制Cu(OH)2的试管,加热,有砖红色沉淀生成。
实验ⅲ:在“黑色”物质中加入热的硫酸,“黑色”物质溶解,无气泡产生。
甲同学根据实验ⅱ和ⅲ的现象,判断“黑色”物质中含有二价铁,其理由是。
-
(5) 乙同学用实验ⅲ中所得溶液进行实验iv,证实了甲的判断,实验iv的离子反应方程式为。
-
(6) 丙同学发现“黑色”物质完全被磁铁吸引,推测“黑色”物质是Fe3O4 , 写出“铁锈色”物质变成Fe3O4的化学方程式。
-
(7) 丁同学为证明“黑色”物质是Fe3O4 , 设计实验方案并预测:取实验ⅲ中少量清液滴入足量的Na2S溶液,认为得到物质的量之比为3∶1的FeS和S沉淀,即可证明。你认为是否合理,并说明理由。
 固体分别与足量等浓度的盐酸反应,前者消耗的盐酸多
固体分别与足量等浓度的盐酸反应,前者消耗的盐酸多
 B . 向无色溶液中滴加氯水,再加CCl4振荡、静置、溶液分层,下层呈紫红色,该溶液中一定含有I-
C . 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水中,石灰水变浑浊,该溶液中一定含有
B . 向无色溶液中滴加氯水,再加CCl4振荡、静置、溶液分层,下层呈紫红色,该溶液中一定含有I-
C . 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水中,石灰水变浑浊,该溶液中一定含有 D . 取洁净的铂丝在酒精灯火焰上灼烧至无色,再蘸取少量溶液置于火焰上灼烧,火焰呈黄色,该溶液一定不含K+
D . 取洁净的铂丝在酒精灯火焰上灼烧至无色,再蘸取少量溶液置于火焰上灼烧,火焰呈黄色,该溶液一定不含K+
- 在植物细胞中,吲哚乙酸主要由色氨酸经一系列酶催化生成。下列相关叙述正确的是() A.吲哚乙酸可在胚芽鞘中大量合成 B.色
- 如图6所示,教室里的天花板下面装有多档位吊扇,当吊扇正常工作时,关于吊扇对天花板的拉力与其重力大小的判断正确的是(
- 亚当・斯密说:“发现美洲和经过好望角至东印度群岛的航道,是人类历史上所记载的最伟大、最重要的事件。”文中所谓“发现美洲和
- 中国许多具有历史文化特色的城镇、街区、古老建筑,其实是阴暗、潮湿的地方,老鼠蟑螂满地跑,影响居民的生活。许多人认为,推动
- 许多动物都有学习的能力,下列动物中学习能力最强的是: A.蚯蚓; B.鱼; C.乌龟; D.黑猩猩
- 第一节:完形填空(共10小题;每小题2分,满分20分) 阅读下面短文,掌握其大意,然后从21~30各题所给的四个选项(A
- 已知在一定温度下,一定体积的密闭容器里有如下平衡:H2(g)+I2(g) 2IH(g), H2和I2的起始浓度均为0.1
- 有关地域文化与人口的说法正确的是 A、地域文化是指一个地区的民族文化 B、地域文化对一地区的人口发展起决定作用 C、地域
- 探测器绕月球做匀速圆周运动,变轨后在周期较小的轨道上仍做匀速圆周运动,则变轨后与变轨前相比 A.轨道半径变小
- 阅读下面的文字,完成下题。 苦梅 马卫 苦梅又叫乌梅,个小,肉少,汁酸。如果不是没有吃的,孩子们是不会去吃苦梅的。一个姑
- — Spell it,please. — OK, A. It’s arule
- 右图为极地俯视图,此时全球为同一个日期,曲线ABC上的太阳高度为0°,回答8-9题。 8.此刻太阳直射点的地理坐标为 A
- 下列关于植物与环境关系的叙述,最合理的是A.影响植物生活的环境因素是指阳光、温度、空气和水分等非生物因素B.植物对于环境
- 一个电子只在电场力作用下从a点运动到b点的轨迹如图中虚线所示,图中一组平行实线可能是电场线也可能是等势面,下列说法中正确
- 民主进程是人类社会进步的重要标志。2010年2月27日,总理与网友交流时说:“我们确实需要一些仰望星空的人,
- (二)古代诗歌阅读(11分) 阅读下面这首宋诗,完成8~9题。 雪后到乾明寺,遂宿【注】 苏轼 门外山光马亦惊,阶前屐齿
- 根据短文的内容,从短文后的选项中选出能填入空白处的最佳选项,选项中有两项为多余选项。 Children start ou
- 1869年,《教会新报》的一篇文章写道:“外国生产皆归男医接生,虽经此例,似不成规矩。……男归男医,女归女医,岂不至善也
- 如图,AD是△ABC的角平分线,DE、DF分别是△ABD和△ACD的高,求证:AD垂直平分EF.(7分)
- 原核细胞和真核细胞最明显的区别在于 ( )
 溶液
溶液
 , 无
, 无




