金属的通性 知识点题库
下列描述的一定是金属元素的是()
A . 易失去电子的物质
B . 原子核内有11个质子的元素
C . 能与酸反应的物质
D . 原子的最外层只有一个电子的元素
金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的说法不正确的是( )
A . 合金的性质与其成分金属的性质不完全相同
B . 工业上金属Mg、Al都是用电解熔融的氯化物制得的
C . 金属冶炼的本质是金属阳离子得到电子变成金属原子
D . 越活泼的金属越难冶炼,冶炼方法与其活泼性有关
下列关于金属元素特征的叙述,正确的是( )
A . 金属元素的原子只有还原性,离子只有氧化性
B . 金属元素在化合物中一定显正价
C . 金属单质都可以和酸反应置换出氢气
D . 金属元素的单质在常温下均为固体
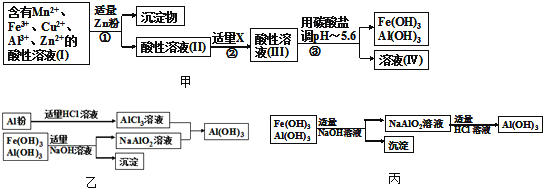
某化工厂以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2 .
-
(1) 在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式: MnO2+ FeS+ H2SO4= MnSO4+ Fe2(SO4)3+ S+ H2O
-
(2) 将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按如图甲的工业流程进行操作处理得溶液(IV),电解溶液(IV)即得MnO2和Zn.
a、操作①中加Zn粉后发生反应的离子方程式为。
b、操作②中加入适量X的作用是什么 ;X的首选物的化学式是: 。
c、操作③中所加碳酸盐的化学式是 。
-
(3) 为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3 , 工厂设计了如图乙的有关流程图。
a、AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为 。若总共得到n molAl(OH)3 , 则消耗的NaOH和HCl的理论量(mol)分别为 、 。
b、若使用如图丙流程回收处理,请比较两个流程消耗酸碱的用量? 。
下列叙述中,属于金属化学性质的是( )
A . 铝在空气中易与氧气反应生成致密的氧化膜
B . 纯铁是银白色固体
C . 铜容易传热、导电
D . 钨有很高的熔点
不属于金属通性的是( )
A . 延展性
B . 高熔点
C . 导热性
D . 导电性
一定量的锌粉和3mol/L的过量盐酸反应,当向其中加入少量的下列物质时能加快化学反应速率但不影响产生H2总量的是( )
①铁粉 ②银粉 ③石墨粉 ④稀硝酸 ⑤CaCO3 ⑥浓盐酸
A . ②④⑥
B . ①②⑤⑥
C . ②③⑥
D . ②③④⑥
将一定量铁粉和铜粉的混合物加入由稀H2SO4和稀HNO3组成的混合溶液中,充分反应后金属粉末有剩余,下列有关推断正确的是( )
A . 反应过程中不可能产生H2
B . 剩余的金属粉末中一定有铜
C . 往反应后的溶液中加入KSCN溶液会变红色
D . 往反应后的溶液中加入足量的稀H2SO4 , 则金属粉末的质量一定会减少
与金属的物理性质无关的是()
A . 良好的导电性
B . 反应中易失去电子
C . 延展性
D . 导热性
铁能压成薄片,这是因为()
A . 熔点低
B . 延展性大
C . 硬度小
D . 密度小
下列有关用途的叙述错误的是()
A . 常温下可用铁容器储运浓硫酸
B . 焰色反应可用于检验某些金属元素的存在
C . 氨是制造硝酸的原料
D . 铝制餐具可以长时间盛放咸的食物
下列金属用途和有关性质的对应关系错误的是( )
| 金属用途 | 金属的有关性质 | |
| A | 金可以制成比纸还薄的金箔 | 延展性 |
| B | 生活用铁锅 | 导热性 |
| C | 用铁回收照相定影废液中的银 | 氧化性 |
| D | 用铜制作印刷电路 | 导电性 |
A . A
B . B
C . C
D . D
金属Ti(钛)是一种具有许多优良性能的较为昂贵的金属,钛和钛合金被认为是21世纪的重要金属材料。某化学兴趣小组用实验探究Ti、Mg、Cu的活泼性顺序。他们在相同温度下,取大小相同的三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象如下:
| 金属[ | Ti | Mg | Cu |
| 金属表面现象 | 放出气泡速度缓慢 | 放出气泡速度快 | 无变化 |
下列有关三种金属的说法正确的是( )
A . 三种金属的活泼性由强到弱的顺序是Ti、Mg、Cu
B . 若钛粉中混有Mg,提纯Ti时可用稀盐酸除去Mg
C . 用Ti从CuSO4溶液中置换出Cu是工业制取Cu的很好途径
D . Cu和稀盐酸不发生化学反应
下列有关金属及其合金的说法正确的是( )
A . 用焰色反应鉴别NaCl、KCl和Na2SO4
B . 合金与各组分金属相比一般具有更低的熔点
C . 生铁、普通钢和不锈钢中的碳含量依次增加
D . Fe2O3是磁铁矿的主要成分,属于碱性氧化物
金属材料在日常生活、生产中有着广泛的运用,下列关于金属的说法错误的是( )
A . 工业上金属Mg、Al都是用电解熔融的氯化物制得的
B . 合金的性质与其成分金属的性质不完全相同
C . 金属冶炼的本质是金属阳离子得到电子变成金属原子
D . 越活泼的金属越难冶炼
关于金属元素的特征,下列叙述正确的是( )
①金属元素的原子只有还原性,离子只有氧化性②金属元素在化合物中一般显正价 ③金属性越强的元素相应的低价离子氧化性越弱④价电子越多的金属原子的金属性越强
A . ①②
B . ②③
C . ①④
D . ③④
下列有关金属及其合金的说法中,错误的是( )
A . 硬铝、青铜、不锈钢都属于合金,合金的许多性能优于纯金属,而熔点低于成分金属
B . 合金中用量最大的是钢,其含碳量越大,韧性越好
C . 日用铝制品表面覆盖着致密的氧化膜,对内部金属起保护作用
D . 纳米铜的水溶液具有丁达尔效应
下列说法错误的是( )
A . 常温下,铁在浓硫酸中发生钝化,可用铁槽车贮运浓硫酸
B . 金属铜具有良好的导电性,可用来制作导线
C . MgO的熔点很高,可用做耐高温材料
D . SO2具有漂白性,可用于木耳食品的漂白
根据所学知识回答下列问题:
-
(1) 常温下镁、铝都具有较强的抗腐蚀性,主要原因是。
-
(2) 标准状况下,
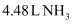 与同条件下
与同条件下 含有相同的氢原子数。
含有相同的氢原子数。
-
(3) 标准状况下,
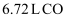 的质量为g。
的质量为g。
-
(4) 实验室用
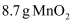 与100mL足量的浓盐酸制取氯气,发生反应:
与100mL足量的浓盐酸制取氯气,发生反应: (浓)
(浓)
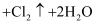 。当
。当 完全反应时,参加反应的HCl的物质的量为
完全反应时,参加反应的HCl的物质的量为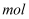 , 假设反应后溶液的体积仍为100mL,则反应后的溶液中生成的
, 假设反应后溶液的体积仍为100mL,则反应后的溶液中生成的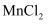 的物质的量浓度为mol/L。
的物质的量浓度为mol/L。
-
(5) 实验室需配制
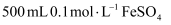 溶液,实际应称量绿矾(
溶液,实际应称量绿矾( )的质量为
)的质量为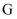 。配制时,其正确的操作顺序是(填标号,每个标号只能用一次)。
。配制时,其正确的操作顺序是(填标号,每个标号只能用一次)。①用
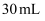 水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,摇匀
水洗涤烧杯内壁和玻璃棒2~3次,洗涤液均注入容量瓶,摇匀②将准确称量的绿矾倒入烧杯中,再加适量水溶解
③将已冷却的溶液沿玻璃棒注入容量瓶中
④将容量瓶盖紧,反复上下颠倒,摇匀
⑤改用胶头滴管加水,使溶液凹面恰好与刻度线相切
⑥继续往容量瓶内小心加水,直到液面接近刻度线下
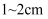 处
处
下列有关金属的用途与相应性质不对应的是( )
A . 用金做饰物是因为金的化学性质稳定、不褪色
B . 用钨做白炽灯灯丝是因为其熔点高、导电性好
C . 用镁合金做汽车部件是因为镁的密度小,化学性质活泼
D . 用铝做包装用的铝箔是因为其延展性好,表面有钝化膜
最近更新
- 现有下列物质:①氧气;②可口可乐;③冰水共存物;④水银;⑤澄清石灰水;⑥高锰酸钾。用序号填空:⑴属于混合物的有
- 下列实验能获得成功的是……( ) ①用醋酸钠晶体和碱石灰共热制取甲烷;②将甲烷气体通入溴水中制取溴甲烷;③用酒精灯加
- 下图是三个神经元及其之间的连接示意图。如果在E部位进行一次电刺激,不会发生电位变化的就位是
- 下列关于35 17Cl和37 17Cl的说法,错误的是 A.35 17Cl和37 17Cl中子数相差2 B.35 17C
- 下列粒子中,带负电的是 A. 电子 B. 中子 C. 质子 D.
- --- What did he say? ---- He said he ________ the sentence
- 阅读下列材料材料一 作为一个国家,我们拒绝了任何彻底的革命计划。为了永远纠正我们经济制度中的严重缺点,我们依靠的是旧
- A、B、C三个物体通过细线和光滑的滑轮相连,处于静止状态,如图所示,C是一箱砂子,砂子和箱的重力都等于G,动滑轮的质量不
- 点P是圆(x+1)2+(y﹣2)2=2上任一点,则点P到直线x﹣y﹣1=0距离的最大值为() A. B. C. D.
- (2011四川广安,4,3分)从《中华人民共和国2011年国民经济和社会发展统计报告》中获悉,去年我国国内生产总值达39
- 航天员若在轨道舱内长时间停留,需要每天进行锻炼,在轨道舱内,下列运动最能有效锻炼肌肉的力量的是A.上下举哑铃
- 对于一切实数x,令[x]为不大于x的最大整数,则函数f(x)=[x]称为高斯函数或取整函数. 计算f(-0.3)+f(1
- 科学家温特做了如下实验:把切下的燕麦尖端放在琼脂块上,几小时后,移去胚芽鞘尖端,将琼脂块切成小块。再将经处理过的琼脂块
- 报道,国外有人利用水的沸点与压强的关系,设计了一种“真空洗衣 机”。它不需要洗衣粉就能使常温的
- 一质量为m的物体,置于水平长木板上,物体与木板间的动摩擦因数为μ.现将长木板的一端缓慢抬起,要使物体始终保持静止,木板与
- 植物根尖中吸收水分和无机盐的主要部位以及具有细胞分裂功能的部位分别是() A.成熟区、分生区 B.分生区、成熟区 C.
- 1919年6月,中国某城市有六七万工人参加罢工。罢工工人说:“我们当前所进行的运动,乃是世界史上一件最为惊人的运动。这是
- 标准状况下,将2.24LNH3通入1L 0.1mol/L的醋酸溶液中,欲确定所得溶液中NH4+、CH3COO-、H+和
- 读右图,比较三个阶段工业发展状况,你能得到的正确信息是①科技是推动工业增长的根本原因 ②生产组织形式变革是工业发展的重要
- One will feel happy when others flatter( 奉承) him in his face



