除杂 知识点题库
pH | 6.5~8.5 |
Ca2+、Mg2+总浓度 | <0.0045 mol·L-1 |
细菌总数 | <100个·mL-1 |
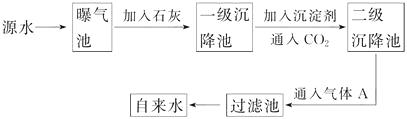
以下是源水处理成自来水的工艺流程示意图:
-
(1) 源水中含Ca2+、Mg2+、HCO、Cl-等,加入石灰后有Ca(OH)2生成,进而发生若干复分解反应,写出其中一个离子方程式?
-
(2) 凝聚剂除去悬浮固体颗粒的过程(填写编号)。
①只是物理过程 ②只是化学过程 ③是物理和化学过程
FeSO4·7H2O是常用的凝聚剂,它在水中最终生成沉淀。
-
(3) 通入CO2的目的是。
-
(4) 气体A的作用是,这种作用是基于气体A和水反应的产物具有性。
-
(5) 下列物质中,可以作为气体A的代用品(填写编号)。
①Ca(ClO)2 ②NH3(液) ③K2FeO4 ④SO2
-
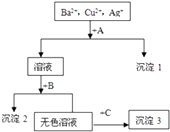
(1) 沉淀的化学式:
沉淀1
沉淀2
沉淀3
-
(2) 写出混合液+A的离子方程式
写出溶液+B的离子方程式.
-
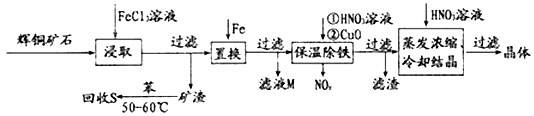
(1) “浸取”时,为了提高浸取速率可采取的措施有(任写一点)。写出“浸取”过程中Cu2S溶解时发生反应的离子方程式:。
-
(2) “保温除铁”过程中,加入CuO的目的是;“蒸发浓缩、冷却结晶”过程中,加入HNO3调节溶液的pH,其理由是。
-
(3) 气体NOx与氧气混合后通入水中能生成流程中可循环利用的一种物质,该反应的化学方程式为。向“滤液M”中加入(或通入) (填字母),可得到另一种可循环利用的物质。
a.铁
b.氯气
c.高锰酸钾
-
(4) “回收S”过程中温度控制在50 ~60℃之间,不宜过高或过低的原因是。
|
实验 |
试剂 |
现象 |
|
|
滴管 |
试管 |
||
|
|
0.8mol/LFeSO4溶液(pH=4.5) |
1mol/LNa2CO3溶液(pH=11.9) |
实验Ⅰ:立即产生灰绿色沉淀,后出现明显的红褐色 |
|
0.8mol/LFeSO4溶液(pH=4.5) |
1mol/LNaHCO3溶液(pH=8.6) |
实验Ⅱ: 产生白色沉淀及少量无色气泡,2min,后出现明显的灰绿色 |
|
|
0.8mol/L(NH4)2Fe(SO4)2溶液(pH=4.0) |
1mol/LNaHCO3溶液(pH=8.6) |
实验Ⅲ: 产生白色沉淀及无色气泡,较长时间保持白色 |
|
-
(1) 实验I中产生HCO3-和红褐色沉淀的离子方程式为
-
(2) 实验Ⅱ中产生FeCO3的离子方程式为
-
(3) 为了探究实验Ⅲ中NH4+所起的作用,甲同学设计了实验Ⅳ进行探究:
操作
现象
实验Ⅳ
向0.8mol/LFeSO4溶液中加入,再加入一定量Na2SO4固体配制成混合溶液(已知Na+对实验无影响,忽略混合后溶液体积变化)。再取该溶液一滴管,与2mL1mol/LNaHCO3溶液混合
与实验Ⅲ现象相同
实验Ⅳ中加入Na2SO4固体的目的是
对比实验Ⅱ、Ⅲ、Ⅳ,甲同学得出结论:NH4+水解产生H+ , 降低溶液pH,减少了副产物Fe(OH)2的产生。
乙同学认为该实验方案不够严谨,应补充的对比实验操作是.再取该溶液一滴管2mL 1mol/L NaHCO3溶液混合。
-
(4) 小组同学进一步讨论认为,定性实验现象并不能直接证明实验Ⅲ中FeCO3的纯度最高。需要利用如图所示的装置进行定量测定。
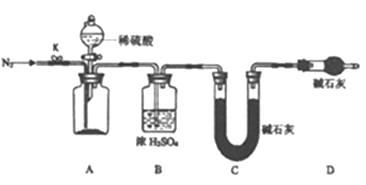
分别将实验Ⅰ、Ⅱ、Ⅲ中的沉淀进行过滤、洗涤、干燥后称量,然后转移至A处的广口瓶中。反应完成后通入N2的作用是。为测定FeCO3的纯度,除样品总质量外,还需测定的物理量是
-
(5) 实验反思:经测定,实验Ⅲ中的FeCO3纯度高于实验Ⅰ和实验Ⅱ。通过以上实验分析。制备FeCO3实验成功的关键因素是.
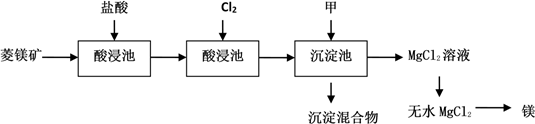
请回答有关问题:
-
(1) 菱镁矿进入酸浸池前需要粉碎,目的是 。
-
(2) 氧化池通入Cl2的目的是氧化 (填化学式),工业上不选用硝酸做氧化剂的原因是和。
-
(3) 物质甲可以是_____________A . MgO B . Mg(OH)2 C . NaOH溶液 D . 稀氨水
-
(4) 由MgCl2溶液制取无水MgCl2的操作方法 。
-
(5) 当Fe3+完全沉淀时,求最小pH。已知:氢氧化铁ksp=1.0×10-38 , 离子浓度小于1×10-5 mol/L认为沉淀完全
-
(1) 过氧化钠可用在呼吸面具里作为氧气的来源,其反应的化学方程式为:;
-
(2) 氢氧化铝可用作治疗胃酸过多的药剂,其原理用离子方程式表示为:;
-
(3) 实验室要除去NaHCO3溶液中的少量Na2CO3 , 其离子方程式为:;
-
(4) 除去FeCl2溶液中的少量FeCl3 , 其离子方程式为:。
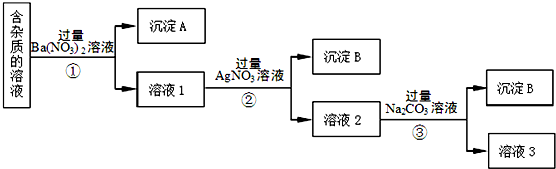
-
(1) 沉淀A的主要成分是、(填化学式)。
-
(2) ③中加入过量的Na2CO3溶液的目的是。
-
(3) 溶液3经过处理可以得到NaNO3固体,溶液3中肯定含有的杂质是,为了除去杂质,可向溶液3中加入适量的。
|
气体(杂质) |
方法 |
|
|
A |
SO2(H2S) |
通过酸性高锰酸钾溶液 |
|
B |
Cl2(HCl) |
通过饱和的食盐水 |
|
C |
N2(O2) |
通过灼热的铜丝网 |
|
D |
NO(NO2) |
通过氢氧化钠溶液 |
-
(1) 为了检验和除去下表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中选出适当的除杂试剂,将所选的答案用字母填入相应的空格内。
物质
检验试剂
除杂试剂
(Ⅰ)甲烷(乙烯)
(Ⅱ)酒精(水)
①检验试剂:A.无水硫酸铜 B.酸性高锰酸钾溶液 C.水 D.氢氧化钠溶液
②除杂试剂:a.无水硫酸铜 b.新制的生石灰 c.乙酸 d.溴水
除杂时,乙烯发生反应的化学方程式为。
-
(2) 如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验。试回答:在右试管中通常加入溶液,实验生成的乙酸乙酯。
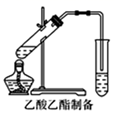
-
(3) 其密度比水,是有特殊香味的液体。请写出左侧试管中的反应方程式。
| A | B | C | D |
| | | | |
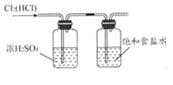
| 向容量瓶中转移液体 | 实验室制备氨气 | 除去甲烷中混有的少量乙烯 | 氯气的净化 |
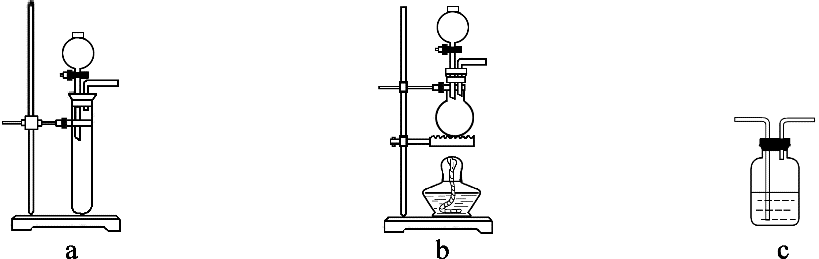
气体 | 制备试剂 | 除杂试剂 | 所选装置 | |
A | SO2 | Cu+浓H2SO4 | 饱和NaHSO3溶液 | b、c |
B | Cl2 | MnO2+浓HCl | 饱和NaCl溶液 | b、c |
C | C2H4 | C2H5OH+浓H2SO4 | KMnO4溶液 | b、c |
D | C2H2 | 电石+饱和NaCl溶液 | CuSO4溶液 | a、c |
-
(1) 补齐下列物质与其用途之间的连线。
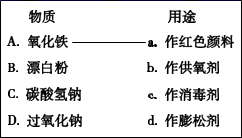
-
(2) 以下物质:①KOH固体②熔融KNO3③盐酸④稀H2SO4⑤NaCl溶液⑥Fe。其中,属于纯净物的是(填“序号”);不能导电的物质是(填“序号”),属于电解质的是(填“序号”)。
-
(3) Na2CO3俗称“纯碱”,属于类(填“酸”、“碱”或“盐”),遇足量稀盐酸产生气泡,该反应的离子方程式为;若Na2CO3粉末中混有少量NaHCO3杂质,除去杂质的方法是 ,涉及的反应的化学方程式为。
选项 | 实验目的 | 实验操作 |
A | 除去溴苯中的少量溴单质 | 向溴苯中加入NaOH溶液,振荡,静置后分液 |
B | 除去苯中少量苯酚 | 向混合物中加入浓溴水,产生白色沉淀后过滤除去沉淀物 |
C | 除去乙烷中的少量乙烯 | 将混合气体通入高锰酸钾溶液中 |
D | 除去苯甲酸中难溶杂质 | 将粗苯甲酸在水中溶解,加热,冷却结晶,过滤 |
- ﹣的相反数是() A.2 B. ﹣2 C.
- 设函数的图象为曲线C,则曲线C与直线的交点个数为 A.0 B.1
- 阅读下面文言小段,完成后面练习。 臧孙行猛政 臧孙行猛政,子贡非之 ,曰:“独不闻子产之相郑乎?推贤举能,抑恶扬善;有大
- 如图所示,BC∥EF,CD⊥BC于点C,CD⊥EF于点D,点A在射线DE上移动,把图形ABCD绕直线EF旋转一周,得到一
- 下列图象能正确地表达可逆反应3A(g)+B(g)2C(g)(△H<0)的是()
- Take the note as a reminder_____ youforget to buy some swee
- 随着智能手机时代的到来,各类电子书被越来越多的年轻人所接受。但也有人认为,对于真正爱书的人来说,读纸质书才能让人享受慢慢
- 成长中的少年,会有一些挥之不去的烦恼。这烦恼来自生活,来自学习,来自与同学的交往……但是,有烦恼并不可怕,关键是要正确对
- 用万用表的电阻档测电阻时,倍率的选取及指针指示如图(指在10与20的正中间),则指针指示的电阻值约为:( )A
- 某同学在做“研究匀变速直线运动”实验时,从打下的若干纸带中选出了如图所示的一条(每两点间还有4个点没有画出来),图中上部
- 下列化学反应的离子方程式正确的是 A.在稀氨水中通入少量SO2: NH3·H2O+SO2=NH+HSO32- B.以石
- There is a 20 minute parking _____ here, so we must get back
- 下列文言加点词解释有错误的一项是( ) (3分) A、非梧桐不止(栖息)
- 如图所示,边长L = 2.5m 、质量m = 0.50kg的正方形金属线框,放在磁感应强度B = 0.80T的匀强磁场
- —When will you return the bookto me? —I’ll give it to you _
- 化学与生产、生活、社会密切相关。下列有关说法中不正确的是( )A.前段时间,我国西南部发生不同程度的旱情,缓解旱情的措
- (09广州市调研)下列关于酶的叙述中,正确的是A. 有酶参与的反应能释放出更多的能量B. 酶的活性随着温度升高而不断升高
- 第三部分 阅读理解(共25小题:第一节每小题2分第二节每小题1分,满分45分) 第一节:阅读下列短文,从每题所给的四个
- 下列各句在文中的意思,翻译有误的一项 A.地势极而南溟深,天柱高而北辰远:地势偏远,南海深邃;天柱高耸,北极星远悬。 B
- 天空有近似等高的浓云层.为了测量云层的高度,在水平地面上与观测者的距离为d=3.0km处进行一次爆炸,观测者听到由空气直