纯碱的制取 知识点题库
1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:①NaCl+NH3+CO2+H2O═NaHCO3+NH4Cl;②2NaHCO3 Na2CO3+H2O+CO2↑;
Na2CO3+H2O+CO2↑;
试回答下列问题:
(1)在反应①的六种物质中,焙制糕点是时常用作发酵粉的是;
(2)胺盐水比食盐水更容易吸收二氧化碳的原因是 .
(3)氯化钠和碳酸钠的溶解度如图2,t2℃时,氯化钠饱和溶液溶质的质量分数碳酸钠饱和溶液溶质的质量分数
(填“大于”“小于”“等于”之一).
(4)生活在盐碱湖附近的人们有一句谚语“夏天晒盐,冬天捞碱”,请结合溶解度曲线,说明这句谚语的原理: .
①NH3+H2O+CO2═NH4HCO3 ,
②NaCl(饱和)+NH4HCO3═NH4Cl+NaHCO3↓,
③2NaHCO3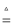 Na2CO3+H2O+CO2↑,
Na2CO3+H2O+CO2↑,
下列说法正确的是( )
我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图),反应原理为NH3+H2O+CO2+NaCl=NH4Cl+NaHCO3(析出),促进了世界制碱技术的发展.下列说法正确的是( )



-
(1) 反应①的化学方程式,反应②的基本反应类型为.
-
(2) 工业上用分离液态空气 的方法制取氮气,属于变化.
-
(3) 操作a的名称是,实验室进行此操作所需的玻璃仪器有烧杯、玻璃棒、.
-
(4) 饱和食盐水中通入氨气的目的是.
【查阅资料】
①生产原理:NaCl(饱和溶液)+NH3+CO2+H2O=NaHCO3(固体)↓+NH4Cl
②主要生产流程如图所示:

③氨气(NH3)是一种有刺激性气味的气体,极易溶于水,其水溶液显碱性.
【理论分析】
-
(1) 依据资料①可知相同条件下,NaHCO3的溶解度NH4Cl的溶解度(填“>”或“<”).
-
(2) NaHCO3受热分解制得纯碱及两种常见的氧化物,该反应的化学方程式是.
【模拟实验】验证侯氏制碱法能获得纯碱
步骤
蘸有稀硫酸
实验装置
实验操作及现象
解释与结论
1

从a管通入NH3 , 一段时间后,从b管通入CO2 , 溶液中有固体析出
(1)蘸有稀硫酸的棉花的作用是
(2)通NH3的a管若伸到液面下,会造成的后果是
2

加热,导管口有气泡,澄清石灰水变浑浊
步骤1析出的固体是碳酸氢钠
3

滴加足量稀盐酸,有气泡产生,固体逐渐消失
步骤2加热后得到的固体是纯碱
【实验反思】同学们认为步骤3的结论存在不足.依据题中信息,设计实验确定步骤2加热后得到的固体成分,其方案是.
-
(1) 在400℃左右,有催化剂存在的条件下,用氨气可将有毒气体NO还原为N2和H2O.试写出该反应的化学方程式.
-
(2) “侯氏制碱法”关键一步的反应原理可表示为:NaCl+H2O+NH3+CO2═NaHCO3+NH4Cl,其生成物NH4Cl的相对分子质量为,NH4Cl中氮元素的质量分数为(精确到0.1%).若上述NH4Cl中氮元素的质量为2.8t,则NH4Cl的质量为 t.(精确到0.1)
-
(3) 在细菌作用下,用氨气处理含甲醇的工业废水,使其变为无毒的N2和CO2 , 从而清除对环境的污染,有关的反应为:6NH3+5CH3OH+12X
 3N2+5CO2+19H2O,上述反应的X处应填入的化学式为.
3N2+5CO2+19H2O,上述反应的X处应填入的化学式为.


回答下列问题:
-
(1) 操作a的名称是.
-
(2) 反应②的化学方程式为.
-
(3) 反应④的化学方程式为;请列举小苏打在生活中的一种常见用途.
-
(4) 向精制饱和食盐水中通入两种气体的顺序是:先通氨气形成饱和氨盐水,然后在加压条件下通入二氧化碳.这样操作的目的是.
-
(5) 仔细观察流程图,其中可循环利用的物质除二氧化碳之外,还有.

-
(1) 写出反应②的化学方程式;
-
(2) 实验室进行操作a所需的仪器有铁架台、烧杯、玻璃棒、;
-
(3) 从物质溶解性的角度分析,操作a(选填“能”或“不能”)将两种物质完全分离.
-
(1) 我国著名化工专家侯德榜先生发明了“侯氏制碱法”为我国民族工业的发展做出了杰出贡献,“NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl“是侯氏制碱法的重要反应之一,下列有关说法错误的是 (填序号).A . 向饱和食盐水中先通入氨气,使溶液呈碱性,更易吸收酸性的CO2气体 B . 反应后,NaHCO3首先结晶析出,过滤即可将其分离出来 C . NaHCO3结晶析出后,剩余溶液中的溶质只有NH4Cl D . NaHCO3结晶析出后,剩余溶液还能继续溶解NaCl固体
-
(2) 海洋是巨大的资源宝库,我们可利用海水为原料制取大量的重要化工产品,例如:海水中存在大量的氯化钠,电解纯净的氯化钠溶液可以制得氢气、氯气和物质A,其反应原理为2NaCl+2H2O
 2A+Cl2↑+H2↑,试推断A的化学式为.
2A+Cl2↑+H2↑,试推断A的化学式为.
-
(3) t1℃时,将a、b两种固体各18g分别加入到盛有100g水的烧杯中,充分搅拌后实验现象如甲图所示,升温到t2℃时,实验现象如乙图所示,a、b两种固体在水中的溶解度曲线如丙图所示.

请根据如图实验现象及溶解度曲线填空:
①从t1℃到t2℃的变化过程中,一直处于饱和状态的是(填“a”或“b”)溶液.
②丙图中,曲线M表示的是(填“a”或“b”)的溶解度曲线.
③若a中混有少量b,可采用的方法提纯a.(填“蒸发结晶”或“降温结晶”).
如图是某厂生产纯碱的工艺流程图:

请完成下列问题:
-
(1) 流程Ⅰ中为了除去杂质,加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是 (填字母序号);A . 加入三种溶液的顺序不能调整 B . 加入三种溶液将粗盐水中的SO42﹣、Mg2+、Ca2+转化为沉淀 C . 按流程Ⅰ所加溶液的顺序除杂,过滤后得到四种沉淀
-
(2) 在流程Ⅰ中,加入BaCl2溶液时发生反应的化学方程式是;
-
(3) 在流程Ⅱ中,如果加入氨气不是为了生产氯化氨,氨气在制碱过程中的作用是;
-
(4) 写出流程Ⅲ中发生反应的化学方程式。
①NH3+H2O+CO2=NH4HCO3 ②NaCl(饱和)+NH4HCO3=NH4Cl+NaHCO3↓
③2NaHCO3  Na2CO3+H2O+CO2↑下列说法正确的是( )
Na2CO3+H2O+CO2↑下列说法正确的是( )
-
(1) 海水晒盐是利用了的方法使食盐晶体析出,得到粗盐。
-
(2) 某制碱工厂以粗盐为原料制纯碱,部分工艺流程如下:

①流程I中为了除去杂质,依次加入过量BaCl2溶液、NaOH溶液和Na2CO3溶液,下列说法正确的是(填字母编号);
A.加入三种溶液的顺序不能调整
B.加入三种溶液可将粗盐水中的SO4、Mg2+、Ca2+转化为沉淀
C.按流程I所加溶液的顺序除杂,过滤后得到四种沉淀
②在流程I中,加入氢氧化钠溶液时发生反应的化学方程式是;
③流程I中Na2CO3溶液的作用是;
④写出流程Ⅲ中发生反应的化学方程式。
-
(3) 将已配制好的100g质量分数为6%的氧化钠溶液变成质量分数为20%的氯化钠溶液,需要再加入NaCl的质量是g。

-
(1) 反应①的化学方程式,其基本反应类型为.
-
(2) 操作a的名称是,实验室进行此操作时所需的玻璃仪器有烧杯、玻璃棒、.
- 读某国的位置示意图(如图),回答3—4题。3. 斐济(18°08′S,178°26′E )位于下图中甲地的( )
- 函数f(x)=的定义域是F,g(x)=+ 的定义域是G,则F与G的关系是( )A.FG B.FG
- 主族元素W、X、Y、Z的原子序数依次增加,且均不大于20。W、X、Z最外层电子数之和为10;W与Y同族;W与Z形成的化合
- 中国传统农业的主要耕作方式是A.耜耕 B.石器锄耕 C.火耕 D.铁犁牛耕
- 下列各项中书写完全正确的一项是【 】 A、鬼鬼崇崇 功亏一匮 工于心计 沽名钩誉 B、鬼斧神工 冠冕堂
- “旧时王谢堂前燕,飞入寻常百姓家。”常被用来形容过去的一些昂贵商品现在变成了大众消费品,造成这种变化的主要原因是
- 某无色溶液,由Na+、Ag+、Ba2+、Al3+、AlO、MnO、CO、SO、SiO中的若干种组成(不考虑水的电离)。取
- 年轻人往往()自己。
- He narrowly escaped _______in the accident. A.killing
- 设函数. (1)求证:; (2)若成立,求的取值范围.
- 我们学校要开办英语专栏,讨论学习习惯的问题。请你结合自身实际,按一下要点,用英语为该专栏写一篇稿件。... 1. 说明学
- 某学生课外活动小组利用下图所示装置分别做如下实验: (1)在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复
- 在标准状况下,一由排空气法收集满氯化氢气体的烧瓶,测得烧瓶内气体对氢气的相对密度为17,现将烧瓶倒立于水中,求进入烧瓶中
- 小鼠是生物、医药等科研人员经常选择的实验材料,根据下面模式图回答下列问题:(1)若实验小鼠为雌性,上图中甲细胞正在进行
- “晚上十点半,板垣征四郎下令按动了爆炸柳条湖铁轨的按钮,中日延续了十四年的第二次战争从此爆发。”材料所指的是 A.鸦片
- 2002年1月1日,欧洲联盟12国使用的单一货币——“欧元”正式进入流通领域,推动了欧洲区域一体化的进程。欧洲联盟成立于
- 某原电池装置如右图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂。下列叙述正确的是 (
- 把面积一定的线圈放在磁场中,关于穿过线圈平面的磁通量和磁感应强度关系的描述,下列说法正确的是: A.若穿过线圈平面
- 亚洲主体在地球上的位置是() A. 东半球、南半球 B. 西半球、北半球 C. 东半球、北半球 D. 西半球、南半球
- 农业、农村、农民问题关系党和国家事业发展全局。山东省委省政府抓住机遇,出台了一系列政策措施支农、扶农、惠农,山东新农村建



