固体溶解度曲线及其作用 知识点题库
甲、乙两种固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法正确的是( )

A . 将t1℃甲、乙两种物质的饱和溶液升温到t2℃时,甲溶液溶质的质量分数大于乙
B . t1℃时,甲、乙两物质的溶解度相同
C . 将乙物质从溶液中大量结晶,可采用冷却热饱和溶液的方法
D . 将甲物质的饱和溶液升温可变为不饱和溶液
去年,我国部分地区爆发了H7N9禽流感.为了防止禽流感蔓延,人们将家禽捕杀、掩埋,并在禽舍和掩埋坑中洒上大量热石灰.
(1)熟石灰属于 (填“酸”、“碱”或“盐”).用熟石灰处理硫酸厂废水中的硫酸,其化学方程式为 .
(2)熟石灰的溶解度曲线如图所示,30℃时,将1g 熟石灰加入100g水中充分搅拌、过滤,若不计溶液损失,得到溶液的质量是 g.将该溶液降温到20℃,是否有固体析出,(填“是”或“否”)溶液中溶质的质量分数将 (填序号)
A.不变B.增大C.减小.

如图是a、b、c三种物质的溶解度曲线,回答下列问题:

-
(1) 溶解度随温度升高而减小的是物质
-
(2) p点的含义:.
-
(3) 使一定量接近饱和的a物质的溶液变为饱和溶液,可采用的方法是(一种即可)
-
(4) t1℃时将一定量C的饱和溶液升温到t2℃时,溶液的质量将(填“增加”“减少”或“不变”)
-
(5) 将t2℃时50g a物质放入50g水中充分溶解,得到的溶液是溶液(填“饱和”或“不饱和”),此时溶液的质量为 g.
-
(6) 将t2℃时等质量的a、b、c三种物质的饱和溶液降温到t1℃时,析出晶体最多的是,没有晶体析出的是.
如图是a、b、c三种物质的溶解度曲线,下列说法不正确的是( )

A . 加水或升温均可使b的饱和溶液变为不饱和溶液
B . t1℃时,将30ga物质放入100g水中充分溶解得到a的饱和溶液(a物质不含结晶水)
C . 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数关系是b>a=c
D . 分别将等质量的t2℃时三种物质的饱和溶液降温到t1℃,a溶液中析出的晶体最多,c溶液中无晶体析出
水是一种重要的资源,请回答下列各题
-
(1) 下列说法正确的是 (填序号)A . 硬水加入肥皂水容易起浮渣 B . 生活中常用煮沸的方法降低水的硬度 C . 蒸馏水、矿泉水、纯净水等都属于纯净物 D . 自来水厂通过沉淀、过滤、吸附、消毒可将泉水变成纯水
-
(2) 氢气燃烧是人们认识水的组成的开始,该反应的化学方程式为.
-
(3) 水常用于灭火,其灭火原理是.
-
(4) 在通电条件下,水和氯化钠发生化学反应生成氢氧化钠、氧气和氯气,写出此反应的化学方程式.
-
(5) 水是一种重要的溶剂,甲、乙两种物质在水中的溶解度曲线如图所示:

①温度t1℃时(填“>”或“<”),甲物质的溶解度大于乙物质的溶解度.
②t2℃时,用等质量的甲和乙分别配成饱和溶液所需要水的质量是甲乙(填“>”“=”或“<”)
③甲、乙两种物质的饱和溶液温度由t2℃降到t1℃时,溶液组成不发生改变的是(填甲或乙)
图1是甲、乙两种固体物质的溶解度曲线,图2是盛水的烧杯中放着t2℃下甲、乙两种物质饱和溶液的试管(不考虑溶剂的蒸发),根据图象和有关信息判断,下列说法中错误的是( )

A . t2℃时,甲、乙两种物质的饱和溶液中溶质的质量分数大小关系为甲>乙
B . 将甲、乙两种物质的饱和溶液都从t2℃将至t1℃时,两种溶液中溶质的质量分数相等
C . 向烧杯的水中加NaOH固体后,只有乙溶液中溶质的质量分数变小
D . 向烧杯的水中加NH4NO3固体后,只有盛放甲溶液的试管中有晶体析出
如图表示M、N两种不含结晶水的固体物质的溶解度曲线。根据图示判断,下列说法中,正确的是( )

A . M、N的溶解度都随温度的升高而增大
B . 将t1℃时M的饱和溶液升温至t2℃,溶质的质量分数增大
C . 在t1℃时,M、N的饱和溶液中溶质的质量分数二者相等
D . 将t2℃时M、N的饱和溶液分别降温至t1℃,两溶液中均析出晶体
下图所示是甲、乙两种固体物质的溶解度曲线,下列说法正确的是( )

A . 甲的溶解度大于乙的溶解度
B . t℃时,甲、乙的饱和溶液中溶质的质量分数相等
C . 升高温度可以使接近饱和的甲溶液变为饱和溶液
D . 10℃时,分别用100 g水配制甲、乙的饱和溶液,所需甲的质量大于乙的质量
根据右图中甲、乙两种固体物质的溶解度曲线回答问题。

-
(1) P点的含义:在t℃时甲与乙的溶解度;
-
(2) 在温度不变的情况下,把乙的不饱和容液变为饱和溶液的方法是;
-
(3) 甲中含有少量的乙,若提纯甲应采用的结晶方法是。
甲、乙两中固体物质(均不含结晶水)的溶解度曲线如图所示,下列说法错误的是( )

A . t2℃时,将甲、乙的两种饱和溶液分别降温到t1℃,所得溶液都是饱和溶液
B . 甲中混有少量乙时,可用降温结晶的方法提纯甲
C . t2℃时,将等质量的甲、乙两种溶液分别降温到0℃,溶质质量分数:甲<乙
D . t1℃时,20g甲的饱和溶液、15g乙的饱和溶液中,甲和乙的溶解度不相等
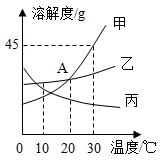
下图为甲、乙、丙三种不含结晶水的固体物质的溶解度曲线。下列说法正确的是( )

A . 三种物质溶解度的大小关系是甲>乙>丙
B .  时甲和丙的饱和溶液中溶质的质量分数相等,均为40%
C .
时甲和丙的饱和溶液中溶质的质量分数相等,均为40%
C .  时将三种物质的饱和溶液恒温蒸发等质量的水,析出晶体的质量关系是乙>甲>丙
D .
时将三种物质的饱和溶液恒温蒸发等质量的水,析出晶体的质量关系是乙>甲>丙
D .  时用等质量的甲、乙、丙分别配制饱和溶液,所得饱和溶液的质量关系是丙>乙>甲
时用等质量的甲、乙、丙分别配制饱和溶液,所得饱和溶液的质量关系是丙>乙>甲
 时甲和丙的饱和溶液中溶质的质量分数相等,均为40%
C .
时甲和丙的饱和溶液中溶质的质量分数相等,均为40%
C .  时将三种物质的饱和溶液恒温蒸发等质量的水,析出晶体的质量关系是乙>甲>丙
D .
时将三种物质的饱和溶液恒温蒸发等质量的水,析出晶体的质量关系是乙>甲>丙
D .  时用等质量的甲、乙、丙分别配制饱和溶液,所得饱和溶液的质量关系是丙>乙>甲
时用等质量的甲、乙、丙分别配制饱和溶液,所得饱和溶液的质量关系是丙>乙>甲
如图是a、b、c三种物质在水中的溶解度曲线(三种物质混合后溶解度不干扰,且它们不发生反应),下列有关叙述不正确的是()

A . 20℃时,b的溶解度大于a
B . 配制c物质的浓溶液时,必须在低温时进行
C . 将50℃时10%a的不饱和溶液降温到20℃,无晶体析出
D . 将50℃时的a和b的饱和溶液降温至20℃,可初步提纯a
右图是甲、乙、丙三种物质的溶解度曲线.下列说法正确的是( )

A . 在t1℃时,三种物质的溶解度由大到水的顺序是甲>乙>丙
B . 在t2℃时,甲、乙两物质的溶解度相等
C . 甲、乙、丙三种物质的饱和溶液升温都会转化为不饱和溶液
D . 当乙的饱和溶液中混有少量丙时,可采用降温结晶的方法析出丙
如图是甲、乙两种固体物质的溶解度曲线.

-
(1) ℃时,甲、乙两种物质的溶解度相等;
-
(2) 把甲物质的不饱和溶液变为饱和溶液,下列有关说法正确是;(填序号,下同)
A 溶剂的质量一定变小
B 溶质的质量可能不变
C 溶质的质量分数一定变大
D 溶液的质量一定变大
E 该饱和溶液还可以溶解其他物质
-
(3) 通常情况下,在实验室用固体甲配制一定溶质质量分数的甲溶液,需用到的仪器有:托盘天平(带砝码盒)、烧杯和.
A 酒精灯 B 药匙 C 玻璃棒 D 漏斗 E 铁架台 F 量筒 G 胶头滴管
如图所示是 A,B,C 三种物质的溶解度曲线,下列分析正确的是 ( )

A . A 物质的溶解度大于 B 物质的溶解度
B . 50 ℃时把 50 g A 放入 50 g 水中能得到 A 的饱和溶液,其中溶质与溶剂的质量比为 1∶2
C . 20 ℃时 A,C 两物质的饱和溶液中含溶质的质量相等
D . 20 ℃时A,B,C 三种物质的饱和溶液升温到50 ℃时,三种溶液的溶质质量分数的大小关系是B>A=C
如图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
-
(1) A点的含义是。
-
(2) 20℃甲,乙,丙三种物质溶解度关系由小到大是。
-
(3) 在30℃时,向30克甲物质中加入50克水,充分溶解后所得溶液质量为。
-
(4) 若甲中混有少量乙,最好采用的方法提纯甲(填“降温结晶”或“蒸发结晶”)。
-
(5) 将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数最小的物质是。
甲、乙、丙三种固体物质的溶解度曲线如图1所示,请回答下列问题:

-
(1) t1℃时,甲、乙、丙三种物质中溶解度最大的是。
-
(2) t2℃时,甲物质的溶解度为g。
-
(3) 将t2℃时的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液溶质质量分数由大到小的顺序为。
-
(4) 如图2,t1℃时,若向烧杯中加入足量的(填字母序号)并使之充分溶解,在试管中可观察到有晶体析出。
A 氯化钠 B 氢氧化钠 C 硝酸铵
如图是A、B、C三种固体物质的溶解度曲线。

-
(1) P点表示的含义是。
-
(2) 图中物质的溶解度与气体物质的溶解度受温度影响变化趋势相似。
-
(3) t1℃时,将35gA物质加入到50g水中,充分溶解后,所得溶液的质量是g。
-
(4) t3℃时,A、B、C三种物质的溶解度由小到大的顺序是。
-
(5) 下列说法不正确的是____(填序号)。A . 能用同一种方法将A、 B . C的不饱和溶液变为饱和溶液B.若B物质中混有少量的A物质,可采用降温结晶法提纯B物质 C . 分别将A、B、C三种物质t3℃时的饱和溶液降温到t1℃,所得溶液的溶质质量分数B>A=C D . 配制一定溶质质量分数的B物质溶液,若量取水时俯视读数,其他操作均正确,则配制得到的B溶液溶质质量分数偏高
氯化钠和硝酸钾部分温度下的溶解度如下表所示:
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 100℃ | |
KNO3 /g | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 246 |
NaCl /g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 39.8 |
-
(1) 欲使硝酸钾的不饱和溶液转化为饱和溶液,可以采取的方法之一是。
-
(2) 从海水中提取食盐通常采取夏天晾晒海水的方法,这是因为随温度升高氯化钠的溶解度。
-
(3) KNO3中混有少量的NaCl可采用的方法分离
-
(4) ①30℃时,在两个各盛有100 g水的烧杯中,分别加入相同质量的氯化钠和硝酸钾,充分溶解后,其结果如图所示。加入的甲物质是。

②有关两种溶液的下列说法中,正确的是。
A.升高温度一定能将剩余的甲物质全部溶解
B.所加入甲物质的质量一定大于36.3g、小于45.8g
C.得到的乙溶液可能是不饱和溶液,也可能是饱和溶液
D.将得到的乙溶液降温至10℃时,溶液中溶质质量分数保持不变
如图是甲、乙两种物质的溶解度曲线,请回答下列问题。

-
(1) 将接近饱和的乙溶液变成饱和溶液的方法是。
-
(2) t2℃时,将50g甲物质加入50g水中,充分搅拌后形成的溶液的溶质质量分数是。
-
(3) t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,此时甲溶液的溶质质量分数乙溶液的溶质质量分数。(填“< ”或“=”或“>”)
最近更新
- 设NA为阿伏加德罗常数的值,下列叙述正确的是 ( )
- 梭伦改革的主要内容是 A.缓和阶级矛盾 B.按财产多寡划分社会等级 C.促进民主政治的发展
- 把抛物线y=x2+2x-3向左平移3个单位,然后向下平移2个单位,则所得的抛物线的解析式为 .
- 传媒真正开始面向大众传递信息,是以的推广为标志的() A.口语媒体 B.文字媒体 C.印刷媒体 D.网络媒体
- 给下列数据填上适当的单位: (1)课桌的高度大约是80 (2)大人行走的速度是4.3 _
- 直线y=2x+k与y=6x-2的交点的横坐标为2,则k=____,交点为(_______).
- .已知反应:① 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ/mol② 稀溶液
- 25.阅读下面的文字,根据要求作文。 皇帝造屋,百工齐集。木匠、石匠暗暗竞赛。一天,木工师傅求胜心切,重责小徒弟。徒
- 如图为验证机械能守恒定律的实验装置示意图.现有的器材为:带铁夹的铁架台、电磁打点计时器、纸带、带铁夹的重锤、天平.回答下
- 实数a,b在数轴上对应点的位置如图所示,化简|a|+的结果是()A.﹣2a+b B.2a﹣b
- (本题满分10分)如图,在梯形中,两点在边上,且四边形是平行四边形.(1)与有何等量关系?请说明理由;(2)当时,求证:
- 已知函数(A>0,>0,0<)的两个邻近的最值点为()和(),则这个函数的解析式为__________
- 用高倍镜观察洋葱根尖细胞的有丝分裂,下列相关叙述正确的是() A.中心体发出的星射线形成纺锤体 B.细胞板出现在分裂期的
- 下列各句中,标点符号使用正确的一项是 A.《中国人的大国情结》一文中(英国《金融时报》12月30日文章)提到,在一些
- 元素R在化合物中只有一种化合价,其氧化物的化学式为R2O3,则下列化学式中正确的是( ) A.R(OH)2 B.R2
- 皮划艇运动员用力划水时,上臂肌肉的状态是( ) A.肱二头肌收缩、肱三头肌收缩 B肱二头肌舒
- Mr. Smith is driving a car in the competition and I’m su
- 两个振动方向和振动频率始终相同的声源,在它们的连线上距离第一声源2 m,距第二声源2.5 m的点上听不到声音,求声源的频
- Why don’t you bring ______ to his attention that you are too
- 请根据下图回答有关问题:(1)在制作人口腔上皮细胞临时装片时,图甲中所滴的液体应是__________。 (2)图乙、丙



