催化剂的特点与催化作用 知识点题库
物质 | a | b | c | d |
反应前质量(g) | 6.4 | 3.2 | 4.0 | 0.5 |
反应后质量(g) | 待测 | 2.56 | 7.2 | 0.5 |
下列说法中错误的是( )
A | B | C | D |
向一定量的石灰水中通入二氧化碳 | 在某一密闭容器内点燃红磷 | 加热一定量氯酸钾和二氧化锰的固体混合物 | 向一定量石灰石中滴加稀盐酸 |
|
|
|
|

-
(1) 写出图中有标号仪器的名称:a、b.
-
(2) 实验室用过氧化氢溶液和二氧化锰制取氧气、选用的发生装置是(填字母编号,下同),反应的化学方程式为,二氧化锰起作用.检验收集氧气是否满瓶的方法是.
-
(3) 实验室常用无水醋酸钠和碱石灰的混合固体在加热条件下制取甲烷气体,选用的发生装置是.甲烷气体一般采用装置F进行收集,当开始收集;收集满后集气瓶的放置方式如图G所示,据此可推断甲烷一定具备的物理性质是.
物 质 | A | B | C | D |
反应前质量/g | 20 | 12 | 2 | 6 |
反应后质量/g | 0 | 2 | 2 | 待测 |



-
(1) 请写出H2O2分解的化学方程式.
-
(2) 【定性研究】如图甲,可通过观察来定性比较两者的催化效果.
-
(3) 【定量研究】如图乙,实验前检查该装置气密性的方法是.要定量比较两者的催化效果,可测量生成等体积气体所需的.
-
(4) 【深入研究】在FeCl3溶液中,究竟是哪种粒子起催化作用呢?猜想1:铁离子(Fe3+)起催化作用; 猜想2:起催化作用; 猜想3:起催化作用;请设计实验,验证猜想1
实验操作
实验现象及结论
 向pH=13的氢氧化钠溶液中加水稀释
B .
向pH=13的氢氧化钠溶液中加水稀释
B .  用相同质量的氯酸钾固体加热分解来制取氧气
C .
用相同质量的氯酸钾固体加热分解来制取氧气
C .  向一定体积的氢氧化钠溶液中逐滴加入稀盐酸
D .
向一定体积的氢氧化钠溶液中逐滴加入稀盐酸
D .  向一定质量一定质量分数的稀盐酸中加入铁粉
向一定质量一定质量分数的稀盐酸中加入铁粉
物质 | a | b | C | d |
反应前的质量/g | 40 | 40 | 10 | 32 |
反应后的质量/g | 12 | x | 10 | 0 |
下列说法正确的是( )
 向一定量铁粉中滴加稀盐酸
B .
向一定量铁粉中滴加稀盐酸
B .  向一定量饱和的硝酸钾溶液中加入硝酸钾固体
C .
向一定量饱和的硝酸钾溶液中加入硝酸钾固体
C .  向一定量CaCO3中加入稀盐酸
D .
向一定量CaCO3中加入稀盐酸
D .  向盛有MnO2的烧杯中加入H2O2溶液
向盛有MnO2的烧杯中加入H2O2溶液

-
(1) 请为此实验拟定一个题目。
-
(2) 写出该反应的化学方程式。
-
(3) pH=时,过氧化氢分解率最高。
-
(4) 实验室用如图装置来制取氧气。

①应选用的反应物的是(填序号)。
A 水 B 过氧化氢 C 高锰酸钾
②该实验中氧气产生快慢可通过观察来实现。
-
(1) 甲同学设计了两种制取氧气的方案:
A、把二氧化锰加入盛有过氧化氢溶液的试管中;
把过氧化氢溶液缓缓加入盛有少量二氧化锰的试管中。
能得到平稳氧气流的是(填A或B)。 -
(2) 乙同学联想二氧化锰作过氧化氢的催化剂,于是想到红砖粉末是否也可以作过氧化氢的催化剂?请你一起参与探究,并回答有关问题。
(猜想与假设)红砖粉末也能作过氧化氢分解的催化剂。
(实验验证)乙同学设计了如下三个实验:
实验一:取一定量过氧化氢溶液于试管中,观察到有极少量气泡产生,将带火星的木条伸入试管中,木条没有复燃。说明过氧化氢在常温下分解缓慢。
实验二:在实验一的试管中加入1克红砖粉末,有大量气泡产生,伸人带火星的木条,木条复燃。
实验三:待反应结束后,将试管中的不溶物滤出,并洗涤、于燥、称量,固体的质量仍为1克,说明。
(实验结论)乙同学认为红砖粉末可以作过氧化氢分解的催化剂。
(反思评价)丙同学认为要证明乙同学的结论正确,还需要再补充一个探究实验,这一探究实验的目的是。
(拓展)下表是丁同学探究影响过氧化氢分解速率的因素时所记录的数据。

通过对数据的分析,你得到的结论是,。(两条)
 比较MnO2和Fe2O3的催化效果
B .
比较MnO2和Fe2O3的催化效果
B .  探究分子的运动
C .
探究分子的运动
C .  测定空气中氧气的含量
D .
测定空气中氧气的含量
D .  证明CO2的密度比空气大
证明CO2的密度比空气大
 B .
B .  C .
C .  D .
D . 
 催化剂表面反应的示意图如下图所示。
催化剂表面反应的示意图如下图所示。 
有关说法错误的是( )
 D .
D .  的质量和性质在化学反应前后都不变
的质量和性质在化学反应前后都不变
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量/g | 40 | 40 | 10 | 32 |
| 反应后的质量/g | 12 | 待测 | 10 | 0 |
下列说法正确的是( )
-
(1) (猜想)Ⅰ、CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ、CuO参与反应产生O2 , 反应前后质量和化学性质发生了改变;
Ⅲ、CuO是反应的催化剂,反应前后
-
(2) (实验)用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如下实验:

填写下表:
步骤③现象
带火星的木条
步骤⑥结果为
固体质量
步骤⑦现象
溶液中有气泡产生
说明
结论
猜想Ⅰ、Ⅱ不成立;
猜想Ⅲ成立
-
(3) 步骤①的目的是。
-
(4) 过氧化氢能被CuO催化分解放出O2的符号表达式为。
2021年9月24日《科学》发表中国科学家首次实现了以二氧化碳为原料,不依赖植物光合作用,直接人工合成淀粉[ 。检测发现,人工合成淀粉分子与天然淀粉分子的结构组成一致。这一人工途径合成淀粉的速率是玉米合成淀粉速率的8.5倍。初步测试显示,在能量供给充足时,理论上1立方米大小的生物反应器年产淀粉量相当于我国5亩玉米地的年产淀粉量。这一突破,为淀粉的车间生产打开一扇窗口,并为以二氧化碳为原料合成复杂分子开辟了新的技术路线。
。检测发现,人工合成淀粉分子与天然淀粉分子的结构组成一致。这一人工途径合成淀粉的速率是玉米合成淀粉速率的8.5倍。初步测试显示,在能量供给充足时,理论上1立方米大小的生物反应器年产淀粉量相当于我国5亩玉米地的年产淀粉量。这一突破,为淀粉的车间生产打开一扇窗口,并为以二氧化碳为原料合成复杂分子开辟了新的技术路线。
-
(1) 二氧化碳到淀粉的转变过程,是变化。(填“物理”或“化学”)
-
(2) 从二氧化碳人工合成淀粉需要11步反应,其中第一步反应
 ;第二步反应:
;第二步反应: 。写出物质X的化学式。已知物质X和Y的组成元素相同,但这两种物质化学性质不同的原因是。
。写出物质X的化学式。已知物质X和Y的组成元素相同,但这两种物质化学性质不同的原因是。
-
(3) 在制造淀粉的过程中使用了催化剂,催化剂在反应前后质量和不变。
-
(4) 下列有关说法正确的是____。A . 人工合成淀粉可减缓粮食危机 B . 人工合成淀粉可降低空气中
 含量
C . 淀粉的相对分子质量162g
D . 淀粉人工合成比玉米通过光合作用合成效率高
含量
C . 淀粉的相对分子质量162g
D . 淀粉人工合成比玉米通过光合作用合成效率高
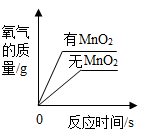 用等质量、等浓度的过氧化氢溶液分别制取氧气
B .
用等质量、等浓度的过氧化氢溶液分别制取氧气
B . 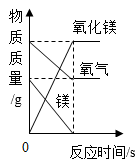 一定量的镁在过量氧气中充分燃烧
C .
一定量的镁在过量氧气中充分燃烧
C . 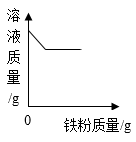 向一定质量的Cu(NO3)2溶液中加入铁粉
D .
向一定质量的Cu(NO3)2溶液中加入铁粉
D . 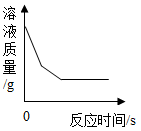 向足量的硫酸铜溶液中加入铁和镁固体混合物
向足量的硫酸铜溶液中加入铁和镁固体混合物
- 火车沿平直铁路匀加速前进,该列车匀加速运动的加速度为0.6m/s2,车头通过某一路标时速度6m/s,当车尾通过该路标时速
- 化简
- 用4种溶液进行实验,下表中“操作及现象”与“溶液”对应关系错误的是选项操作及现象溶液A通入CO2,溶液变浑浊.再升高至6
- 下列溶液中的Cl-浓度与50 mL 1 mol ·L-1 MgCl2溶液中的Cl-浓度相等的是( )
- 甲、乙两个实验小组分别进行“测定Na2CO3和NaCl混合物中Na2CO3含量”的实验。 (1)甲组:沉淀分析法:
- 如下图所示是老师放在实验桌上的三瓶无色气体。它们可能是H2、CO2、O2,下列关于这三种气体的鉴别方法中,不正确的是
- 已知全集U=R,集合A={x|x2-2x>0},B={x|y=lg(x-1)},则(∁UA)∩B等于() A.{x
- 下列物质一定不是天然高分子的是 ( ) A.橡胶
- He is not _______ as a leader but he has gained _______ in t
- 造成“温室效应”的主要物质是 A、二氧化氮B、二氧化碳 C、二氧化硫 D、
- 莱茵河一度几乎被工业污染变成死河,人们用30年时间,700亿欧元,才使它基本恢复。50年代的日本,一些居民因为食用受污染
- 政府承担重要的职能,这些职能的实施所达到的效果,就是政府的作用。我们在生活中主要通过( )来体验政府的作用.
- (8分)为进行Ⅰ项中的除杂实验(括号内为杂质),请从Ⅱ项中选出一种试剂,从Ⅲ项中选出合适的实验操作方法分离,将标号填在后
- 请介绍你最喜爱的电影明星成龙(JackieChan),不少于80字。 内容要点如下: 1. 成龙(Jackie
- 从下面的文字中筛选出具有新闻价值的信息,拟一个新闻标题,不超过15字。 国庆30周年前夕,北京民族文化宫为举行全国民族工
- 给下列句子排序,恰当的一项是 ①病痛是人必须面对的最残酷、最强大和最无情的敌人。 ②它从人刚刚诞生的那一刻起
- 具有相反作用的两种激素是 () ①赤霉素 ②细胞分裂素 ③脱落酸 ④乙烯 A.①和②
- 1.下列词语中加点的字,注音全都正确的一项是 A.矜(jīn)持 挨(āi)批 髌(bìn)骨 不着(
- 2008年7月9日,八国集团首脑会议在日本闭幕。与会者就当前世界面临的一些主要问题达成了一定共识,但并没有取得多少突破。
- 不能从右图中获取的信息是( )A.中央对地方实行分郡管理 B.王朝的都城位于西部







