金属的化学性质 知识点题库
化学就在我们身边,生活中处处有化学。根据你所学过的化学知识,下列说法错误的是( )
A . 体温表中的水银不是银,是金属汞
B . 熟石灰可以用作食品包装袋内的干燥剂
C . “请往菜里加点盐”中的“盐”特指食盐
D . “真金不怕火炼”是指黄金不与氧气反应
称取铜、锌混合物10克置于烧杯中,慢慢加入稀硫酸使其充分反应,直至固体质量不再减少为止,此时用去49克稀硫酸,剩余固体3.5克,计算:
-
(1) 该混合物中铜的质量分数是多少?
-
(2) 所用的稀硫酸溶质的质量分数是多少?
-
(3) 反应后所得溶液中溶质的质量分数是多少?
下列有关说法正确的是( )
A . 酸碱中和后溶液一定呈中性
B . 不饱和溶液变为饱和溶液,溶质质量分数一定变大
C . 向某固体中滴加稀盐酸,有气泡产生,则固体中一定含有碳酸根离子
D . 金属与酸溶液发生置换反应,所得溶液质量一定大于原来酸溶液的质量
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关 系如右图所示,下列说法不正确的是( )

A . a点溶液中的溶质有3种
B . b点溶液是蓝色的
C . c点得到的固体为两种
D . 取d点的固体,加入稀盐酸,无气泡产生
根据要求回答问题:
-
(1) 家用液化石油气(主要成分是丙烷等物质)往往加入少量有特殊气味的物质(如二硫醇),请用分子观点解释下列问题:
①25m3的石油气可以装入0.024m3的钢瓶中.
②液化石油气泄漏时,能嗅到特殊的气味.
③液化石油气燃烧时,生成了水和二氧化碳.
-
(2) 金属在日常生活中应用广泛,请利用金属的性质回答:①铝元素在地壳中的含量远比铜大,但铝的利用却比铜晚得多,其主要原因是什么?②假黄金首饰通常是用黄铜(含Cu、Zn和Pb的合金)制成的,从外观和密度上很难区别其真伪.请你利用家中现有条件,鉴别一件黄金首饰的真假.简述你的操作方法、现象及结论.
下列除去杂质(少量)的方法中,正确的是( )
选项 | 物质 | 杂质 | 除杂方法 |
A | 锌 | 铜 | 滴加适量硝酸银溶液 |
B | 二氧化碳气体 | 氯化氢气体 | 将气体依次通过氢氧化钠溶液、浓硫酸 |
C | 硫酸钠溶液 | 硫酸铜 | 滴加适量氢氧化钠溶液,过滤 |
D | 氯化钾溶液 | 碳酸钾 | 滴加过量硝酸钡溶液,过滤 |
A . A
B . B
C . C
D . D
试设计实验证明:一包黑色炭粉中是否混有铁粉?
常温下,A B均为液态,且组成元素相同.生活中,F可用作补钙剂.x是氧化物,y是红色金属,各物质间的转化关系如图所示(个别产物略去).

-
(1) 推断:E(写化学式)
-
(2) 由H和石灰水可配制农业上常用的杀虫剂波尔多液,波尔多液不能用铁质容器盛放的原因是(用化学方程式表示).
-
(3) 反应④结束后,从混合物中分离出F的方法是.
-
(4) 写出反应⑥的反应方程式:.
向5.6g铁中加入200g硫酸溶液,铁与硫酸恰好完全反应,下列有关说法正确的是( )
A . 反应后溶液中的溶质是Fe2(SO4)3
B . 反应后溶液中SO42﹣质量是9.8g
C . 原硫酸溶液的溶质质量分数是4.9%
D . 反应后溶液的质量是205.5g
下列图象分析错误的是( )
A .  加热氯酸钾和二氧化锰的混合物制取氧气
B .
加热氯酸钾和二氧化锰的混合物制取氧气
B .  利用过氧化氢制取氧气
C .
利用过氧化氢制取氧气
C .  分别向足量的、浓度相同的稀盐酸加入相同质量的镁和锌
D .
分别向足量的、浓度相同的稀盐酸加入相同质量的镁和锌
D .  一定质量的红磷在密闭容器中燃烧
一定质量的红磷在密闭容器中燃烧
 加热氯酸钾和二氧化锰的混合物制取氧气
B .
加热氯酸钾和二氧化锰的混合物制取氧气
B .  利用过氧化氢制取氧气
C .
利用过氧化氢制取氧气
C .  分别向足量的、浓度相同的稀盐酸加入相同质量的镁和锌
D .
分别向足量的、浓度相同的稀盐酸加入相同质量的镁和锌
D .  一定质量的红磷在密闭容器中燃烧
一定质量的红磷在密闭容器中燃烧
如图是实验室模拟工业炼铁的装置图.

-
(1) .分别写出硬质玻璃管内产生的现象反应的化学方程式
-
(2) 实验开始时要先通入CO,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是。
-
(3) 高炉炼铁中,焦炭的两个作用是(用化学方程式表示)。
-
(4) 用含氧化铁80%的赤铁矿200t,可炼制含杂质2%的生铁吨
-
(5) 某合金6 g与足量的稀硫酸充分反应后,如果生成0.2 g氢气,该合金中的金属可能是A . Zn 和Fe B . Cu和Ag C . Zn和Cu D . Mg 和Al
现欲探究一固体混合物A的成分,已知其中可能含有CuSO4、CaCO3、NH4NO3、Cu四种物质中的两种或多种。按下图所示进行实验,出现的现象如图中所述(设过程中所有发生的反应都恰好完全反应)。

试根据实验过程和出现的现象做出判断,填写以下空白:
-
(1) 固体C的化学式为。
-
(2) 在混合物A中,共含有种物质。
-
(3) 气体E的气味是。
-
(4) 溶液G中存在的金属阳离子为(写离子符号)。
-
(5) 写出实验过程②中生成气体E所发生反应的化学方程式:。
我国约在南北朝时就开始冶炼黄铜。黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。为了测定某黄铜样品中锌的质量分数(不考虑黄铜中的其他杂质),现将15mL稀盐酸分三次加入到5g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
|
|
第一次 |
第二次 |
第三次 |
|
加入稀盐酸的体积(mL) |
5 |
5 |
5 |
|
生成氢气的质量(g) |
0.04 |
m |
0.02 |
试求:此黄铜样品中锌的质量分数是多少?(写出计算过程,结果保留至0.1%)
学习了化学知识后,同学们发现生活中处处离不开化学.
-
(1) 生活中的化石燃料包括、石油、天然气.
-
(2) 铝制品耐腐蚀的原因;
-
(3) 生活中将硬水软化的方法是;
-
(4) 炒菜时油锅里的油着火,可以用锅盖灭,灭火原理是.
锌不但能与稀硫酸反应,还能与浓硫酸反应。现将19.5克锌加入含有49克H2SO4的浓硫酸溶液中,充分反应后,测得锌与硫酸恰好反应完全,得到SO2和H2的混合气体。已知锌与浓硫酸反应的化学方程式:Zn+2H2SO4(浓)═ZnSO4+SO2↑+2H2O。
-
(1) H2SO4由(填元素名称)元素组成。
-
(2) ZnSO4中硫原子与氧原子的个数比为。
-
(3) SO2的相对分子质量为,其中硫元素的质量分数为。
-
(4) 计算上述反应产生的气体中SO2的质量。(要求写出计算过程)
铝及其合金在生活中扮演着越来越重要的角色。
-
(1) 医用口罩中鼻梁的绒布里面有一根较软的金属条,该金属最好是(填“纯铝”或“铝合金”)。
-
(2) 铝制品除了在口罩中使用,建筑的门窗中也大量使用了铝合金,铝制品能够耐腐蚀的原因是(用化学方程式表示)。
-
(3) 铝合金中包含铝、镁、铜三种金属,为验证这三种金属的活动顺序,以下药品选择方案不可行的是。
A、硫酸铝溶液、硫酸镁溶液、铜 B、硫酸铝溶液、镁、铜
C、铝、镁、铜、盐酸 D、氯化铝溶液、氯化镁溶液、铝、铜
下面四个图象,能正确反映对应变化关系的是( )
A .  红磷与足量O2充分反应
B .
红磷与足量O2充分反应
B .  铁和硫酸铜溶液反应
C .
铁和硫酸铜溶液反应
C .  将高锰酸钾固体充分加热
D .
将高锰酸钾固体充分加热
D .  等质量的锌和铁与足量稀盐酸反应
等质量的锌和铁与足量稀盐酸反应
 红磷与足量O2充分反应
B .
红磷与足量O2充分反应
B .  铁和硫酸铜溶液反应
C .
铁和硫酸铜溶液反应
C .  将高锰酸钾固体充分加热
D .
将高锰酸钾固体充分加热
D .  等质量的锌和铁与足量稀盐酸反应
等质量的锌和铁与足量稀盐酸反应
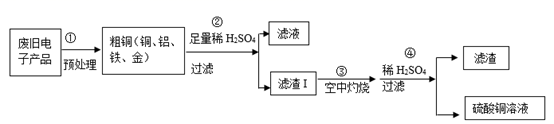
为了从某废旧电子产品中提炼贵重金属,得到硫酸铜溶液。小军所在的学习小组设计了如下流程:
-
(1) 废旧电子产品属于(填“厨余垃圾”或“可回收物”或“有害垃圾”)。
-
(2) ②中发生反应的基本类型为,滤液中存在的金属阳离子有、(填离子符号)。
-
(3) 滤渣Ⅱ中的贵重金属为。
-
(4) 写出④中发生反应的化学方程式。
同学们用锌和稀硫酸制取氢气。向气体发生装置中加入一定量锌粒,加入40g稀硫酸恰好完全反应,产生氢气的质量随时间变化情况如下表。请计算:
|
时间/s |
t1 |
t2 |
t3 |
t4 |
|
生成氢气质量/g |
0.04 |
0.08 |
0.1 |
0.1 |
-
(1) 共制得氢气g。
-
(2) 所用稀硫酸的溶质质量分数。
某工厂废液中含有氯化钠、氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如图所示:

请回答下列问题:
-
(1) 工厂废液中加入过量A反应的化学方程式为。
-
(2) 用化学式表示固体甲的成分。
-
(3) 加入过量B发生反应的基本类型是。
-
(4) 完成步骤④的化学方程式:
 。
。
最近更新
- 生物DNA分子具有特异性的根本原因是因为不同生物的DNA分子具有特定的() A.
- 县乡人大将产生本级人民政府、人民法院、人民检察院,这表明 A.我国国家机构遵循三权分立原则 B.我国国家权力机关即人民代
- 下列是四幅关于光合作用和细胞呼吸的图,有关叙述正确的是()A.图甲中O2浓度为a时,无氧呼吸与有氧呼吸消耗的有机物量相同
- 用自来水养鱼时,通常先将自来水晒一段时间,再注入鱼缸,原因是A.提高水温 B.增加水中氧气的含量C.
- When you are stressed out,you should _________ music. A.list
- 下列不是生物特征的是() A、能进行呼吸 B、会活动 C、能生长繁殖 D、能对刺激发生反应
- ---- Where _______ the guidebook? I can’t see it anywhere.
- 中国人寿作为国内寿险行业的龙头企业,近年来保费收入和资产一直占据领先地位。随着中国加入WTO,面对日趋激烈的市场竞争,该
- 17.阅读下面的材料,根据要求作文。 沙粒进入蚌体内,蚌觉得不舒服,但又无法把沙粒排出。好在蚌不怨天尤人,而是逐步用体内
- 2010年6月我国CPI同比上涨3.3%,物价是反映国民经济运行与发展的重要指标,是国民经济运行与发展的“晴雨表”。作为
- 点是圆内一点,过点最长的弦所在的直线的 方程为( ). A. B. C. D.
- 下列化学用语书写正确的是 A.乙烯的结构简式 CH2CH2 B.氯离子的结构示意图:
- 生活在绿草地的螳螂,体色一般为绿色。对这种现象解释不正确的() A.容易获得食物 B.不易被天敌发现 C.人工
- 甲、乙两个一次射击比赛各射靶5次,两人成绩的条形统计图如图所示,则( ) A.甲的成绩的方差小于乙的成绩的方差 B
- 一辆汽车从车站以初速度为零匀加速直线开去,开出一段时间之后,司机发现一乘客未上车,便紧急刹车做匀减速运动。从启动到停止一
- 某工厂设计了一款产品,成本为每件20元.投放市场进行试销,得到如下数据:售价(元∕件)……30405060……日销售量(
- 已知为虚数单位,且,则的值为 A.4 B. C. D.
- 若a=73 426,k=4,则GET a[k]的值为( ) …A.2 B.6
- —Volunteering is becoming popular in China . —Yeah, peo
- 下列句子中,没有语病的一句是 A.“两会”过后,各地廉租房、限价房政策的相继出台,



