金属活动性顺序及其应用 知识点题库
某兴趣小组为探究活泼金属与酸反应的规律,将质量相等的甲、乙两种金属分别放入到质量分数相同的足量稀盐酸中,经实验测定并绘制出生成氢气的质量与反应时间的关系如图所示。分析图像得到的以下结论一定正确的是( )

某回收站回收的废金属粉末中含锰(Mn)、金(Au)、铜三种金属。为了回收贵重金属,回收站将有关三种金属随意编号为:A,B,C,并设计了如下回收流程:
(1)A,B,C三种金属的活动性顺序为:>>。
(2)C是;B的氧化物的化学式是。
(3)已知A的硫酸盐中A元素显+2价,请写出步骤①的反应的化学方程式:。
(4)你认为步骤③中所加入的X溶液是。
(5)欲直接从蓝色溶液中制得金属B,可选用的试剂是(填标号)。
a、氢氧化钠溶液 b、氯化钠溶液 c、稀盐酸 d、铁
-
(1) 用化学符号或名称填空
①H②Na+③硫酸根④氧化钙⑤2个氮气分子
-
(2) 请用元素符号完成金属活动性顺序表

 B . 向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量
B . 向硫酸和硫酸铜的混合溶液中加入氢氧化钠溶液直至过量 C . 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
C . 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 D . 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
D . 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出
【查阅资料】铁的活动性比铜强。
-
(1) 【进行猜想】对三种金属的活动性顺序做出如下猜想:
猜想一:R>Fe>Cu; 猜想二:; 猜想三:Fe>Cu>R
【收集证据】为了验证哪一种猜想成立,甲、乙、丙三位同学分别展开实验探究。
主要操作
主要现象
实验结论
甲
将打磨好的R丝插入盛有硫酸铜溶液的试管中
猜想一正确
乙
将粗细相同打磨好的R丝、铁丝,分别插入体积和溶质质量分数都相同的稀盐酸中
R丝表面产生气泡速率比铁丝表面产生气泡速率(填“快”或“慢”)
丙
将粗细相同打磨好的R丝、铁丝,分别在空气中点燃
R丝在空气中剧烈燃烧,铁丝在空气中不燃烧
写出铁丝在氧气中燃烧的化学方程式。
-
(2) 【交流反思】三位同学交流讨论后认为,比较金属活动性强弱的方法有多种。
【归纳总结】他们总结得出比较金属活动性强弱的常见方法有:
①金属与氧气反应的难易和剧烈程度;
②金属与酸溶液是否反应或反应的剧烈程度;
③金属与是否反应。
-
(1) 空气中能供给呼吸的气体是;
-
(2) 熄灭酒精灯用灯帽盖灭,其灭火原理是。
-
(3) 标出水中氢元素的化合价。
-
(4) 铁制容器不能盛放硫酸铜溶液的原因(用化学方程式表示)。

-
(1) 写出b~c(不包括b点)段反应的化学方程式.
-
(2) 分别写出a、d所对应溶质的化学式、。
-
(3) 指出a~b段溶液质量变化的原因。

-
(1) 图1是向滤液中加入稀盐酸,观察到有白色沉淀产生。
①滤液中一定含有的金属离子为(填离子符号);
②写出一个产生滤渣的反应的化学方程式。
-
(2) 图2是向滤渣中加入稀盐酸,观察到有无色气体产生。
①滤渣中一定含有(填化学式,下同);
②滤液中可能含有。

-
(1) A中发生反应的化学方程式为。
-
(2) C中铜不与硫酸亚铁溶液反应,其原因是。
-
(3) 若要验证铁、铜、银的金属活动性顺序,依据的现象是。

-
(1) 该浅绿色溶液所含的溶质有(写出化学式)。
-
(2) 写出固体残渣与稀盐酸反应的化学方程式。
-
(3) 将Zn、Fe分别加入到CuSO4溶液中能否根据实验现象判断Zn、Fe、Cu三种金属的活动性强弱 (填“能”或“不能”)。
-
(1) [作出假设]对三种金属的活动性顺序提出三种可能的假设是:
①Cr>Al>Cu②Al>Cr>Cu③Cr>Cu>Al
[设计实验]同温下,取大小相同的这三种金属薄片,分别投入等体积等浓度的足量稀盐酸中,观察现象,记录以下:
金属
Cr
Al
Cu
与盐酸反应现
气泡产生缓慢,金属逐渐溶解
气泡产生激烈,金属迅速溶解
无气泡产生,金属无变化
[控制实验条件]三种金属加入盐酸前都先用纱布将其表面擦光亮,其目的是_________。
A . 除去氧化膜,利于直接反应 B . 使表面光亮,易观察现象 C . 使金属温度相同,易反应 -
(2) [得出结论]原假设中正确的是(选填假设中①、②,③)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式。
-
(3) [结论应用]根据探究结果,请你预测铬与硫酸铜溶液(填“能”或“不能”)反应,理由是。
-
(1) 请分析所得固体的成分。
-
(2) 写出一个有关反应的化学方程式。
-
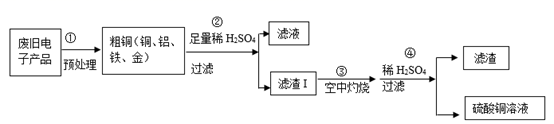
(1) 废旧电子产品属于(填“厨余垃圾”或“可回收物”或“有害垃圾”)。
-
(2) ②中发生反应的基本类型为,滤液中存在的金属阳离子有、(填离子符号)。
-
(3) 滤渣Ⅱ中的贵重金属为。
-
(4) 写出④中发生反应的化学方程式。

-
(1) 孔穴⑤中发生反应的化学方程式为。
-
(2) 六个实验中无明显现象的是(填序号)。
-
(3) 由上述实验得出有关金属的活动性顺序是。
- 下列说法正确的是( ) A.原电池正极发生氧化反应 B.放热的反应在常温下一定易进行 C.反应是放热还是吸热是由反
- 下列观点属于唯物主义的是 ( ) A.天地合
- My name is Dave.I’m from(A) ________.Now I am in Shanghai wi
- The extraordinary EastgateBuilding in Harare, Zimbabwe’s cap
- 某同学要测量一节旧电池的电动势和内阻,实验器材有一个电流表、一个电阻箱R、一个阻值为2Ω的定值电阻R0,一个开关和导线若
- 第二节: (共5小题;每小题2分,满分10分) 根据短文内容,从短文后的选项中选出能填入空白处的最佳选项。选项中有两项为
- 下列各组物质中化学键的类型完全相同的一组是: A. HCl MgCl2 NH4Cl
- 如图,这是农民采用的笼养蝇蛆法而形成的食物网.(说明:鸡粪中含有较多的营养物质未被消化,因此,可添加其他饲料养猪,从生态
- 如果说“舌尖上的中国”展现了中华饮食文化的博大精深,那么“舌尖上的浪费”,则呈现了一种丑陋的饮食观。有效遏制“舌尖上的
- 生物多样性的形成是生物进化的结果,以下说法正确的是 () A.体现了个体水平、生态系统水平上
- 根据句意及所给中文提示、英文解释或首字母写出句中所缺单词,每空限填一词。 1. The thick haze (雾霾)
- —You’ve done a nice job! —Thanks. I always do everything __
- 16世纪初,西班牙的一位家庭主妇抱怨说:“过去一个月的生活费就五个银币,现在十个银币还不够。”这反映当时西班牙出现了
- 装满沙的箱子总重为200N,在50N的水平拉力F的作用下沿地面做匀速直线运动,箱受到地面的摩擦力为___________
- 在下列溶液中一定能大量共存的离子组是A.pH=2的溶液:Fe2+、NH4+、Cl—、NO3—B.能使pH试纸变深蓝色的溶
- So sudden _____ that the enemy had no time to escape.A.did t
- The world has twice as much shipbuilding _______ as it need
- 常温下,下列各组物质中,Y既能与X反应又能与Z反应的是 X Y Z ① NaOH溶液 Al(OH)3 稀硫酸 ② KOH
- (2013北京市海淀区模拟)一般来说,正常人从距地面1.5m高处跳下,落地时速度较小,经过腿部的缓冲,这个速度对人是安
- 在用显微镜观察人的口腔上皮细胞的实验中,下列说法正确的是() A.制作临时装片时要在载玻片的中央滴一滴清水 B.盖盖玻片



