原子的构成与探索过程 知识点题库
下列粒子中,带正电的是( )
A . 电子
B . 质子
C . 中子
D . 原子
汤姆生发现了电子说明是可分的,原子又由和构成。
科学家发现一种新元素.该元素原子核外电子数为117,中子数为174,相对原子质量为291,元素名称Ununseptium,符号Uus.该原子的原子核中的质子数为( )
A . 291
B . 174
C . 117
D . 57
请填表并比较氯原子与氯离子、镁原子与镁离子、镁离子与氯离子,把它们的异同点写在横线上。
粒子名称 | 核内质子数 | 核外电子数 | 粒子所带电荷 |
镁原子 | 12 | 12 | 0 |
镁离子 | 12 | 10 | 两个单位正电荷 |
氯原子 | 17 | 17 | 0 |
氯离子 | 17 | 18 | 一个单位负电荷 |
氯原子与氯离子:。
镁原子与镁离子:。
镁离子与氯离子:。
2015年10月,中国科研团队首次证实了天然铀单质的存在。用于核电工业的一种铀原子中含有92个质子和143个中子。有关该原子的说法不正确的是( )
A . 属于金属元素
B . 电子数为92
C . 核电荷数为92
D . 相对原子质量为143
用“  ”“
”“  ”和“●”分别表示质子、中子和电子,如图表示四种原子结构模型,下列有关说法正确的是( )
”和“●”分别表示质子、中子和电子,如图表示四种原子结构模型,下列有关说法正确的是( )
 甲
甲  乙
乙  丙
丙  丁
丁
A . 甲、丁互为同位素
B . 乙、丁为同一种元素
C . 甲、丙的核电荷数不同
D . 甲、丙为同一种原子
如图表示四种原子的结构模型,下列说法正确的是( )

A . 甲、丁的相对原子质量相同
B . 乙、丁不属于同一种元素
C . 甲、丙的核电荷数不同
D . 甲、乙为互为同位素原子
图示分析法是学习科学的一种重要方法。下列图示分析正确的是( )
A . 地壳中元素含量  B . 原子结构
B . 原子结构  C . 物质分类
C . 物质分类  D . 空气中各成分含量
D . 空气中各成分含量 
 B . 原子结构
B . 原子结构  C . 物质分类
C . 物质分类  D . 空气中各成分含量
D . 空气中各成分含量 
课本中的图表、数据等可以提供很多信息。下面有关的说法正确的是( )
①根据相对分子质量可比较气体的密度大小
②根据不同物质的溶解度曲线图,可确定混合物的分离方法
③“酸、碱和盐溶解性表”是判断复分解反应能否发生的依据之一
④根据某元素的原子结构示意图可判断该元素原子核内中子的数目
A . ①②④
B . ①③④
C . ②③④
D . ①②③
关于原子及原子结构发现史的说法不正确的是( )
A . 汤姆生、卢瑟福两位科学家都是在实验的基础上,通过推理和想象建构原子模型
B . 汤姆生发现了电子,证实原子是可分的
C . 原子核外的电子数发生变化时,元素的种类也发生了变化
D . 原子在化学变化中的表现主要取决于原子的最外层电子
如图为元素周期表的一部分(X元素信息不全)。下列说法正确的是( )
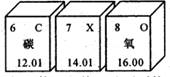
A . 碳的化学性质最活泼
B . X表示N2
C . 氧原子的质子数是8
D . 三种元素原子的中子数肯定不同
在α粒子散射实验中,绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,甚至有极少数α粒子几乎达到180°,像是被金箔弹了回来。α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料。卢瑟福推测:除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。

-
(1) 支持卢瑟福推测的依据是。
-
(2) 1um金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变,说明 。A . 原子的质量是均匀分布的 B . 原子内部绝大部分空间是空的
-
(3) 1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒是。
人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911 年物理学家卢瑟福用 带正电的α粒子轰击金属箔。实验发现:多数α粒子穿过金属箔后仍保持原来的运动 方向,极少数α粒子发生了较大角度的偏转。

-
(1) 卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的。
-
(2) 当用α粒子轰击金属箔时,图中四条运动轨迹不可能出现的是(填字母)。
下列说法中错误的是( )
A . 通常情况下,气体分子间的空隙大于液体分子间的空隙
B . 原子核由中子和电子构成,每个电子带1个单位负电荷
C . 阳离子的质子数一定大于核外电子数
D . 构成物质的粒子有分子、原子和离子
生物体死亡后,体内含有的碳-14会逐渐减少(称为衰变)。科学家可通过测量生物体遗骸中碳-14的含量,来计算它存活的年代,这种方法称为放射性碳测年法。碳-14原子核中含6个质子和8个中子,在衰变时,一个中子变成质子,形成新的原子核。下列关于新原子核的说法正确的是( )
A . 碳原子核,含7个质子,8个中子
B . 氮原子核,含7个质子,7个中子
C . 碳原子核,含6个质子,7个中子
D . 氧原子核,含7个质子,8个中子
2011年3月11日,日本近海发生9.0级强烈地震,从而引发核泄露危机,核事故时往往泄漏出污染物(具有放射性的碘原子)。为避免核辐射,需一次性口服100毫克(不具放射性的碘原子),使人体甲状腺中碘达到饱和而不再吸收外界的碘,从而起到保护作用。请回答:
-
(1) 碘-131是一种质子数为53、中子数为78的碘原子。该原子核外电子数为。
-
(2) 存在于自然界中的另外一种碘原子“碘-127”,其核内质子数是53,中子数是74,它与碘-131的关系是____。A . 同种元素 B . 同种物质 C . 同种分子 D . 同种原子
-
(3) 假设所处的环境已受污染,通过服用加碘食盐(注:加碘食盐中的碘为)的方法能否有效起到避免核辐射的目的呢?
【查阅资料】成人每天食用食盐的质量通常为6 g;某种加碘食盐的标签如图所示。
配料表:氯化钠、碘酸钾(
 )
)净含量:500 g
碘含量(以I计):

【问题分析】500 g该品牌食盐中,含碘的最大质量是。
【结论】日常服用加碘食盐能否起到避免核辐射目的?,原因是。
人们为了揭示原子结构的奥秘,经历了漫长的探究过程。以下是英国科学家卢瑟福进行的探究。
1911年英国科学家卢瑟福进行了著名的α粒子(带正电)轰击金属箔实验。结果发现:绝大多数α粒子穿过金属箔后仍沿原方向前进,但是有少数α粒子却发生了较大角度的偏转,并且有极少数α粒子的偏转角度超过90°,有的几乎达到180°,像是被金属箔弹了回来。
-
(1) 通过上述实验,可推出的原子结构模型为(填字母,下同)。

-
(2) 当α粒子轰击金属箔时,如图所示的运动轨迹不可能的是。

2022年北京冬奥会,碲化镉发电玻璃成为绿色奥运和科技奥运的创新点。碲元素是一种重要的工业添加剂,如碲-128。其相对原子质量为128,质子数为52,则碲-128原子中的中子数为( )
A . 128
B . 52
C . 76
D . 180
“镅”元素目前应用于烟雾探测器、温度计、火灾自动报警仪及医学上。镅的相对原子质量为241,核外电子数为95,则“镅”元素的核电荷数是( )
A . 95
B . 146
C . 241
D . 336
2021年,我国科学家首次合成铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数为92,则铀-214 原子的中子数为( )
A . 92
B . 122
C . 214
D . 306
最近更新
- For a few years, I have been wearing a ring onmy right hand
- 如图中的实线是某时刻的波形图像,虚线是经过0.2s时的波形图像。(1)假定波向左传播,求它传播的可能距离。(2)若这列波
- 不等式x-的解集是__________________.
- 已知函数y=f(x)的反函数为y=g(x),若f(3)=-1,则函数y=g(x-1)的图象必经过点 .
- DNA在氯化钠溶液中的溶解度随着NaCl溶液浓度的变化而变化。请在下列浓度的氯化钠溶液中,选出能使DNA析出最彻底的一种
- 10、函数的图象与直线有且仅有两个不同的交点,则的取值范围是__________。
- 在一次远足活动中,某班学生分成两组,第一组由甲地匀速步行到乙地后原路返回,第二组由甲地匀速步行经乙地继续前行到丙地后原路
- 回答下列有关生态学的问题: ⑴研究人员将Sl与S2两个种群放在一起培养,在环境温度为T1与T2条件下,测得种群数量变化如
- _______ studying English, he also studies Japanese. A. Inste
- 下列说法正确的是( )A. 加入铝粉能产生H2的溶液中,可能存在大量的Na+、Ba2+、AlO2-、NO3- B.
- 反应PCl5(g) PCl 3(g)+Cl2(g) ①2HI(g) H2(g)+I2(g)
- 今年4月中旬,受强冷空气的持续影响,本该是春暧花开的我国北方地区却出现“倒春寒”,暴雪降温严重影响了当地人们的生活和工作
- 根据要求在横线上默写出课文内容、作者或篇名。(11分)1. ,流响出疏桐。居高声自远,
- 实验是学习化学的一个重要途径.请根据如图完成下列各题.(1)仪器①的名称是 ;仪器②的名称是 . (2)实验室用高锰
- 向空中发射一物体,不计空气阻力,当此物体的速度恰好沿水平方向时,物体炸裂成a、b两块,若质量较大的a块速度方向仍沿原来方
- 阅读下面的文字,完成12~15题。 闲 的 视 镜 汪涌豪 ①“闲”是古代文论主体范畴中很重要的一个概念,由其所指称的主
- 2015年10月29日,党的十八届五中全会决定,全面实施一对夫妇可生育两个孩子的政策,这是党中央根据社会发展状况作出的适
- 已知函数的图象关于点A对称,则点A的坐标为 (A)(0,2) (B) (C)
- 已知为虚数单位,为实数,复数在复平面内对应的点为,则“”是“点在第四象限”的 A.充分而不必要条件
- 阅读下面一段文字,在横线上续写一段话,从不同方面阐述写好汉字的意义,并写一句建议 性结语。要求:角度恰当,观点明确,语言



