物质的分离与提纯 知识点题库
-
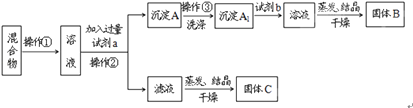
(1) 操作①的名称是,操作②的名称是.
-
(2) 试剂a是,试剂b是,固体B是.(填化学式)
-
(3) 加入试剂a所发生的化学反应方程式为:.
加入试剂b所发生的化学反应方程式为:
-
(4) 该方案能否达到实验目的:若不能,应如何改进(若能,此问不用回答).
-
(5) 若要测定原混合物中KCl和BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是(填“A”、“A1”、“B”、“C”)的质量.
已知:①NaFeO2在水溶液中强烈水解生成对应的氢氧化物.
②2CrO 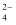 +2H+⇌Cr2O
+2H+⇌Cr2O 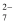 +H2O
+H2O
-
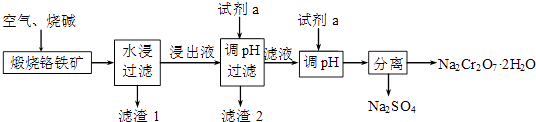
(1) 完成煅烧过程中铬铁矿发生的主要反应的化学方程式:
FeO•Cr2O3+7O2+
 Na2CrO4+NaFeO2+
Na2CrO4+NaFeO2+上述反应中每熔化1mol FeO•Cr2O3 , 转移的电子数为
-
(2) 浸出液的成分除Na2CrO4、NaOH外,还含有(写化学式,下同),滤渣1的成分是.
-
(3) 调节浸出液pH所加的试剂a是(写化学式).
-
(4) 该流程中用了两步调节pH,若合并成一步调pH,酸性过强,产品Na2Cr2O7晶体中可能含有较多杂质,用离子方程式说明引入该杂质的原因.
-
(5) 100kg铬铁矿(含FeO•Cr2O3 89.6%)最多可获得Na2Cr2O7•2H2O的质量为 kg.
物质 | 熔点℃ | 沸点℃ | 密度g•cm﹣3 | 水溶性 |
A | ﹣98 | 57.5 | 0.93 | 可溶 |
B | ﹣84 | 97 | 0.90 | 可溶 |
由此,分离A和B的最佳方法是( )
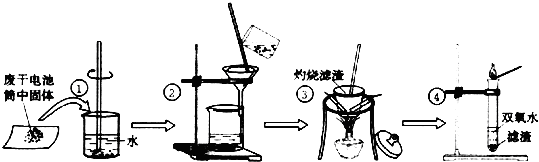
查阅教材可知,普通锌锰电池的黑色物质主要成分为MnO2、NH4Cl、ZnCl2等物质.请回答以下问题:
-
(1) 操作①的名称是;操作②的名称是;
-
(2) 操作③灼烧滤渣时所用主要仪器有酒精灯、玻璃棒、、 和三脚架;操作③灼烧滤渣中的黑色固体时,产生一种使澄清石灰水变浑浊的气体,由此推测滤渣中还存在的物质为.
-
(3) 操作④的试管加入③中所得黑色滤渣,试管中迅速产生能使带火星的木条复燃的气体,据此可初步认定黑色固体为.
-
(4) 该同学要对滤液的成分进行检验,以确认是否含有NH4Cl和ZnCl2 , 下面是他做完实验后所写的实验报告,请你写出其空白处的内容:
实验目的
操作
实验现象
结论
①.检验Cl﹣
取少许滤液于试管中,加入
产生白色沉淀
含有Cl﹣
②.检验NH4+
取少许滤液于试管中,加入
含有NH4+ k
③.检验Zn2+
取少许滤液于试管中,加入稀氨水
先产生白色沉淀,继续加入氨水,沉淀又溶解
含有Zn2+
-
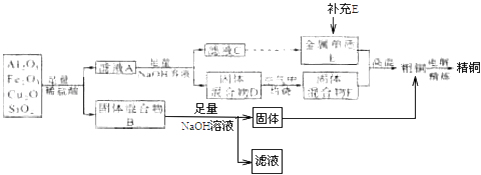
(1) 已知:Cu2O易溶于稀酸溶液,溶液变为蓝色且有紫红色的金属单质生成,写出并配平其反应的离子方程式.
-
(2) 滤液A中铁元素的存在形式为(填离子符号),检验滤液A中存在该离子的试剂为(填试剂名称).
-
(3) 固体混合物B主要含有,其中氧化物的用途为(填写一种用途即可).
-
(4) 金属E与固体混合物F发生反应的化学方程式为.
-
(5) 将Na2CO3溶液滴入到一定量的FeCl3溶液中,有无色无味气体放出,写出相应的离子方程式:.
-
(6) 取10g该铜矿石炼制精铜,可用酸性高锰酸钾溶液滴定法测定粗铜精炼后电解液中铁元素的含量(假设其他物质不与高锰酸钾反应,且流程中不考虑铁元素的损耗).若滴定时用去0.1mol/L的酸性高锰酸钾溶液20.00mL,则该铜矿石中Fe2O3的含量为.
-
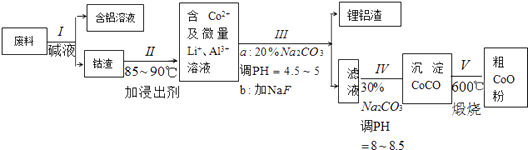
(1) 过程I中采用NaOH溶液溶出废料中的Al,反应的化学反应方程式为.
-
(2) 过程II中加入稀H2SO4酸化后,再加入Na2S2O3溶液浸出钴.则浸出钴的离子反应方程式为(产物中只有一种酸根).请从反应原理分析不用盐酸酸化的主要原因.
-
(3) 碳酸钠溶液在过程III和IV中所起作用有所不同,请分别用离子方程式表示在过程III、IV中起的作用:.
-
(4) 某天然碱的化学式可表示为2Na2CO3•NaHCO3•2H2O,取少量该物质溶于水得稀溶液P.下列有关溶液P中微粒的物质的量浓度关系正确的是 (填序号).A . c(CO32﹣)>c(HCO3﹣)>c(OH﹣)>c(H+) B . c(OH﹣)=c(H+)+c(HCO3﹣)+2c(H2CO3) C . 3c(Na+)>5c(CO32﹣)+5c(HCO3﹣)+5c(H2CO3) D . 将P溶液与少量NaOH溶液混合:c(Na+)+c(H+)=c(HCO3﹣)+2c(CO32﹣)+c(OH﹣)
-
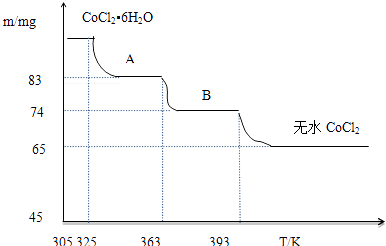
(5) CoO溶于盐酸可得粉红色的CoCl2溶液.CoCl2含结晶水数目不同而呈现不同颜色,利用蓝色的无水CoCl2吸水变色这一性质可制成变色水泥和显隐墨水.如图是粉红色的CoCl2•6H2O晶体受热分解时,剩余固体质量随温度变化的曲线,B物质的化学式是.
已知:
①NaFeO2常温遇大量水会强烈水解,高温时不与水反应
②2CrO42-(黄色)+2H+ ![]() Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
③+6价的铬元素在强酸性条件下具有强氧化性,还原产物为Cr3+ , 强碱性条件下几乎没有氧化性
请回答下列问题:
-
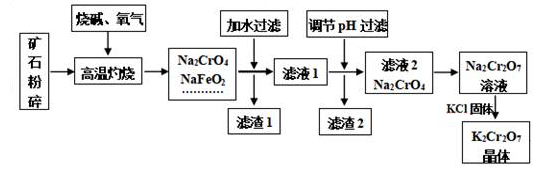
(1) 将矿石粉碎的目的是。
-
(2) 高温灼烧时生成NaFeO2的化学方程式。
-
(3) ①滤渣1的成分为(写化学式,下同),写出生成该物质反应的离子方程式。
②滤渣2的主要成分是。
-
(4) 若向Na2CrO4溶液中加入浓盐酸进行酸化,出现的现象为
-
(5) 生产后的废水中主要含有一定量的Cr2O72- , 通常加一定量的绿矾进行净化并调节pH约为6,可生成两种难溶于水的沉淀,请写出该反应的离子方程式。
A | B | C | D |
从碘水中分离出碘 |
检验溶液中NH4+的存在 |
干燥SO2气体 |
收集HCl气体 |
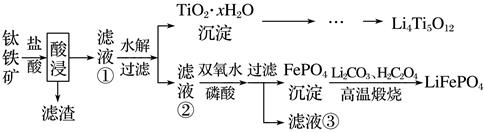
已知:“酸浸”后,钛主要以TiOCl42-形式存在FeTiO3+4H++4Cl-=Fe2++TiOCl42-+2H2O
下列说法错误的是( )
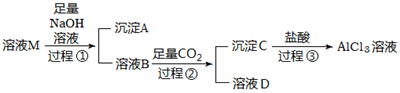
-
(1) 沉淀A的化学式为,过程①中Al3+发生反应的离子方程式为。
-
(2) 氢氧化钠溶液(填“能”或“不能”)用氨水代替,原因是。
-
(3) 溶液B中大量存在的阳离子是,过程②中生成沉淀C的离子方程式为。
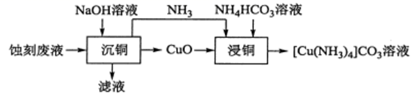
下列有关说法错误的是( )
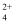 +2OH-
+2OH- 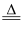 4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、
4NH3↑+CuO↓+H2O
C . “滤液”中大量存在的离子有Na+、  、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
、Cl-和OH-
D . “浸铜”时温度过高可能导致铜的浸出率下降
-
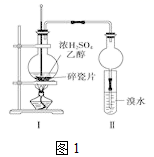
(1) 写出该实验中生成乙烯的化学方程式。
-
(2) 甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确的是。
a.乙烯与溴水易发生取代反应
b.使溴水褪色的反应,未必是加成反应
c.使溴水褪色的物质,未必是乙烯
-
(3) 乙同学经过细致观察后试管中另一实验现象后,证明反应中有乙烯生成,请简述这种这一实验现象。
-
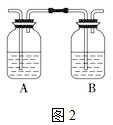
(4) 丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加上图2装置以除去乙醇蒸气和SO2 , 则A中的试剂是,B中的试剂为。
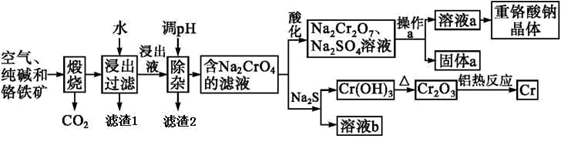
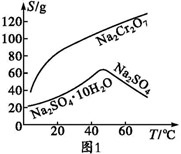
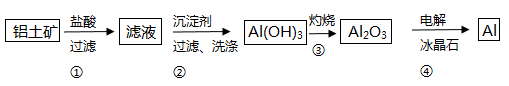
已知部分物质的溶解度曲线如图 1 所示。
请回答下列问题:
-
(1) 若煅烧操作在实验室进行最好选用_____(填序号);A . 石英坩埚 B . 铁坩埚 C . 瓷坩埚
-
(2) 煅烧生成 Na2CrO4 的化学方程式为 。
-
(3) 滤渣 1 的成分为 Fe2O3 , 滤渣 2 的成分除了Al(OH)3之外还有。
-
(4) 操作 a 的实验步骤为,洗涤干燥。
-
(5) 加入
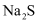 溶液后使硫元素全部以
溶液后使硫元素全部以  的形式存在,写出生成Cr(OH)3的离子方程式。
的形式存在,写出生成Cr(OH)3的离子方程式。
-
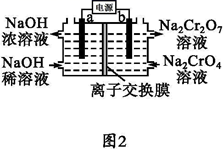
(6) 采用石墨电极电解 Na2CrO4 溶液制备 Na2Cr2O7 , 其原理如图 2 所示。电极 b 为极(填“阳”或“阴”),写出电极 b 的电极反应方程式:。
-
(7) 根据有关国家标准,含
 的废水要经化学处理使其浓度降至5.0×10-7mol·L-1 以下才能排放。可采用加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入硫酸处理多余的Ba2+的方法处理废水。加入可溶性钡盐后,废水中 Ba2+的浓度应不小于mol·L-1 , 废水处理后方能达到国家排放标准。
的废水要经化学处理使其浓度降至5.0×10-7mol·L-1 以下才能排放。可采用加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入硫酸处理多余的Ba2+的方法处理废水。加入可溶性钡盐后,废水中 Ba2+的浓度应不小于mol·L-1 , 废水处理后方能达到国家排放标准。
 、Cl-、NO
、Cl-、NO  。回答下列问题:
。回答下列问题:
-
(1) 下列离子中,能大量存在于该废水中的是_______(填标号)A . Ag+ B . Mg2+ C . OH- D . HCO

-
(2) 取100mL该废水于烧杯,逐滴加入NaOH溶液至呈碱性过程中,原废水中存在的离子的量会发生变化的是Na+、(用离子符号表示)。
-
(3) 某化学社团小组成员欲除去废水样品中的Cu2+和SO
 ,最终得到中性溶液,设计的方案流程如图:
,最终得到中性溶液,设计的方案流程如图: 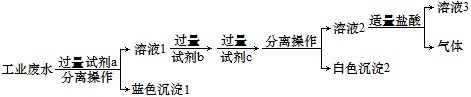
①试剂c为(写化学式);溶液3所含溶质离子有Cl-、。
②“分离操作”的名称是,需用到的玻璃仪器主要有。
③向“白色沉淀2”中加入足量盐酸,发生反应的离子方程式为。
- 真空中有一电场,在电场中的P点放一电荷量为4×10-9C的检验电荷,它受到的电场力为2×10-5N,则P点的场强为___
- 下列结果中,与根的生长有关的部分是A.根冠和生长点B.伸长区和成熟区C.分生区和伸长区D.根冠和伸长区
- ●Tower Bridge is one of London’s most well known landmarks.
- 南宋诗人李清照《乌江》云“生当作人杰,死亦为鬼雄。至今思项羽,不肯过江东。” 这首诗反映了 A.宋词豪放派特点
- 松油醇是一种调香香精,它是α、β、γ三种同分异构体组成的混合物,可由松节油分馏产品A(下式中的18是为区分两个羟基而人为
- 下列各组的两种物质属于同素异形体的是 A. C和C B. 红磷和白磷 C. 丁烷和异丁烷 D. K和Ca
- 下列对某未知溶液中离子的检验方法及其结论一定正确的是( ) A.加入稀盐酸产生无色气体,一
- 隋与秦的统治的相似之处有①结束了长期分裂局面,实现国家的统一②都创立了新的统治制度③兴建了重大的、影响深远的的工程④实行
- 直线交于A、B两点,|AB|=, 则实数k= .
- Having ended the major combat (主战), President Bush_____ rebu
- 下面这段文字有三句话,各有一处语病,请加以修改。(3分)①对于房价的调控,我觉得当前最重要的是各项政策措施的落实。②对于
- 低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为2NH3(g)+NO(g)+NO2(g)2N2(g)+3H2O(
- 如图所示,在研究摩擦力的实验中,用弹簧测力计水平拉一放在水平桌面上的小木块,小木块的运动状态及弹簧测力计的读数如下表所示
- 止痛药并不损伤神经元的结构,却能在一定时间内阻断神经冲动向感觉中枢的传导。 它的作用部位在 A.细胞体 B
- 选词填空,注意使用适当形式。teach, knife, pronounce nine, they【小题1】 Dear,
- 工业上用分离液态空气法制取氧气的依据是 A.氧气与氮气的化学性质不同 B.氧气与氮气
- 根据要求作文。(50分)题目: 来了要求:①把题目补充完整;②有真情实感,力求有创意,不得套写抄袭
- 一个容量为20的样本数据分组后,分组与频数分别如下:[10,20),2;[20,30),3;[30,40),4;[40,
- 嗜盐菌是一种能在高浓度盐溶液中生长的细菌,该菌中有一种结合蛋白质称为菌紫质,菌紫质能将光能转换成化学能。下列叙述正确的是
- 小彤家到学校有一条500m长的平直马路,一次他从学校回家,开始以lm/s的速度匀速行走,当走了一半路程时突然下起了大雨,