有机分子式的推断与计算 知识点题库
-
(1) 求此有机物A的分子式.
-
(2) 若此有机物A跟FeCl3溶液作用显紫色,且有机物A与溴水反应,1mol 有机物A消耗3mol溴单质,写出此有机物A的结构简式以及A与溴水反应的化学方程式.
-
(1) 烃A的分子式为
-
(2) 下列物质与A以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不变的是;若总质量一定,充分燃烧消耗氧气的量不变的是.
A. C7H8 B.C6H14 C.C7H14 D.C8H8
-
(3) 若烃A为链烃,分子中所有的碳原子在同一平面上,该分子的一氯取代物只有一种.
①A的结构简式为名称为
②链烃A与Br2的CCl4溶液反应生成B,写出由A生成B的化学方程式:
③与A互为同分异构体,且主链碳原子个数与A相同的链烃有种(不包括A)
-
(4) 若A不能使溴水褪色,且其一氯代物只有一种,则A的结构简式为.
-
(1) A的分子式是.A的结构简式是.
-
(2) 下列物质中,一定条件能与A发生反应的是 .A . H2 B . Na C . KMnO4 D . Br2
-
(3) 有机物B是A的同分异构体,1mol B可与1mol Br2加成.该有机物所有碳原子在同一个平面,没有顺反异构现象.B中含氧官能团的名称是,B的结构简式是.
-
(4) B可以通过下列变化得到四元环状化合物F
B
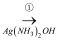
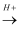 C
C  D
D 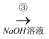
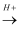 E
E 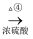 F(C5H8O3)
F(C5H8O3)请写出反应③化学方程式;
上述转化关系中①、②、④的反应类型是:①,②,④.
-
(1) 该化合物的实验式.
-
(2) 若测得该化合物的相对分子质量是30,该化合物的分子式.
-
(1) 此有机物的相对分子质量(结果保留到整数位);
-
(2) 此有机物的分子式;
-
(3) 其所有可能的结构简式.
-
(1) 原混合气体中CO2的质量.
-
(2) 写出该单炔烃可能的结构简式.
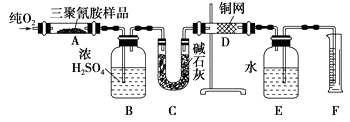
已知三聚氰胺的相对分子质量为126.取1.26g三聚氰胺样品,放在纯氧中充分燃烧,生成CO2、H2O、N2 , 实验测得装置B增重0.54g,C增重1.32g,排入F中水的体积为672mL(可按标准状况计算).
-
(1) E装置的作用是.
-
(2) 需要加热的装置是(填字母代号).
-
(3) 装置D的作用是.
-
(4) F处读数时应该注意:、.
-
(5) 三聚氰胺的分子式为.
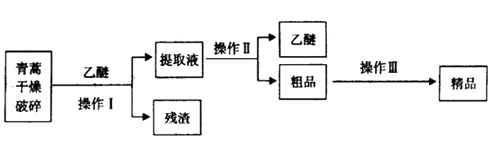
Ⅰ.提取青高素的方法之一是乙醚浸取法,提取流程如下:
-
(1) 对青蒿进行破碎的目的是
-
(2) 操作Ⅰ用到的玻璃仪器是,操作Ⅱ的名称是
-
(3) Ⅱ.燃烧法测定青蒿素的最简式:
利用下列实验装置,将28.2g青蒿素放在燃烧管C中充分燃绕,测出生成的CO2和H2O的质量后,计算得出青蒿素的最简式。
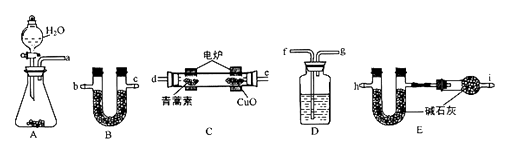
主要实验步骤如下:
①组装仪器,并检查装置的气密性。
②先将A装置的药品反应一会后,再将C装置通电反应。
③称量有关装置的实验前后的质量。
请回答下列问题:
仪器各接口的连接顺序从左到右依次为(每个装置限用一次)。
-
(4) ①装置B中的试剂为,其作用是。
②装置C中CuO的作用是。
③装置D中的试剂为,其作用是。
④装置E中的试剂为,其作用是。
⑤装置F中的试剂为,其作用是。
-
(5) 已知青蒿素是烃的含氧衍生物,用合理连接后的装置进行实验,测量数据如表:
装置质量
实验前/g
实验后/g
B
22.6
42.4
E
80.2
146.2
则青蒿素的最简式为.
-
(1) A的分子式为。
-
(2) A与溴的四氯化碳溶液反应的化学方程式为,反应类型是。
-
(3) 已知:
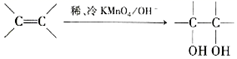 ,请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物的结构简式:。
,请写出A与稀、冷的KMnO4溶液在碱性条件下反应所得产物的结构简式:。
-
(4) 在一定条件下,A与氢气反应得到的化合物中碳的质量分数为85.7%,写出所得化合物的结构简式:。
-
(1) Ⅰ.有机物A的质谱图和红外光谱图分别如下:
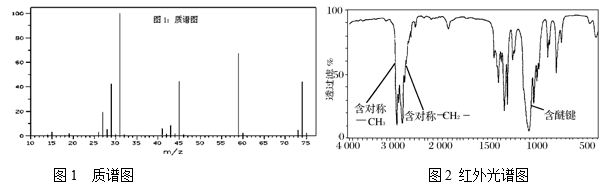
A的结构简式为。
-
(2) Ⅱ.相对分子质量不超过100的有机物B,既能与金属钠反应产生无色气体,又能与碳酸钠反应产生无色气体,还可以使溴的四氯化碳溶液褪色。B完全燃烧只生成CO2和H2O。经分析其含氧元素的质量分数为37.21%。经核磁共振检测发现B的氢谱如图:
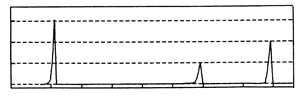
B的结构简式为。
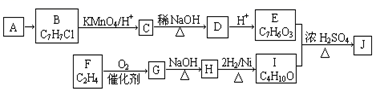
已知:①A是相对分子质量为92的烃
② ![]()

![]() (—R1、—R2—表示氢原子或烃基)
(—R1、—R2—表示氢原子或烃基)
③R1CHO+R2CH2CHO 
![]() +H2O
+H2O
④D的核磁共振氢谱表明其有两种不同化学环境的氢,且峰面积之比为1︰1。
请回答下列问题:
-
(1) A的分子式为,由A→B的反应试剂为。
-
(2) 写出C→D的反应方程式。
-
(3) 同时符合下列条件的E的同分异构体共有种。
①能发生银镜反应 ②能使FeCl3溶液发生显色反应。
-
(4) F的结构式为;写出G→H的反应方程式:。
-
(5) 检验H中含氧官能团的试剂为(填试剂名称)
-
(6) J的结构简式为。
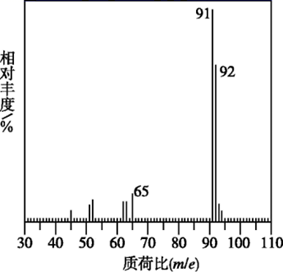
-
(1) A的名称为,1molA完全燃烧消耗氧气的物质的量为。
-
(2) A的二氯代物共有种。
-
(3) A中最多有个原子共平面。
-
(4) 已知9.2gA在足量O2中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重 g和 g。
-
(5) A分子的核磁共振氢谱峰面积之比为。
-
(1) 该有机物的实验式。
-
(2) 若该有机物A的相对分子量为122,属于芳香族化合物,其核磁共振氢谱上有4组峰,且峰面积之比为1∶2∶2∶1,能与金属钠反应产生氢气,也能和新制
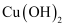 加热后产生砖红色沉淀,该有机物的结构简式是,请写出该有机物与足量新制
加热后产生砖红色沉淀,该有机物的结构简式是,请写出该有机物与足量新制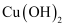 加热后反应的化学方程式。
加热后反应的化学方程式。
-
(3) 有机物A的某种同分异构体B,可用作食品防腐剂,能和碳酸氢钠溶液反应产生气泡。B是无色结晶,熔点122℃,沸点249℃,在水中溶解度如下图:
温度/℃
25
50
75
溶解度/g
0.34
0.85
2.2
B中混有KCl固体和泥沙,若要提纯B,在下列选项中选取合适的操作并正确排序。
①热水溶解 ②趁热过滤 ③过滤 ④冷却结晶 ⑤蒸发结晶 ⑥蒸馏 ⑦洗涤 ⑧干燥
- 下列句子中没有语病的一句是(3分)( ) A、花粉含菌量高的主要原因,往往是收集后未及时脱水或储存方法不当造成
- 辛亥革命“不过是宗法式的统一国家及奴才制的满清宫廷瓦解之表征。至于一切教会式的儒士阶级思想,经院派的诵咒书符教育,几乎丝
- 党的十六届五中全会提出了建设社会主义新农村的重大历史任务。《中共中央国务院关于推进社会主义新农村建设的若干意见》指出,建
- 已知点P()在第三象限,则角在 ( ) A.第一象限 B
- 如图所示,一质点沿螺旋线自外向内运动,已知其走过的弧长s与运动时间t成正比,关于该质点的运动,下列说法正确的是
- 古诗文默写。(10分) (1)问君何能尔? 。 (陶渊明《饮酒(其五)》) (2)不畏浮云遮望眼,
- 正确的实验操作对实验结果、人身安全都非常重要。下列实验操作正确的是( )
- You must choose Mike ourleader. A、as B、with
- I arrived late; I ______ the road to be so icy. A. wouldn’t
- 如图表示生长素浓度对根生长发育的影响,下列叙述正确的是()A.a点是促进根生长的浓度 B.b点是抑制根生长的最佳浓度 C
- 中考体育考试,短跑是必考项目.小宇同学为了考出好成绩,除了刻苦训练之外,还特意购买了一种跑步专用的钉鞋(如图所示).鞋底
- 补写出下列名篇名句中的空缺部分。 荀子在《劝学》中指出:“青, , 。
- 若方程mx+ny=6的两个解是 ,则m= ,n= .
- 下列各组物质中,都是由极性键构成极性分子的是() A.CH4和Br2 B.NH3和H2
- “顶上阴谋家的帽子刚脱,头上便戴上了改革家的桂冠;策略家的徽章未送进门庭,蛮干家的门牌就已挂出。”这是对苏联一位政治家的
- 会展设计师、宠物驯导师、婚姻家庭咨询师、珠宝首饰评估师、调香师……社会日新月异的发展催生了很多新风扑面、生机勃勃的新兴职
- 已知等差数列满足。 (I)求数列的通项公式; (II)求数列的前项和。
- 两圆的半径分别为3和5,若两圆的圆心距等于2,则这两圆的位置关系是 ▲ .
- When I ________________ her in the hall,she was playing the
- 明明和妈妈到商场去购买电饭锅。它从品种繁多的电饭锅说明书中取出一份,下表所示即为该说明书一部分:明明与妈妈商议后,购买了



