不同晶体的结构微粒及微粒间作用力的区别 知识点题库
美国Lawrece Liermore国家实验室(LINL)成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2的原子晶体说法,正确的是:
A . CO2的原子晶体和分子晶体互为同分异构体
B . 在一定条件下,CO2原子晶体转化为分子晶体是物理变化
C . CO2的原子晶体和 分子晶体具有相同的物理性质和化学性质
D . 在CO2的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
干冰和二氧化硅晶体同属ⅣA族元素的最高价氧化物,它们的熔、沸点差别很大的原因是( )
A . 二氧化硅分子量大于二氧化碳分子量
B . C和 O键键能比Si和O键键能小
C . 干冰为分子晶体,二氧化硅为原子晶体
D . 干冰易升华,二氧化硅不能
能与氢氧化钠溶液反应的分子晶体是( )
A . 氧化铝
B . 金刚石
C . 二氧化碳
D . 二氧化硅
下列说法正确的是( )
A . 用乙醇或CCl4提取碘水中的碘单质
B . NaCl和SiC晶体熔化时,克服粒子间作用力类型相同
C . 24Mg32S晶体中电子总数与中子总数之比为1:1
D . H2S与SiF4分子中各原子最外层都满足8电子结构
2014年12月科学家发现了迄今为止最轻的冰﹣﹣“冰十六”,它是水的一种结晶形式,有着像笼子一样、可以困住其他分子的结构.下列相关叙述中不正确的是( )
A . 冰的密度比液态水小
B . 冰与干冰由不同分子构成
C . “冰十六”可以包合气体分子
D . 液态水转变成“冰十六”是化学变化
下列每组物质发生状态变化时所克服的微粒间的相互作用属于同种类型的是( )
A . 食盐和蔗糖熔化
B . 金刚石和硫熔化
C . 碘和干冰升华
D . 二氧化硅和氧化钠熔化
下列有关性质比较不正确的是( )
A . 晶体熔点的高低: 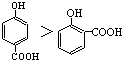 B . 硬度由大到小:金刚石>碳化硅>晶体硅
C . 熔点由高到低:Na>Mg>Al
D . 晶格能由大到小:NaF>NaCl>NaBr>NaI
B . 硬度由大到小:金刚石>碳化硅>晶体硅
C . 熔点由高到低:Na>Mg>Al
D . 晶格能由大到小:NaF>NaCl>NaBr>NaI
 B . 硬度由大到小:金刚石>碳化硅>晶体硅
C . 熔点由高到低:Na>Mg>Al
D . 晶格能由大到小:NaF>NaCl>NaBr>NaI
B . 硬度由大到小:金刚石>碳化硅>晶体硅
C . 熔点由高到低:Na>Mg>Al
D . 晶格能由大到小:NaF>NaCl>NaBr>NaI
下列物质发生变化时,所克服的粒子间的相互作用属同种类型的是( )
A . 液态HF与液态HBr分别受热变为气体
B . 氯化铵与苯分别受热变为气体
C . 氯化钠与氯化氢分别溶解在水中
D . 碘与干冰分别受热变为气体
下列有关说法正确的是( )
A . 物质熔沸点的高低顺序是:晶体硅>氯化钠>干冰>汞
B . 分子晶体中一定存在分子间作用力
C . 水是一种非常稳定的化合物,这是由于氢键所致
D . CO2、HCl、CF4、PCl3四种物质分子中的所有原子都满足最外层为8电子的稳定结构
水的状态有气态、液态、固态,还有玻璃态.玻璃态水是液态水急速冷却到165K时形成的,无固定形状,不存在晶体,且密度与普通水相同.下列有关叙述正确的是( )
A . 当水结成冰时,水分子间的间距会减小,因而密度增大
B . 玻璃态水与液态水具有不同酌化学性质
C . 玻璃态水是水的一种特殊状态
D . 纯净水与食盐水的冰点相同
下列说法正确的是( )
A . 六方最密堆积和面心立方最密堆积的原子堆积方式,空间利用率最高
B . 分子晶体中,分子间作用力越大,分子越稳定
C . 熔点:BaO>CaO>NaCl>KCl
D . 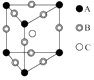 某晶体的晶胞如图所示,这种晶体中A、B、C三种粒子个数之比是1:2:1
某晶体的晶胞如图所示,这种晶体中A、B、C三种粒子个数之比是1:2:1
 某晶体的晶胞如图所示,这种晶体中A、B、C三种粒子个数之比是1:2:1
某晶体的晶胞如图所示,这种晶体中A、B、C三种粒子个数之比是1:2:1
判断下列有关说法中错误的是( )
A . SiCl4是分子晶体
B . 单质B是原子晶体
C . AlCl3是离子晶体
D . MgCl2离子晶体
关于晶体的下列说法正确的是( )
A . 化学键都具有饱和性和方向性
B . 晶体中只要有阴离子,就一定有阳离子
C . 氢键具有方向性和饱和性,也属于一种化学键
D . 金属键由于无法描述其键长、键角,故不属于化学键
下列有关晶体的说法中一定正确的是
①原子晶体中只存在非极性共价键;②稀有气体形成的晶体属于原子晶体;③SO2与S都属于分子晶体,且SO2的摩尔质量比S的摩尔质量大,所以SO2熔沸点高于S;④MgCO3与CaCO3都是离子晶体,且Mg2+半径比Ca2+半径小所以MgCO3的分解温度更高;⑤分子晶体的堆积均为分子密堆积;⑥金属晶体和离子晶体都能导电;⑦离子晶体和金属晶体中均存在阳离子,但金属晶体中却不存在离子键;⑧依据构成粒子的堆积方式可将晶体分为金属晶体、离子晶体、分子晶体、原子晶体( )
A . ①③⑦
B . 只有⑦
C . ②④⑤⑦
D . ⑤⑥⑧
有关晶体的下列说法中正确的是( )
A . 分子晶体中共价键越强,熔点越高
B . 原子晶体中分子间作用力越强,熔点越高
C . 氯化钠晶体熔化时离子键发生断裂
D . 金属晶体熔化时金属键未发生断裂
下列各组物质熔化或气化时,所克服的微粒间的作用力属同种类型的是( )
A . SiO2和CaO的熔化
B . 氧化钠和铁的熔化
C . 碘和干冰的气化
D . 晶体硅和晶体硫的熔化
下列关于晶体的说法正确的组合是( )
①分子晶体中都存在共价键
②在晶体中只要有阳离子就一定有阴离子
③金刚石、SiC、H2O、H2S晶体的熔点依次降低
④离子化合物中只有离子键没有共价键,分子晶体中肯定没有离子键
⑤CaTiO3晶体中(晶胞结构如图所示)每个Ti4+和12个O2-相紧邻
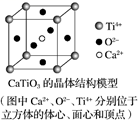
⑥SiO2晶体中每个硅原子与两个氧原子以共价键相结合
⑦晶体中分子间作用力越大,分子越稳定
⑧氯化钠溶于水时离子键被破坏
A . ①②③⑥
B . ①②④
C . ③⑤⑦
D . ③⑤⑧
下列“类比”结果正确的是( )
A . 乙炔的分子构型为直线形,则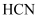 的分子构型也为直线形
B . 单质的熔点
的分子构型也为直线形
B . 单质的熔点 , 则单质的熔点
, 则单质的熔点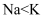 C .
C .  、
、 是酸性氧化物,则
是酸性氧化物,则 也是酸性氧化物
D .
也是酸性氧化物
D .  通入
通入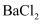 溶液不产生沉淀,则
溶液不产生沉淀,则 通入
通入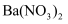 溶液也不产生沉淀
溶液也不产生沉淀
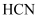 的分子构型也为直线形
B . 单质的熔点
的分子构型也为直线形
B . 单质的熔点 , 则单质的熔点
, 则单质的熔点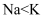 C .
C .  、
、 是酸性氧化物,则
是酸性氧化物,则 也是酸性氧化物
D .
也是酸性氧化物
D .  通入
通入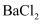 溶液不产生沉淀,则
溶液不产生沉淀,则 通入
通入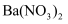 溶液也不产生沉淀
溶液也不产生沉淀
第三代半导体中,碳化硅(SiC)和氮化镓(GaN)是核心半导体。它们具有更宽的禁带宽度、更高的导热率、更高的抗辐射能力、更大的电子饱和漂移速率等特性。
-
(1) 基态Ga原子的价电子排布式为。
-
(2) 晶体硅、碳化硅、金刚石三种晶体的熔点由高到低的顺序为。
-
(3) 氮化镓不存在于自然界中,只能通过人工合成来制备,反应为
 。
。①GaCl3熔点为77.9℃,其晶体类型为。GaF3的熔点为1000℃,则将GaF3熔化时,被破坏的作用力是。
②上述反应涉及的元素中,电负性最小的是(填元素符号,下同),第一电离能最大的是。
回答下列问题:
-
(1) 用系统命名法进行命名:
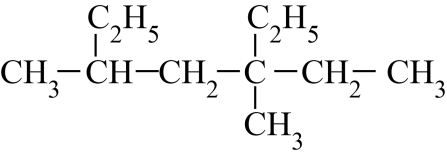 ,若该有机物是由炔烃加成而来,则该炔烃可能的结构有种。
,若该有机物是由炔烃加成而来,则该炔烃可能的结构有种。
-
(2) 邻羟基苯甲醛沸点比对羟基苯甲醛低,因其形成分子内氢键,画出邻羟基苯甲醛的分子内氢键示意图。(用“…”表示氢键)
-
(3) 已知下列物质对应的熔点
物质

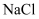
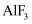
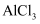




熔点/℃
920
801
1291
190
-107
2073
-57
1723
①指出下列变化时需克服的作用力:干冰升华,
 晶体熔化,
晶体熔化, 溶于水。
溶于水。②
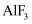 的熔点远高于
的熔点远高于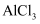 的原因。
的原因。
最近更新
- 下列各组中的三种酸,按酸性由强到弱的顺序排列的是 A.H2SiO3, H2CO3,HNO3
- 下列注音错误最少的一项:( )(2分)A.骸骨 hài踉跄 liàng山峦lān喑哑yā憔悴chuìB.市肆s
- 卤代烃能发生下列反应:2CH3CH2Br+2Na→CH3CH2CH2CH3+2NaBr下列有机物可以合成环丙烷的是()
- 甲队修路120m与乙队修路100m所用天数相同,已知甲队比乙队每天多修10m.设甲队每天修路xm,依题意,下面所列方程正
- 已知f(x)=asin(x+)+bcos(x+),其中a,b, ,均为非零实数,且f(2007)=1, 则f(2008)
- 关于布朗运动,正确的说法是( ). A. 布朗运动是悬浮颗粒的无规则运动 B. 布朗运动是液体分子的无规则运
- 梭伦说:“我拿着一支大盾,保护两方,不让任何一方不公正的占据优势。”“两方”是指A.氏族贵族、奴隶 B.氏族
- .如图,是利用木杆撬石头的示意图.现有一块石头,要使其滚动,杠杆的B端必须向上翘起12cm,已知杠杆的动力臂OA与阻力臂
- 近年来,江苏徐州市积极探索推进基层民主,依靠完善和落实村党组织决策权、村民代表会议议定权、村委会执行权、群众监督权,形成
- 在观察细胞的有丝分裂活动中,将低倍镜转换成高倍物镜后,视野内 A.细胞数目增多,视野变暗 B.细胞数目增多
- 常温下,下列各溶液中能大量共存的离子组是( ) A.由水电离出的c(H+) = 10-12 mol·L-1 的
- 某同学在做蜡烛及其燃烧的探究实验后,知道蜡烛燃烧生成二氧化碳和水,想进一步探究蜡烛熄灭时产生的白烟到底是什么物质,在老师
- — I saw Tom in the school just now. — No, it________ hi
- 将过量CO2通入下列溶液中,最终可能有固体生成的是() A.CaCl2溶液 B.澄清石灰水 C.Na2CO3饱和溶液 D
- 对“生命活动离不开细胞”的理解不正确的是( )A.单细胞生物体具有新陈代谢、应激性等基本的生命特征 B.没有细胞结
- 列各句中按宾语前置情况进行分类,分类正确的一项是 ( ) ①苟得闻大夫之言,何后之有? ②故凡为愚者
- 叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究. 【查阅资料】: ①NaN3受撞击会迅速分
- 有甲、乙、丙三瓶等体积等物质的量浓度的NaOH溶液,若将甲蒸发掉一半水分,在乙中通入少量的CO2,丙不变,然后分别向甲、
- The judge paid no attention to _____ he had just lost his wi
- 孟德尔在对一对相对性状进行研究的过程中,发现了基因的分离定律。下列有关基因分离定律的几组比例,能说明基因分离定律实质的是



