极性键和非极性键 知识点题库
下列化学反应中,同时存在离子键、极性键、非极性键的断裂与生成的是( )
A . 2Na2O2+2H2O=4NaOH+O2↑
B . Mg3N2+6H2O=3Mg(OH)2↓+2NH3↑
C . Cl2+H2O=HClO+HCl
D . NH4Cl+NaOH=NaCl+NH3↑+H2O
下列物质中既有离子键又有非极性共价键的化合物是( )
A . H2SO4
B . NaOH
C . N2
D . Na2O2
石墨烯是从石墨材料中剥离出来、由碳原子组成的只有一层原子厚度的二维晶体.其结构如图:有关说法正确的是 .
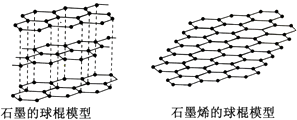

A . 固态时,碳的各种单质的晶体类型相同
B . 石墨烯中含有非极性共价键
C . 从石墨中剥离石墨烯需要破坏化学键
D . 石墨烯具有导电性
H2O2、Na2SO4、KCl、Na2O2、HCl、O2中只含离子键的是,只含极性键的是,只含非极性键的是,既含离子键又含极性键的是,既含离子键又含非极性键的是,既极性键含又含非极性键的是.
下列说法正确的是( )
① H2O2 分子中既含极性键又含非极性键
② F2、Cl2、Br2、I2 熔点随相对分子质量增大而升高
③Na2O2 固体中的阴离子和阳离子个数比是 1∶2
④由于非金属性 Cl > Br > I,所以酸性 HCl > HBr > HI
A . ②③④
B . ①③④
C . ①②③
D . .①②③④
下列说法正确的是( )
A . 气态单质分子中一定含有非极性共价键
B . 含有共价键的化合物可能是共价化合物,也可能是离子化合物
C . 离子键是由阴、阳离子通过静电引力达到平衡时形成的,含有离子键的化合物一定是离子化合物
D . 双原子气体分子中的共价键一定是非极性键
科学家最近研制出可望成为高效火箭推进剂的  (如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关
(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关  的说法正确的是( )
的说法正确的是( )
 (如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关
(如下图所示)。已知该分子中N-N-N键角都是108.1°,下列有关  的说法正确的是( )
的说法正确的是( ) 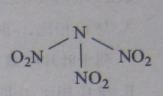
A . 分子中N、O间形成的共价键是非极性键
B . 分子中四个氮原子共平面
C . 该物质既有氧化性又有还原性
D . 15.2g该物资含有6.02×  个原子
个原子
 个原子
个原子
今有A,B两种元素,A的+1价阳离子与B的-2价阴离子的电子层结构与氖相同。
-
(1) 用电子式表示A与B两种元素构成的两种化合物分别为和,前者只有键;后者既有键,又有键。
-
(2) A的氢化物的电子式为,其中含有键,它与水反应的化学方程式为。
-
(3) 元素B的气态氢化物的电子式为,该分子中的键属于(填“极性”或“非极性”)键,该氢化物与H+形成的键属于。
-
(4) 元素A的最高价氧化物的水化物的电子式为,其中既有键,又有键。
-
(5) B元素的单质有和,二者互称为。
下列说法中正确的是( )。
A . 分子之间存在化学键
B . 所有物质中都含有化学键
C . 一个分子中不可能既有极性键又有非极性键
D . 离子化合物中可能含非极性共价键
下列说法正确的是( )
①N2H4分子中既含极性键又含非极性键
②若R2-和M+的电子层结构相同,则离子半径:M+>R2-
③F2、Cl2、Br2、I2熔点随相对分子质量增大而升高
④NCl3、PCl3、CO2、CS2分子中各原子均达到8e-稳定结构
⑤固体融化成液体的过程是物理变化,所以不会破坏化学键
⑥HF分子很稳定是由于HF分子之间能形成氢键
⑦由于非金属性Cl>Br>I,所以酸性HCl>HBr>HI
A . ②⑤⑦
B . ①③④
C . ①③⑥
D . ①③⑤⑥
下列分子中含有的电子数目与HF相同,且只有两个极性共价键的是( )
A . CO2
B . N2O
C . H2O
D . CH4
A、B、W、D、E为短周期元素,且原子序数依次增大,质子数之和为39,B、W同周期,A、D同主族,A、W能形成两种液态化合物  和
和  ,E元素的周期序数与主族序数相等。
,E元素的周期序数与主族序数相等。
 和
和  ,E元素的周期序数与主族序数相等。
,E元素的周期序数与主族序数相等。
-
(1) E元素在周期表中的位置。将B过量的最高价氧化物通入E的含氧酸盐溶液中,可以观察到的现象为。
-
(2)
 分子中存在的,不同于
分子中存在的,不同于  中的化学键被称为。用
中的化学键被称为。用  和稀硫酸浸泡废印刷电路板可溶解其中的
和稀硫酸浸泡废印刷电路板可溶解其中的 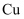 ,试写出反应的离子方程式。
,试写出反应的离子方程式。
-
(3)
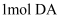 和入足量的水充分反应,生成气体的体积为(标准状况下).
和入足量的水充分反应,生成气体的体积为(标准状况下).
下列物质中只有非极性共价键的是( )
A . NaCl
B . NaOH
C . H2S
D . H2
下列关于物质结构与性质的论述错误的是( )
A . I  离子的空间构型为V形
B . 斜方硫和单斜硫都易溶于CS2 , 是因为这两种物质的分子都属于非极性分子
C . PH3和H2O分子中均含有孤电子对,且PH3提供孤电子对的能力强于H2O
D . 键能O—H>S—H>Se—H>Te—H,因此水的沸点在同族氢化物中最高
离子的空间构型为V形
B . 斜方硫和单斜硫都易溶于CS2 , 是因为这两种物质的分子都属于非极性分子
C . PH3和H2O分子中均含有孤电子对,且PH3提供孤电子对的能力强于H2O
D . 键能O—H>S—H>Se—H>Te—H,因此水的沸点在同族氢化物中最高
 离子的空间构型为V形
B . 斜方硫和单斜硫都易溶于CS2 , 是因为这两种物质的分子都属于非极性分子
C . PH3和H2O分子中均含有孤电子对,且PH3提供孤电子对的能力强于H2O
D . 键能O—H>S—H>Se—H>Te—H,因此水的沸点在同族氢化物中最高
离子的空间构型为V形
B . 斜方硫和单斜硫都易溶于CS2 , 是因为这两种物质的分子都属于非极性分子
C . PH3和H2O分子中均含有孤电子对,且PH3提供孤电子对的能力强于H2O
D . 键能O—H>S—H>Se—H>Te—H,因此水的沸点在同族氢化物中最高
最近,一支研究团队开发了一种新的铜和铁基催化剂,可利用光将二氧化碳转化为天然气的主要成分甲烷,这是迄今最接近人造光合作用的方法。  加氢制CH4的一种催化机理如图。下列说法正确的是( )
加氢制CH4的一种催化机理如图。下列说法正确的是( )
 加氢制CH4的一种催化机理如图。下列说法正确的是( )
加氢制CH4的一种催化机理如图。下列说法正确的是( ) 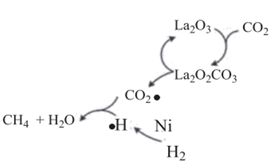
A . 该历程实现了化学能转化为光能,所以反应断键吸收能量大于成键释放的能量
B .  转化为CH4利用了
转化为CH4利用了  的还原性
C . 该历程只有极性键的断裂和极性键的形成
D . 该历程的化学反应方程式为:
的还原性
C . 该历程只有极性键的断裂和极性键的形成
D . 该历程的化学反应方程式为: 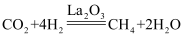
 转化为CH4利用了
转化为CH4利用了  的还原性
C . 该历程只有极性键的断裂和极性键的形成
D . 该历程的化学反应方程式为:
的还原性
C . 该历程只有极性键的断裂和极性键的形成
D . 该历程的化学反应方程式为: 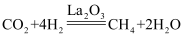
下列说法正确的是( )
A . CH4、CCl4都是含有极性键的极性分子
B .  与NH3、H3O+的空间结构均为三角锥形
C . CS2、H2O、C2H2都是直线形分子
D . 分子中共价键的键能越大,分子的熔、沸点越高
与NH3、H3O+的空间结构均为三角锥形
C . CS2、H2O、C2H2都是直线形分子
D . 分子中共价键的键能越大,分子的熔、沸点越高
 与NH3、H3O+的空间结构均为三角锥形
C . CS2、H2O、C2H2都是直线形分子
D . 分子中共价键的键能越大,分子的熔、沸点越高
与NH3、H3O+的空间结构均为三角锥形
C . CS2、H2O、C2H2都是直线形分子
D . 分子中共价键的键能越大,分子的熔、沸点越高
下列物质中,只含有非极性共价键的是( )
A . NaOH
B . NaCl
C . Cl2
D . H2S
已知A、B、C、D、E、F是原子序数依次增大的前四周期元素,其中元素A的L电子层电子数为0;B元素基态原子的最外层有2个未成对电子;D元素原子的价层电子排布式为nsnnp2n;E元素原子有5个未成对电子;F3+的3d轨道为半充满状态。
-
(1) B2A2分子中,σ键和π键的个数比为;BA
 的键角BA
的键角BA 的键角(填“>”“=”或“<”)。
的键角(填“>”“=”或“<”)。
-
(2) C2的电子式为,CA3的价层电子对互斥模型名称为。
-
(3) A2D2的结构式为,是分子(填“极性”或“非极性”),D元素的杂化类型是。
-
(4) 固体A2D的结构模型中,每个A2D最多与相邻的个A2D相连接,这主要是由氢键的决定的。
-
(5) 气态E2+再失去一个电子比气态F2+再失去一个电子更难的原因是。
新型CeO2材料催化氧化碳烟技术可有效减少汽油燃烧不完全产生的颗粒物,其机理如下图所示,下列说法错误的是新型CeO2材料催化氧化碳烟技术可有效减少汽油燃烧不完全产生的颗粒物,其机理如下图所示,下列说法错误的是( )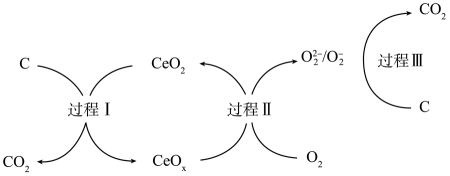

A . 过程III中涉及非极性共价键的断裂
B . 过程II中仅Ce元素的化合价发生变化
C . 环境中 的浓度对除碳烟效果有一定影响
D . 产物
的浓度对除碳烟效果有一定影响
D . 产物 中的氧原子来自于
中的氧原子来自于 和
和
 的浓度对除碳烟效果有一定影响
D . 产物
的浓度对除碳烟效果有一定影响
D . 产物 中的氧原子来自于
中的氧原子来自于 和
和
尿素,又称碳酰胺,其合成原理为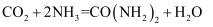 。下列说法正确的是( )
。下列说法正确的是( )
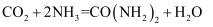 。下列说法正确的是( )
。下列说法正确的是( )
A .  是含有极性键的极性分子
B .
是含有极性键的极性分子
B . 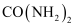 的核磁共振氢谱图中只有一组吸收峰
C .
的核磁共振氢谱图中只有一组吸收峰
C .  分子中氮原子采取
分子中氮原子采取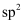 杂化
D .
杂化
D . 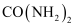 与氰酸铵(
与氰酸铵( )互为同分异构体,组成晶体微粒中作用力类型相同
)互为同分异构体,组成晶体微粒中作用力类型相同
 是含有极性键的极性分子
B .
是含有极性键的极性分子
B . 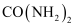 的核磁共振氢谱图中只有一组吸收峰
C .
的核磁共振氢谱图中只有一组吸收峰
C .  分子中氮原子采取
分子中氮原子采取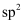 杂化
D .
杂化
D . 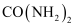 与氰酸铵(
与氰酸铵( )互为同分异构体,组成晶体微粒中作用力类型相同
)互为同分异构体,组成晶体微粒中作用力类型相同
最近更新
- 13. 依次填入下列各句中的成语,最恰当的一组是( )(3分) ①九龙峰古木参天,绿树成荫,泉水淙淙,______
- 已知二次函数的图象如图(7)所示,那么下列判断不正确的是()A.B.C.D.关于x的方程的根是
- 中心法则揭示了生物遗传信息由DNA向蛋白质传递与表达的过程。请回答下列问题。(1)a、b、c、d所表示的四个过程依次分别
- 下列作品中直接反映标志着全国性抗日战争开始事件的是 A.歌曲《我的家在东北松花江上》 B.诗句“宛平城外狼狗叫,卢
- 填入下面横线上的句子,排列恰当的一项是( )(2分)天地有大美,于简单处得;人生有大疲惫,在复杂处藏。人,
- 某学习小组同学用右图实验装置来探究鸡蛋壳里含有CO32﹣(以CaCO3的形式存在)的可能性,请你一起参与学习探究. 【讨
- 用如图的装置来测定空气中氧气含量,根据实验回答下列问题: (1)测定原理:利用固体药品 与空气中的 反应生成,使集气瓶内
- 向澄清的石灰水中吹气的实验证明了人体呼出的气体( ) A.有二氧化碳
- 法国大革命曾给人们带来了极大的想象空间,但大革命经过多次反复之后,人们看到的却是一个欲望横流、道德沉降的讽刺画面。&ld
- 下列实验方案能够达到目的的是A.将溴乙烷与NaOH溶液混合后振荡、静置,直接向反应后的混合物中滴加AgNO3溶液,检验B
- 已知某溶液Cl-、Br-、I-的离子数之比为1:2:3,要使溶液Cl-、Br-、I-的离子数之比变为3:2:1,则通入C
- 阅读以下材料,回答问题。 河流的侵蚀、沉积及沼泽的吸收(附)影响河流泥沙和营养物质含量,水体中营养物质含量影响浮游生物量
- 某犯了贪污罪的官员说:“近几年,逢年过节,迎来送往,在这种温柔的攻势下,我丧失了警惕。我的堕落就像温水里煮青蛙,没有感到
- 读世界不同地区或国家的地理事物景观图,判断回答以下小题。 1.图中①②③④地理事物景观所在地区或国家分别是(
- We can’t help believe that the old hatred shall someda
- 在下面横线上,根据提供的语句,续写句子。 画家画花,独绘一枝,意在留些天地,让欣赏者自己去想; 音乐家演奏,抑扬顿挫,有
- 下列分子或离子中的中心原子杂化轨道的类型不相同的是 ( )A.NO3-、CH2O
- (5 分) 在测定玻璃砖折射率的实验中,某同学只插了三根大头针,但记录了玻璃砖的界面MN和PQ,MN平行于PQ,请在图上
- 阅读下文,完成第18―21题。鸟梁秋实①我爱鸟。②从前我常见提笼架鸟的人,清早在街上溜达。我感觉兴味的不是那人的悠闲,却
- 某化学兴趣小组为了制取并探究氨气性质,按下列装置(部分夹持装置已略去)进行实验。 【实验探究】 (1) 利用如图装置制取



