用电子式表示简单的离子化合物和共价化合物的形成 知识点题库
已知:①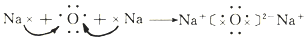
②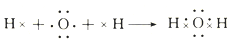
下列说法不正确的是( )
A . ①和②的变化过程中都有电子的得失或偏移
B . ①和②所得的化合物中各原子均达到8电子稳定结构
C . Na2O中含有离子键,H2O中含有极性共价键
D . ①和②过程中原子的总能量高于相应的化合物的总能量
氮化镁是科学家们制备的一种重要化合物,它可由单只直接化合而成,它与水作用的产物之一为NH3 . 请回答下列问题:
-
(1) Na3N是由键形成的化合物,写出它的电子式:.
-
(2) Na3N与水反应属于 (填基本反应类型),写出该反应的化学方程式:.
-
(3) Na+与N3﹣的半径关系是Na+(填“>”、“<”或“=”)N3﹣ .
-
(4) Mg3N2与盐酸的反应生成种盐,用电子式表示其中只含有离子键的盐的形成过程,写出另一种盐的电子式
下列各式用电子式表示的物质的形成过程,其中正确的是( )
A . 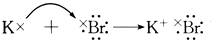 B .
B . 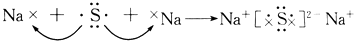 C .
C . 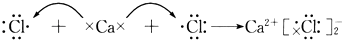 D .
D . 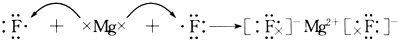
A~H均为短周期元素,A~F在元素周期表中的相对位置如图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素.由B、G组成的气态化合物甲水溶液呈碱性.
A | B | C | |
D | E | F |
请回答下列问题:
-
(1) 写出甲的电子式,实验室制取气体甲的化学方程式为
-
(2) B,C,G个数比为1:1:5形成的化合物的化学键类型为.
a.离子键 b.极性键 c.非极性键
-
(3) 请用电子式表示AE2的形成过程.
-
(4) 用离子符号表示C、E、F、H四种离子的半径由大到小的顺序.
-
(5) 用一个离子方程式解释A比D非金属性强的原因.
下列叙述中错误的是( )
A . 共价化合物中,一定含非金属元素
B . 共价化合物中,一定没有离子键
C . 离子化合物中可能含有共价键
D . 离子化合物中一定含有金属元素和非金属元素
下列关于共价化合物和离子化合物说法正确的是( )
A . 只含共价键的物质一定是共价化合物
B . 离子化合物都能溶于水,且熔点一般都较高
C . 全由非金属元素组成的化合物中可能含有离子键
D . 气态单质分子中一定含有非极性共价键
下列表示正确的是 ( )
A . 双氧水的电子式: 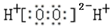 B . 二氧化硅的分子式:SiO2
C . 乙炔的球棍模型:
B . 二氧化硅的分子式:SiO2
C . 乙炔的球棍模型:  D . 聚氯乙烯的结构简式:
D . 聚氯乙烯的结构简式: 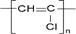
A、B、C、D、E、F、G是周期表中短周期的七种元素,有关性质或结构信息如下表:
|
元素 |
有关性质或结构信息 |
|
A |
其一种单质可吸收紫外线,是地球的保护伞 |
|
B |
B阳离子与A阴离子电子数相同,且是所在周期中单核离子半径最小的 |
|
C |
C与B同周期,且是所在周期中原子半径最大的(稀有气体除外) |
|
D |
D原子最外层电子数是电子层数的2倍,其氢化物有臭鸡蛋气味 |
|
E |
E与D同周期,且在该周期中原子半径最小 |
|
F |
F的氢化物和最高价氧化物的水化物反应生成一种离子化合物 |
|
G |
G是形成化合物种类最多的元素 |
-
(1) B元素符号为,G的元素名称为,它的一种同位素可测定文物年代,这种同位素的符号是。
-
(2) A与C以原子个数比为1:1形成的一种化合物,其所属化合物类型为(填“离子化合物”或“共价化合物”),包含的化学键有(填“离子键”、“极性共价键”或“非极性共价键”)。
-
(3) F常温下可以形成两种用途广泛的氢化物,它们的电子式分别为和,并用电子式表示出其最简单气态氢化物的形成过程。
-
(4) D在元素周期表中的位置,D与E相比非金属性较强的是 (填元素名称),请从原子结构的角度解释原因:。
-
(5) KClO3可用于实验室制O2 , 若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1。写出该反应的化学方程式:。
下列关于化学用语表达正确的是( )
A . 硫原子的原子结构示意图: 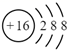 B . CaCl2的电子式为:
B . CaCl2的电子式为: 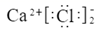 C . CO2的电子式为
C . CO2的电子式为 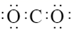 D . CCl4的电子式为:
D . CCl4的电子式为: 
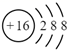 B . CaCl2的电子式为:
B . CaCl2的电子式为: 
下列有关化学用语的表达错误的是( )
A . 次氯酸的电子式: 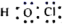 B . CCl4分子的比例模型:
B . CCl4分子的比例模型:  C . 硫离子的结构示意图:
C . 硫离子的结构示意图: 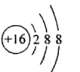 D . 过氧化钠的形成过程:
D . 过氧化钠的形成过程: 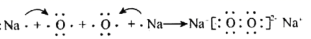
 D . 过氧化钠的形成过程:
D . 过氧化钠的形成过程: -
(1) 小明同学想通过比较两种最高价氧化物水化物的酸性强弱来验证S与C的非金属性的强弱,他查阅了资料:可以利用强酸制备弱酸的原理来判断酸性强弱。于是小明采用了下图所示的装置进行实验。请回答:
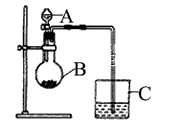
仪器A的名称是,应盛放下列药品中的。
a.稀硫酸 b.亚硫酸 c.氢硫酸 d.盐酸
-
(2) 仪器B的名称是,应盛放下列药品中的。
a.碳酸钙 b.硫酸钠 c.氯化钠 d.碳酸钠
-
(3) 仪器C中盛放的药品是澄清石灰水,如果看到的现象是澄清石灰水变浑浊,证明B中发生反应生成了,即可说明H2SO4 比H2CO3 酸性强,非金属性S比C强,B中发生反应的离子方程式为。
-
(4) 用电子式表示下列化合物的形成过程:
CaF2:
H2S:
-
(5) 有下列物质:①NaOH ②I2 ③MgCl2 ④Na2O2 ⑤氩气 回答下列问题:
①不存在化学键的是,
②既存在离子键又存在极性键的是。
下列叙述正确的有( )个
①用电子式表示MgCl2的形成过程为: ![]()
②两个不同种非金属元素的原子间形成的化学键都是极性键
③离子化合物在熔融状态时能够导电
④含有非极性键的化合物一定是共价化合物
⑤元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
⑥次氯酸的电子式: ![]()
⑦离子化合物中一定含有离子键
A . 1
B . 2
C . 3
D . 4
甲、乙、丙、丁、戊五种元素,其中甲元素原子核外L层上s能级和p能级电子个数相同;乙元素原子3p能级上只有1对成对电子;丙和丁元素原子N层上都只有1个电子,但其中丙元素原子各内层均已充满;而丁元素原子次外层的电子充满在2个能级中;戊元素原子最外层电子排布图是 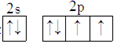 ,它的单质常温时为气态。试用化学符号回答以下问题。
,它的单质常温时为气态。试用化学符号回答以下问题。
-
(1) 甲是,乙是,丙是,丁是,戊是。
-
(2) 丙和乙的单质发生化合反应的化学方程式是:。
-
(3) 丙的硝酸盐溶液跟乙的气态氢化物发生反应的离子方程式是:。
-
(4) 甲和乙元素组成的化合物的化学式是,用电子式表示该化合物的形成过程。
-
(5) 乙和戊元素的气态氢化物沸点高低关系是>。
-
(6) 丙的硫酸盐跟少量氨水反应的离子方程式是:。
-
(7) 丙元素原子的外围电子排布式是。
-
(8) 乙和丁形成的化合物的电子式是。
A、B、C、D、E、F、G七种短周期元素,其原子半径和化合价关系如下表所示。已知:Mg的原子半径为0.160nm。
|
元素 |
A |
B |
C |
D |
E |
F |
G |
|
原子半径(nm) |
0.037 |
0.074 |
0.075 |
0.077 |
0.099 |
0.102 |
0.186 |
|
最高正化合价 |
+1 |
+5 |
+4 |
+7 |
+6 |
+l |
|
|
最低负化合价 |
-1 |
-2 |
-3 |
-4 |
-l |
-2 |
-
(1) 元素G在周期表中的位置为,D、E、F的氢化物中最稳定的是(填化学式)。
-
(2) 元素A、B形成的1:1型化合物的电子式为,根据电子是否得失与电子对是否偏移的角度判定:该物质含有的化学键类型有。
-
(3) 用电子式表示G2F的形成过程。
-
(4) 写出D的单质与ACB3的浓溶液反应的化学方程式(注明条件)。
-
(5) 元素A和元素D可组成含9e-的中性原子团,其名称是。
下列化学用语书写错误的是( )
A .  的分子结构模型为:
的分子结构模型为:  B . 碳酸钾电离方程式:
B . 碳酸钾电离方程式: 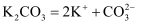 C . 用电子式表示
C . 用电子式表示  的形成过程:
的形成过程: 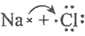 →Na+
→Na+ 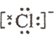 D .
D .  还原
还原 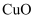 反应中电子的转移:
反应中电子的转移: 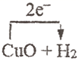
 Cu+H2O
Cu+H2O
 的分子结构模型为:
的分子结构模型为:  B . 碳酸钾电离方程式:
B . 碳酸钾电离方程式: 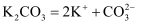 C . 用电子式表示
C . 用电子式表示  的形成过程:
的形成过程:  还原
还原 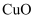 反应中电子的转移:
反应中电子的转移: 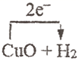
 Cu+H2O
Cu+H2O
A、B、C均为短周期元素,可形成A2C和BC2两种化合物。A、B、C的原子序数依次递增,A原子的K层的电子数只有一个,B原子2p能级有一个空轨道,而C原子M 层只有两对电子对。
-
(1) 它们的元素符号分别为:A;B;C;
-
(2) 用电子式表示A2C的形成过程;
-
(3) BC2是由键组成的(填“极性”或“非极性”)分子;BC2分子中B原子采用杂化类型。
下列关于化学用语的描述中正确的是( )
A . 硫离子的结构示意图: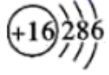 B .
B .  的电子式:
的电子式: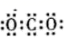 C . 乙烷的结构式:
C . 乙烷的结构式: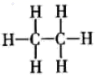 D . 用电子式表示氯化氢分子的形成过程:
D . 用电子式表示氯化氢分子的形成过程:
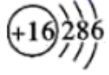 B .
B .  的电子式:
的电子式: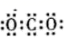 C . 乙烷的结构式:
C . 乙烷的结构式: D . 用电子式表示氯化氢分子的形成过程:
D . 用电子式表示氯化氢分子的形成过程:
过氧化钠常用作供氧剂:2Na2O2+2H2O=4NaOH+O2↑。下列说法错误的是( )
A . Na2O2 的电子式: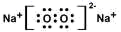 B . Na+的结构示意图:
B . Na+的结构示意图: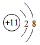 C .
C .  O 与
O 与 O互称为同位素
D . NaOH 属于离子化合物,仅含有离子键
O互称为同位素
D . NaOH 属于离子化合物,仅含有离子键
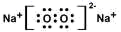 B . Na+的结构示意图:
B . Na+的结构示意图: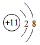 C .
C .  O 与
O 与 O互称为同位素
D . NaOH 属于离子化合物,仅含有离子键
O互称为同位素
D . NaOH 属于离子化合物,仅含有离子键
如图列出了①~⑩十种元素在周期表中的位置:
|
族 周期 |
ⅠA |
0 |
||||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
② |
③ |
④ |
|||||
|
3 |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
|||
|
4 |
⑩ |
|||||||
请回答下列问题:
-
(1) 上述元素中,M层电子数最多的是(填元素名称),最高价氧化物对应的水化物酸性最强的是(填酸的化学式)。
-
(2) 由④、⑤、⑦、⑧四种元素形成的简单离子半径由大到小的顺序是(用离子符号表示)。
-
(3) 由元素①和④形成的18电子的物质的电子式为;由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程:。
-
(4) 元素⑦的最高价氧化物对应的水化物与元素⑨的最简单氢化物的水溶液反应的离子方程式为。
-
(5) 请用一个化学方程式证明元素⑧和⑨的非金属性强弱关系:。
-
(6) 下列可以比较⑤、⑥两元素金属性强弱的实验是___________(填字母)。A . 比较这两种元素最高价氧化物对应的水化物的碱性 B . 将⑤的单质投入到⑥的盐溶液中 C . 将形状、大小相同的这两种元素的单质分别与等体积
 的水反应
D . 比较这两种元素的单质与酸反应时失电子的数目
的水反应
D . 比较这两种元素的单质与酸反应时失电子的数目
下表是元素周期表的一部分,回答下列关问题:
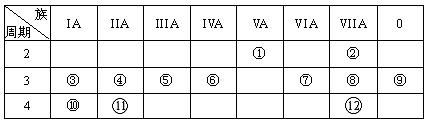
-
(1) 下列表述中能证明元素⑦与元素⑧非金属性强弱关系的是。
a.常温下⑦的单质和⑧的单质状态不同
b.⑧的氢化物比⑦的氢化物稳定
c.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
d. 元素⑧的氧化物的水化物酸性强于元素⑦的氧化物的水化物酸性
-
(2) 第三周期中,原子半径最大的元素是(填元素符号),简单离子半径最小的是(填化学式)。
-
(3) ④与⑧可以形成(填离子或共价)化合物,请用电子式表示其形成过程:。
最近更新
- 在做完“验证力的平行四边形定则”实验后,某同学将其实验操作过程进行了回顾,并在笔记本上记下如下几条体会,你认为他的体会中
- 下图为某时刻我国局部地区太阳高度分布示意图,图中圆圈为等太阳高度线,水平直线表示纬线,竖直的直线表示经线,读图回答问题。
- 下列词语中加点的字,读音全都相同的一组是 A.捆扎 挣扎 扎堆聊天 安营扎寨 B.绯红 扉页
- 根据课文默写古诗文。(10分) (1)、感时花溅泪,________________。(杜甫《春望》) (2)、晴川历历
- ......
- 一门反坦克炮瞄准一辆坦克,开炮后经过0.6s看到炮弹在坦克上爆炸,又经过2.1s听到爆炸声,则大炮距离坦克_______
- 昆明是中国历史文化名城之一,在昆明有一条很不起眼的小巷——先生坡。从图一的路牌上我们可以读到的历史A.禅让制
- 17世纪70年代末,英国国会内两个政党(辉格党和托利党)的出现,表明 A.英国资产阶级革命的完成 B.英国近代政党的起源
- 阅读下面文言文。完成下面题目。(8分)《公输》片段于是见公输盘。子墨子解带为城,以牒为械。公输盘九设攻城之机变,子墨子九
- (1)有一内电阻为100欧姆的微安表,其刻度盘如图所示。今给此微安表串联一个9 900欧的电阻,使之改装成为一个电压表。
- (3分)请按以下要求画图: (1)在图中,画出静止在斜面上的物体A受到的重力的示意图。(2)如图是安装在安全文明小区进出
- 如图,已知,是斜边的中点, 过作于,连结交于; 过作于,连结交于; 过作于,…,如此继续,可以依次得到点,…,,分别记…
- 三角形的三条边长分别是,则的取值范围是 .
- A government official was murdered lastFriday and the police
- 人不寐,
- 在化学学习、研究中,类推的思维方法有时会产生错误的结论,因此类推的结论最终要经过实践的检验才能确定其正确与否。下列几种类
- “如果你无法成为山顶的青松,那就成为山谷的树吧,如果你不能成为太阳,那你就成为一颗星星吧!” 以及“你最好接受自己的长相
- 古代诗歌阅读(11分) 咸阳城东楼① (唐)许浑 一上高城万里愁,蒹葭杨柳似汀洲②。 溪云初起日沉阁,山雨欲来风满楼。
- —Your English is very good. —______.A.You're right
- George _________ too far. His coffeeis still warm. A. must



