化学反应速率和化学计量数的关系 知识点题库
-
(1) 此反应在四种不同情况下的反应速率分别为:
①v(A)=5mol•L﹣1•min﹣1
②v(B)=6mol•L﹣1•min﹣1
③v(C)=4.5mol•L﹣1•min﹣1
④v(D)=8mol•L﹣1•min﹣1
其中反应速率最快的是 (填编号).
-
(2) 下列叙述能证明该反应已达到化学平衡状态的是(填标号,下同) .A . 容器内压强不再发生变化 B . C的体积分数不再发生变化 C . 容器内气体原子总数不再发生变化 D . 相同时间内消耗2n mol B的同时消耗n molA E . 气体密度保持不变 F . 气体的平均摩尔质量保持不变.
 3B(g)+C(g),若反应物在前20s由3mol降为1.8mol,则前20s的平均反应速率为( )
3B(g)+C(g),若反应物在前20s由3mol降为1.8mol,则前20s的平均反应速率为( )
①v(A)=0.15 mol·L-1·s-1
②v(B)=0.6 mol·L-1·s-1
③v(C)=0.4 mol·L-1·s-1
④v(D)=0.45 mol·L-1·min-1
该反应进行的快慢顺序为( )
-
(1) 已知:
CoS2(s) +CO(g)
 CoS(s) +COS(g) ∆H1
CoS(s) +COS(g) ∆H12COS(g) +SO2(g)
 3S(s) +2CO2(g) ∆H2
3S(s) +2CO2(g) ∆H2S(s) +CoS(S)
 CoS2 (s) △H3
CoS2 (s) △H3则2CO(g)+ SO2(g)
 2CO2(g)+S(s) ∆H4=。 (用∆H1、 ∆H2、∆H3表示)
2CO2(g)+S(s) ∆H4=。 (用∆H1、 ∆H2、∆H3表示) -
(2) 在恒温、恒压的容器中模拟回收硫,加入SO2起始量均为1mol,测得CO2的平衡体积分数随CO和SO2的投料比变化如图:
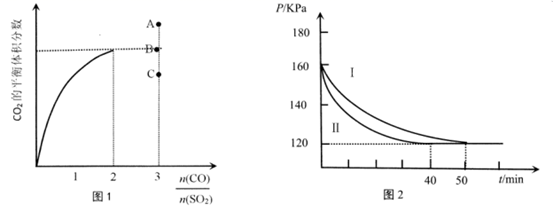
①当投料比为2时,t min 时测得SO2转化率为50%,则用S的生成速率表示的反应速率v=g·min-1。
②当投料比为3时,CO2 的平衡体积分数对应的点是。
-
(3) 向体积均为1L的恒温、恒客密团容器通入2 mol CO和| mol SO2。反应体系总压强随时间的变化如图:
①相对于I,II改变的外界条件是。
②SO2的平衡转化率为,平衡常数Kp =(用平衡分压代替平衡浓度计算)。
-
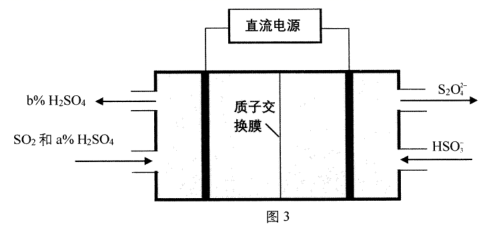
(4) 利用电解法处理SO2尾气可制备保险粉 (Na2S2O4).电解装置如图,则a b (填“>” “=”或“<”),生成S2O42-的电极反应式为。
 2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
2C(g)+2D(g),在四种不同情况下用不同物质表示的反应速率分别如下,其中反应速率最大的是( )
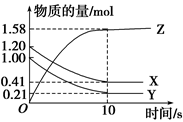
 Z(g)
Z(g)
 2P(g)+2Q(g),改变条件测得化学反应速率如下,其中能符合题意表示反应最快速率的是( )
2P(g)+2Q(g),改变条件测得化学反应速率如下,其中能符合题意表示反应最快速率的是( )
 xC(g)+2D(g),经5min后,测得D的量为1mol,C的平均反应速率是0.1mol/(L·min)。则x的值为( )
xC(g)+2D(g),经5min后,测得D的量为1mol,C的平均反应速率是0.1mol/(L·min)。则x的值为( )
①v(A)=0.45 mol·L-1·min-1
②v(B)=0.6 mol·L-1·s-1
③v(C)=0.4 mol·L-1·s-1
④v(D)=0.5 mol·L-1·s-1
下列有关反应速率的比较中正确的是
 2C(g)+2D(g)的速率如下:
2C(g)+2D(g)的速率如下: ①v(A)=0.15mol∙L-1∙s -1 ②v(B)=0.6mol∙L-1∙s -1
③v(C)=0.5mol∙L-1∙ s -1 ④v(D)=1.2 mol∙L-1∙min -1
其中反应最快的是( )
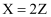 经历两步:①
经历两步:① 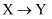 ;②
;② 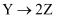 。反应体系中
。反应体系中  、
、  、
、 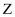 的浓度c随时间t的变化曲线如图所示。下列说法错误的是( )
的浓度c随时间t的变化曲线如图所示。下列说法错误的是( )
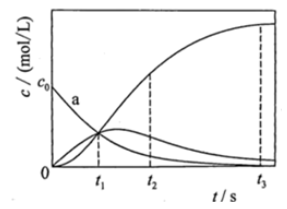
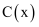 随t的变化曲线
B .
随t的变化曲线
B . 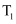 时,
时, 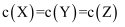 C .
C .  时,
时,  的消耗速率大于生成速率
D .
的消耗速率大于生成速率
D .  后,
后, 
 COS(g)+H2(g)+Q。
COS(g)+H2(g)+Q。完成下列填空:
-
(1) 写出H2S的结构式,它的电离方程式为。
-
(2) 若反应容器的体积为2L,反应前将10mol的CO与一定量的H2S混合加热,20秒后,达到平衡,CO变为8mol,以H2S表示速率,则v(H2S)=mol/(L•s)。
-
(3) 写出一个能表示该反应达到平衡的标志:。
-
(4) 写出一个既能增大H2S转化率,又能加快反应速率的措施:。
-
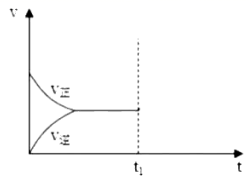
(5) 该反应在一定条件下的反应速率(v)与时间(t)的关系如图所示,若反应达到平衡时(t1时),升高温度,v正、v逆如何变化,分别用v′正、v′逆表示画在如图。
主反应: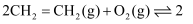
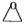 (环氧乙烷)
(环氧乙烷)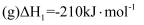
副反应: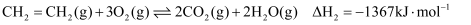
已知: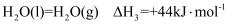
回答下列问题:
-
(1) 乙烯的燃烧热(∆H)为
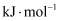 , 该反应每产生
, 该反应每产生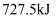 的热量,转移的电子数为
的热量,转移的电子数为 。
。
-
(2) 下列说法正确的是____(填标号)。A . 在主反应中,每消耗
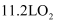 , 断裂的碳碳键数目为
, 断裂的碳碳键数目为 B . 在副反应中,每消耗
B . 在副反应中,每消耗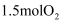 同时消耗
同时消耗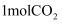 , 该反应达到平衡
C . 加入合适的催化剂,主副反应的速率均加快,乙烯的平衡转化率也增大
, 该反应达到平衡
C . 加入合适的催化剂,主副反应的速率均加快,乙烯的平衡转化率也增大
-
(3) 某温度下,在
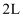 的恒容密闭容器中充入
的恒容密闭容器中充入 和
和 后,反应达到平衡,此时测得反应后的总压强与反应前的总压强之比为
后,反应达到平衡,此时测得反应后的总压强与反应前的总压强之比为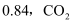 的物质的量与总物质的量的比值为
的物质的量与总物质的量的比值为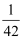 。
。①
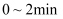 内,
内,
 。
。②
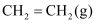 的转化率为,
的转化率为,
 。
。③反应达到平衡时,主反应的平衡常数K=(写出计算式即可)。
-
(4) 环氧乙烷经水解可得到乙二醇(C2H6O2),写出乙二醇一氧气碱性燃料电池的负极的电极反应式:。
- 如图所示,A、B两物体相距s=7m,物体A以vA=4m/s的速度向右匀速运动。而物体B此时的速度vB=10m/s,向右做
- 下列属于第一次工业革命期间出现于美国的发明的是( )①水力织布机 ②缝纫机 ③轮船 ④蒸汽机车 ⑤机器零部件的标
- 下图甲表示当B接受一定强度刺激后引起C收缩过程的示意图,乙表示图甲中A结构的放大示意图。据图分析,下列叙述正确的是:(
- 十二届全国人大常务委员会经过三次审议、二次征求民众意见,于2013年10月25日通过了《关于修改(中华人民共和国消费者权
- 下图是第二次世界大战盟军的一次重大军事行动,它使法西斯德国陷入到盟军的东西夹击之中。它是A. 莫斯科保卫战 B.
- 发生地震时,被困在建筑物废墟中的人向外界求救的办法之一是用石块敲击铁管,这是利用声音可以在 ________(填“固体”
- 阅读下面的作品,完成后面题目。 于是之 陈丹青 北京人民艺术剧院,总算没拆,模样,也还大致没变。前年去看了场话剧《阮玲玉
- American cities are similar to other cities around the world
- 关于俄罗斯港口和城市的叙述,正确的是() A. 符拉迪沃斯托克是北冰洋沿岸的主要海港 B. 摩尔曼克斯是太平洋沿岸的主要
- 单项选择 There will be a school sportsmeet ____a week. A
- 设集合则= A.[0.1) B.[0,1] C. D.
- 据调查,旅游黄金周到青岛来旅游的游客大多来自山东省的各地市及周边省市,这说明旅游资源具有有限的 A.环境
- 花生有大花生和小花生两个品种,以下说法正确的是 A.决定花生大小品种的主要因素是土壤的肥沃程度 B.大花生中最小的种子也
- 不等式|x+2|+|x-1|<4的解集是()A.(-2,1) B.[-2,1]
- 下图是植物组织培养流程图,据图回答问题:(1)A过程是 ,B、C过程是 。(
- NA为阿伏加德罗常数,下列说法正确的是 ( ) A.标准状况下,11.2
- .“(美利坚合众国)在邦联时期,国内经济濒临崩溃,债台高筑,人民的生活陷于困境,终于激起了谢斯起义;外部的英、法、西等国
- Li-Al/F eS电池是一种正在开发的车载电池,该电池中正极的电极反应式为:2Li++FeS+2e-===Li2S+
- 已知反比例函数y=kx(k是常数,k≠0)的图象在第一、三象限,请写出符合上述条件的k的一个值:.
- 罗马城内有架“圣梯”,凡人只要爬上去便可赎罪。一天,有人爬到中间,又突然退了下来,旁人问其原因,他说:“只要心中有了信仰



