活化能及其对化学反应速率的影响 知识点题库
化学反应 | 催化剂 | Ea/KJ•mol-1 | k(催)或k(无) | |
无催化剂 | 有催化剂 | |||
C12H22O11(蔗糖)+H2O═C6H12O6 (葡萄糖)+C6H12O6(果糖) | 蔗糖酶 | 107 | 36 | 9.2×1011(310K) |
2HI═H2+I2 | 金 | 184 | 105 | 1.6×108(503K) |
CH3CHO═CH4+CO | 碘 | 210 | 136 | 7.5×104(793K) |
2H2O2═2H2O+O2 | 过氧化氢酶 | 75 | 25 | 5.8×108(298K) |
请根据表中数据分析:催化剂能 化学反应速率(“加快”或“减小’),催化剂是通过参与反应改变反应历程, 来提高化学反应的平衡常数, 改变平衡转换率.
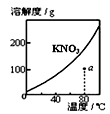 表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B . 图
表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B . 图 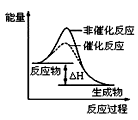 表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C . 图
表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C . 图 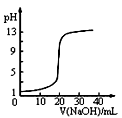 表示0.1000mol•L—1NaOH溶液滴定20.00mL0.1000mol•L—1醋酸溶液的滴定曲线
D . 图
表示0.1000mol•L—1NaOH溶液滴定20.00mL0.1000mol•L—1醋酸溶液的滴定曲线
D . 图 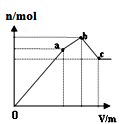 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
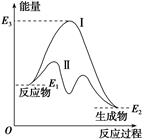
-
(1) 该反应是(填“放热”或“吸热”)反应。
-
(2) 该反应的ΔH=。
-
(3) 使用催化剂(填“能”或“不能”)影响该反应的反应热。
-
(4) 逆反应的活化能可表示为。
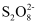 和I-的混合溶液中,反应
和I-的混合溶液中,反应 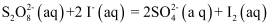 的催化机理和反应进程中的能量变化如下:
的催化机理和反应进程中的能量变化如下: 步骤①: 2Fe3+(aq)+2I-(aq)=I2(aq)+2Fe2+ (aq)
步骤②: 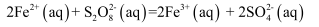
下列有关该反应说法错误的是( )
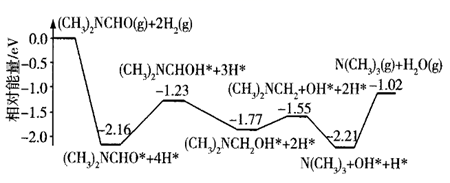
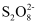 的总能量高于2mol Fe3+和 2mol
的总能量高于2mol Fe3+和 2mol  的总能量
的总能量
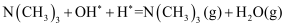 是该反应历程的决速步
C . 使用铜作催化剂可以降低反应的活化能,从而改变反应的焓变
D . 该历程中最大能垒(活化能)E正=2.16 eV
是该反应历程的决速步
C . 使用铜作催化剂可以降低反应的活化能,从而改变反应的焓变
D . 该历程中最大能垒(活化能)E正=2.16 eV
已知:N2(g)+O2(g)⇌2NO(g) ΔH1=+180.0kJ·mol-1
N2(g)+3H2(g)⇌2NH3(g) ΔH2=-92.4kJ·mol-1
H2的燃烧热为285.8kkJ·mol-1。
回答下列问题:
-
(1) 写出NO与NH3反应生成N2和液态水的热化学方程式。
-
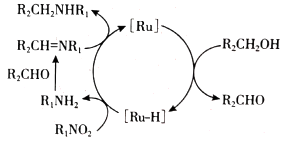
(2) 研究者用负载Cu的ZSM-5分子筛作催化剂对NO催化分解,M表示催化剂表面活性中心,对该反应提出如下反应机理。分解产生的O2浓度增大易占据催化剂活性中心M。
I:NO+M→NO-M 快;
II:2NO-M→N2+2O-M 慢;
III:20-M⇌O2+2M 快。
三个反应中,活化能较高的是(填“I”、“II”或“III”);反应要及时分离出O2其目的是。
-
(3) 一密闭容器中,加入1molN2、3molH2发生反应:N2(g)+3H2(g)⇌2NH3(g),t0时达到平衡,在t1、t3、t4时均只改变某一个条件,如图是某一时间段中反应速率与反应进程的曲线关系图。
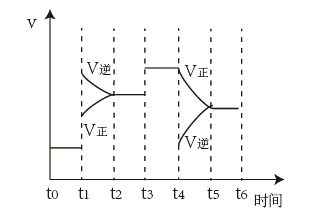
①t1、t3时改变的条件分别是、。
②下列时间段中,氨的百分含量最低的是(填标号)。
a.t0~t1 b.t2~t3 c.t3~t4 d.t5-t6
③在恒温密闭容器中,进料浓度比c(H2):c(N2)分别等于3:2、3:1、7:2时N2平衡转化率随体系压强的变化如下图所示:
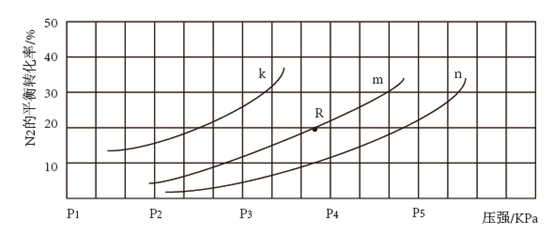
表示进料浓度比c(H2):c(N2)=7:2的对应曲线是(填标号),设R点c(NH3)=xmol/L,则化学平衡常数K=(列出计算式)。
-
(1) 工业上在
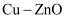 催化下利用CO2发生如下反应I生产甲醇,同时伴有反应II发生。
催化下利用CO2发生如下反应I生产甲醇,同时伴有反应II发生。 I.

II.
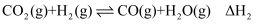
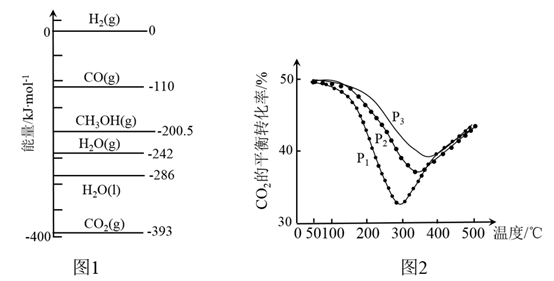
①已知:298 K时,相关物质的相对能量如图1,反应I的△H1为。
②不同条件下,按照n(CO2):n(H2)=1:1投料,CO2的平衡转化率如图2所示。
压强p1、p2、p3由大到小的顺序是。压强为p1时,温度高于300℃之后,随着温度升高CO2平衡转化率增大的原因。
③在温度T时,在容积不变的密闭容器中,充入0.5 mol CO2(g)和1.0 mol H2(g),起始压强为p kPa,10 min达平衡时生成0.3 mol H2O(g),测得压强为
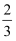 p kPa。
p kPa。若反应速率用单位时间内分压变化表示,则10 min内CH3OH的反应速率v(CH3OH)为
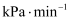 。则反应Ⅰ的平衡常数Kp=
。则反应Ⅰ的平衡常数Kp= 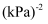 (写出Kp的计算式)。
(写出Kp的计算式)。 -
(2) 甲醇催化制取内烯的过程中发生如下反应:
I.

II.

反应Ⅰ的
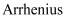 经验公式的实验数据如图3中曲线a所示,已知
经验公式的实验数据如图3中曲线a所示,已知 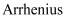 经验公式为
经验公式为  (
(  为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=kJ/mol。当改变外界条件时,实验数据如图3中的曲线b所示,则实验可能改变的外界条件是。
为活化能,k为速率常数,R和C为常数)。则该反应的活化能Ea=kJ/mol。当改变外界条件时,实验数据如图3中的曲线b所示,则实验可能改变的外界条件是。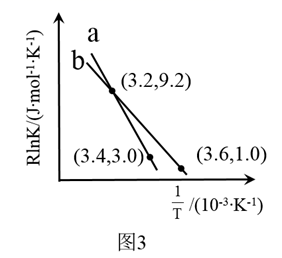
 )在紫外线的作用下可解离出氯原子,氯原子破坏臭氧层的原理如图所示,下列有关说法中正确的是( )
)在紫外线的作用下可解离出氯原子,氯原子破坏臭氧层的原理如图所示,下列有关说法中正确的是( ) 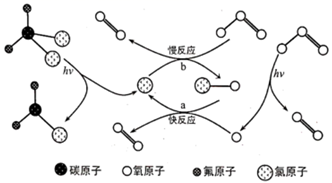
 D . 氟利昂分子的空间构型是正四面体形
D . 氟利昂分子的空间构型是正四面体形
①CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH1=- 53.7 kJ/mol
CH3OH(g)+H2O(g) ΔH1=- 53.7 kJ/mol
②CO2(g)+H2(g)  CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
CO(g)+H2O(g) ΔH2=+41.2 kJ/mol
在恒压、反应物起始物质的量比n(CO2)∶n(H2)=1∶2.2条件下,相同反应时间测得的实验数据如下:
| 实验编号 | T(K) | 催化剂 | CO2转化率(%) | 甲醇产率(%) |
| 1 | 543 | 催化剂a | 12.3 | 5.2 |
| 2 | 543 | 催化剂b | 10.9 | 7.9 |
| 3 | 553 | 催化剂a | 15.3 | 6.0 |
| 4 | 553 | 催化剂b | 12.0 | 8.6 |
下列有关说法正确的是 ( )
 和
和  合成甲醇(
合成甲醇(  )。
)。
-
(1) 利用
 和
和  反应合成甲醇时发生两个平行反应:
反应合成甲醇时发生两个平行反应: 反应Ⅰ
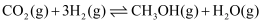
反应Ⅱ
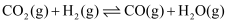
控制
 和
和  初始投料比为
初始投料比为 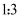 ,温度对
,温度对  平衡转化率及甲醇和
平衡转化率及甲醇和  产率的影响如图所示:
产率的影响如图所示: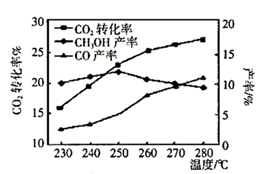
①反应Ⅰ能自发的反应条件:。(填“低温”、“高温”、“任何温度”)
②由图可知温度升高
 的产率上升,其主要原因可能是。
的产率上升,其主要原因可能是。③由图可知获取
 最适宜的温度是。
最适宜的温度是。④控制
 和
和  初始投料比为
初始投料比为 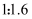 ,在
,在 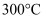 时反应Ⅰ已达到平衡状态,
时反应Ⅰ已达到平衡状态,  的转化率为
的转化率为 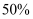 ,甲醇选择性为
,甲醇选择性为 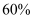 ,此时容器的体积为
,此时容器的体积为 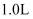 ,若
,若  初始加入量为
初始加入量为 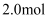 ,则反应Ⅰ的平衡常数是。(甲醇的选择性:转化的
,则反应Ⅰ的平衡常数是。(甲醇的选择性:转化的  中生成甲醇的百分比)
中生成甲醇的百分比) -
(2) 利用
 和
和  在一定条件下亦可合成甲醇,发生如下反应:
在一定条件下亦可合成甲醇,发生如下反应: 反应Ⅲ
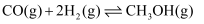
其两种反应过程中能量的变化曲线如图中a、b所示,下列说法正确的是______。
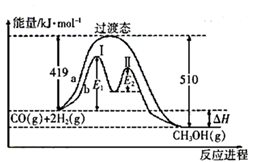 A . 上述反应的
A . 上述反应的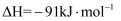 B .
B .  反应正反应的活化能为
反应正反应的活化能为 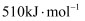 C .
C .  过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D .
过程中第Ⅰ阶段为吸热反应,第Ⅱ阶段为放热反应
D .  过程使用催化剂后降低了反应的活化能和
过程使用催化剂后降低了反应的活化能和 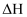 E .
E .  过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
过程的反应速率:第Ⅱ阶段>第Ⅰ阶段
-
(3) 甲和乙两个恒容密闭容器的体积相同,向甲中加入
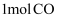 和
和 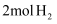 ,向乙中加入
,向乙中加入 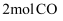 和
和 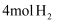 ,发生反应Ⅲ,测得不同温度下甲中
,发生反应Ⅲ,测得不同温度下甲中  的平衡转化率如图所示,请在图中画出不同温度下乙容器中
的平衡转化率如图所示,请在图中画出不同温度下乙容器中  的平衡转化率变化趋势的曲线。
的平衡转化率变化趋势的曲线。 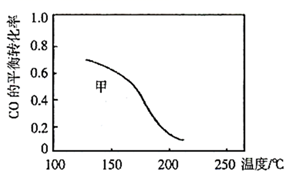
-
(4) 反应Ⅰ生成的甲醇常用作燃料电池的原料,请写出以甲醇、空气、氢氧化钾溶液为原料,石墨为电极构成的燃料电池的负极电极方程式。
途径Ⅰ: 
途径Ⅱ:在N2O中加入少量碘蒸气
① 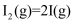 (快反应)
(快反应)
② 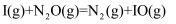 (慢反应)
(慢反应)
③  (快反应)
(快反应)
下列表述错误的是( )
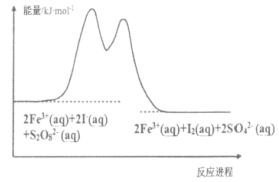
 2SO3(g),反应过程中能量的变化如图所示。
2SO3(g),反应过程中能量的变化如图所示。

-
(1) 由图可知该反应的正反应为(填“吸热”或“放热”)反应。
-
(2) 向反应体系中加入催化剂后,图中E1(填“增大”“减小”或“不变”,下同),E3。
-
(3) 已知:2H2S(g)+O2(g)=2S(s)+2H2O(g) △H=-442.4kJ•mol-1;
S(s) +O2 (g)=SO2 (g) △H=-297.0kJ•mol-1。
则H2S(g)与O2(g)反应产生SO2(g)和H2O(g)的热化学方程式是。
 、
、 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:Ⅰ. 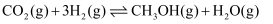
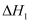
Ⅱ. 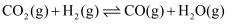
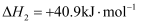
回答下列问题:
-
(1) 已知
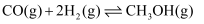
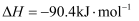 , 请计算
, 请计算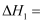 。
。
-
(2) 在恒温恒容的容器中发生上述反应,下列说法正确的有____。A . 气体平均摩尔质量保持不变,反应体系已达平衡 B . 加入催化剂,可提高
 的平衡转化率
C . 平衡后缩小体积增大体系压强,有利于提高
的平衡转化率
C . 平衡后缩小体积增大体系压强,有利于提高 产率
D . 平衡后升高温度,反应Ⅱ的正反应速率增大、逆反应速率减小,平衡正移
产率
D . 平衡后升高温度,反应Ⅱ的正反应速率增大、逆反应速率减小,平衡正移
-
(3) 研究表明:其他条件相同的情况下,用新型催化剂可以显著提高甲醇的选择性。使用该催化剂,将
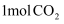 和
和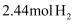 在
在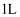 密闭容器中进行反应,
密闭容器中进行反应, 的平衡转化率和甲醇的选择率(甲醇的选择率:转化的
的平衡转化率和甲醇的选择率(甲醇的选择率:转化的 中生成甲醇的物质的量分数)随温度的变化趋势如图所示:
中生成甲醇的物质的量分数)随温度的变化趋势如图所示: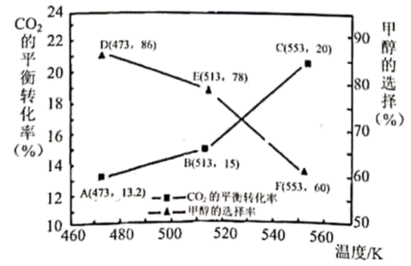
①温度为
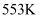 , 经
, 经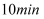 体系达到平衡,则
体系达到平衡,则 的平均反应速率为,该温度下反应Ⅰ的平衡常数
的平均反应速率为,该温度下反应Ⅰ的平衡常数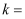 。
。②随着温度的升高,
 的平衡转化率增加但甲醇的选择率降低,分析其原因。
的平衡转化率增加但甲醇的选择率降低,分析其原因。 -
(4) 研究表明,在电解质水溶液中,
 可以被电化学还原。两种不同催化剂
可以被电化学还原。两种不同催化剂 、
、 上
上 电还原为
电还原为 的反应进程中(溶液中
的反应进程中(溶液中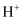 被还原为
被还原为 的反应也同时发生)相对能量变化如图。由此判断,电解质溶液中主要发生
的反应也同时发生)相对能量变化如图。由此判断,电解质溶液中主要发生 还原为
还原为 反应的是(填
反应的是(填 或
或 ),理由是。
),理由是。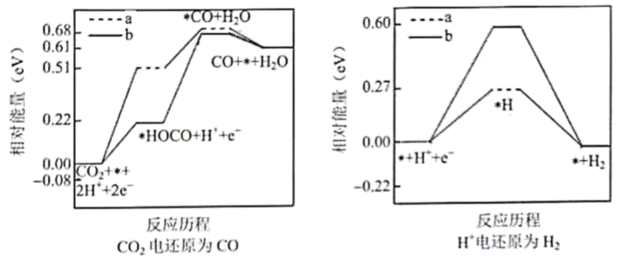
选项 | 科技成果 | 相关表述 |
A | 利用催化剂Ni2Al3实现原生生物质大分子高选择性转化成CH4 | 催化剂能降低反应活化能,提高活化分子的百分数 |
B | 在纳米Cu2O表面控制CO2电化学还原制备C2H4和合成气 | 纳米Cu2O增大了反应物的接触面积,接触面积越大,分子碰撞频率越高,反应速率越大 |
C | 首次发现烷基型产甲烷的古菌,原油有望高效转化成天然气 | 天然气、沼气的主要成分都是CH4 , 它们都是不可再生能源 |
D | 锂电池或二次电池的研究引领全球清洁能源 | 锂电池能将化学能转化成电能 |
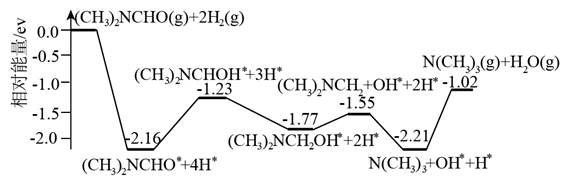
 CH3OH(g)+H2O(g)是我国科学家2021年发布的由CO2人工合成淀粉中的重要反应之一。CO2与H2制备甲醇在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的物种用*标注,TS为过渡态),下列说法正确的是( )
CH3OH(g)+H2O(g)是我国科学家2021年发布的由CO2人工合成淀粉中的重要反应之一。CO2与H2制备甲醇在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的物种用*标注,TS为过渡态),下列说法正确的是( ) 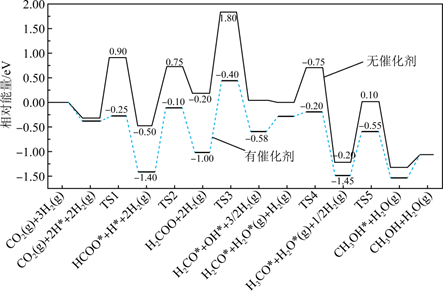
-
(1) 消除CO、NO污染物的反应机理如下[Pt(s)表示催化剂,带“*”表示吸附状态]:
I.NO+Pt(s)=NO*
II.CO+Pt(s)=CO*
III.NO*=N*+O*
IV.CO*+O*=CO2+Pt(s)
V.N*+N*=N2+Pt(s)
经测定汽车尾气中反应物浓度及生成物浓度随温度T变化关系如图一和图二所示。
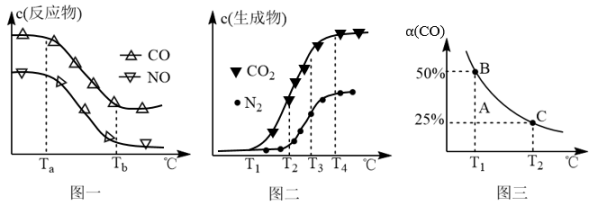
①图一中温度从Ta℃升至Tb℃的过程中,反应物浓度急剧减小的主要原因是。
②由图二知,T2℃时反应V的活化能反应IV的活化能(填“<”、“>”或“=”)。
-
(2) 为模拟汽车的“催化转化器”,将2molNO(g)和2molCO(g)充入1L密闭容器中,加入催化剂后发生反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g),测得CO的平衡转化率α随温度T变化曲线如图三所示。
①图像中A点正反应速率逆反应速率(填“>”、“=”或“<”);T1℃,下列说法能表明该反应已达到平衡状态的是(填序号)。
a.混合气体的密度不变 b.体系的压强不变
c.混合气体中N2的体积分数不变 d.2υ正(CO)=υ逆(N2)
②T1℃,该反应的化学平衡常数Kc=(mol·L-1)-1。
③T2℃时,实验测得:v正=k正·c2(NO)·c2(CO),v逆=k逆·c(N2)·c2(CO2),k正、k逆分别是正、逆反应速率常数。则T2℃时k正∶k逆=1∶。
- 下列操作符合实验要求并能达到实验目的的是 A.吸收HCl防倒
- The old man was quite weak after the accident, so he______.
- 右侧是一幅民国时期时尚女性的图画,它从一个侧面反映了民国时期在风俗文化领域出现的新变化。下列对此理解正确的是( )A.
- 某些保健品含有一定量的性激素(或性激素类似物),对青少年的发育会造成不良影响。从化学成分上分析,性激素属于( ) A
- 图1为我国某地区1951-2010年每10年的人口变化。读图,完成1-2题。1.1951-2010年,该地区 A.人口自
- 2005年,“西气东输”工程为青岛市送来了天然气。天然气的主要成分是甲烷(CH4),它是一种“清洁能源”,甲烷在空气中完
- They usually have _____ to do after school.A. lots of homewo
- 为了验证胰岛素具有降低血糖含量的作用.在设计实验时,如果以正常小鼠每次注射药物前后小鼠症状的变化为观察指标,则下列对实验
- 根据右图所示实验,不能得到的结论是A.CO2不能燃烧 B.CO2不支持燃烧C.CO2密度比空气
- 下列各组物质加入水中充分搅拌后,同组反应物恰好完全反应,过滤后,在滤纸上留下两种不溶物质的是() A.Ca(NO3)2、
- 下列关于洋务运动的表述,不正确的是 A总理衙门是洋务运动的中央机构 B兴办的军事工业和民用工业都是近代工业 C海军重要舰
- 把6mol铜粉投入含8 mol硝酸和2 mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为 A.2 mol B.3
- —Nice to meet you.---_______. A. I’m Lisa
- 已知某K-Na合金6.2 g,下列关于其物质的量的说法正确的是( )A.总物质的量为2.0 molB.总物质的量介
- 阅读下面一段文字,并按要求回答问题。(4分) 也许,我们前行的步覆总是沉重、蹒跚;也许,我们虞诚的信念总会被世俗的晨雾缭
- 28.目前,全国各级人大代表和政协委员中有党外人士50余万人,担任县处级以上领导干部职务的党外干部有3.2万人,各省、市
- 在数中任取三个相乘,其中最大的积是_________,最小的积是___________.
- 青藏铁路在广大建设者的努力下.于2006年7月1日全线胜利通车,不少游客乘坐第一列列车去西藏旅游,但刚到达青藏高原时有的
- 早在19世纪匈牙利物理学家厄缶就明确指出:“沿水平地面 向东运动的物体,其重量(即:列车的视重或列车对水平轨道的压
- 抛物线可由抛物线平移得到,则下列平移过程正确的是( ) A、先向右平移1个单位,再向上平移2个单位 B、先向右平移1



