铁的吸氧腐蚀 知识点题库
-
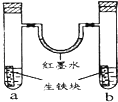
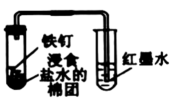
(1) 如图1所示水槽中试管内有一枚铁钉,放置数天发现试管内液面下降,则原溶液呈性,发生 (填“析氢”或“吸氧”)腐蚀,正极反应式为:.
-
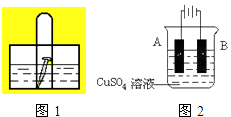
(2) 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一.在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如2:
请回答:①A电极为(写名称),B电极的电极反应式是.
②若电镀前铁、铜两电极的质量相同,电镀完成后将它们取出洗净、烘干、称量,
二者质量差为5.12g,则电镀时电路中通过的电子为 mol.
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因..
-
(3) 目前我国许多大型铜质文物露天放置腐蚀严重,在不影响观瞻效果的条件下,除用加保护层法保护外,请你再提出一项简单而有效的保护方法.
-
(1) 在潮湿空气中,钢铁发生吸氧腐蚀时的正极反应式为。
-
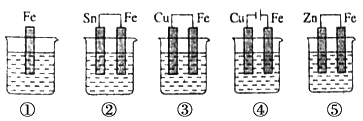
(2) 已知草酸分解的化学方程式为:H2C2O4
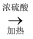 CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是。
CO↑ + CO2↑ + H2O,下列装置中,可用作草酸分解制取气体的是。 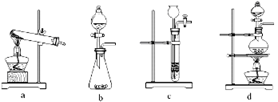
-
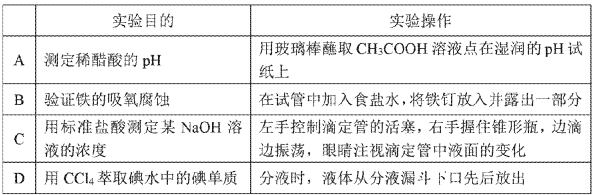
(3) 某实验小组利用草酸分解产生的CO和铁锈反应来测定铁锈样品的组成(假定铁锈中只有Fe2O3· nH2O和Fe两种成分),实验装置如下图所示。
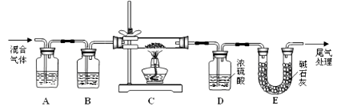
①为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次可能是、(填答案编号)。
a. 浓硫酸
b.澄清的石灰水
c. 氢氧化钠溶液
d. 无水氯化钙
②在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;(b)。
③E装置的作用是 。
④准确称量样品10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32 g,D中浓硫酸增重0.72 g,则n =。
⑤在本实验中,下列情况会使测定结果n偏大的是(填答案编号)。
a.缺少装置B
b.缺少装置E
c.反应后的固体中有少量Fe2O3·nH2O
-
(1) 检测锈蚀产物
主要成分的化学式
Fe3O4
Fe2O3·H2O
FeO(OH)
FeOCl
铁器在具有O2、等环境中容易被腐蚀。
-
(2) 分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.Fe转化为Fe2+。
Ⅱ. FeO(OH)和Fe2+反应形成致密的Fe3O4保护层,Fe2+的作用是(填字母)。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
-
(3) 研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成Fe3O4保护层,方法如下:
将铁器浸没在盛有0.5 mol·L-1 Na2SO3、0.5 mol·L-1 NaOH溶液的容器中,缓慢加热至60~90 ℃。一段时间后,取出器物,用NaOH溶液洗涤至无Cl-。
①检测洗涤液中Cl-的方法是。
②脱氯反应:FeOCl+OH-=FeO(OH)+Cl-。离子反应的本质是离子浓度的减小,比较FeOCl与FeO(OH)溶解度的大小:。
③Na2SO3还原FeO(OH)形成Fe3O4的离子方程式是SO32-+FeO(OH)=SO42-+Fe3O4+H2O(将反应补充完全)。
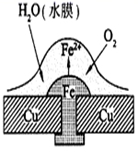
| 实验装置 | 实验编号 | 浸泡液 | pH | 氧气浓度随时间的变化 |
| | | | 5 | |
| | | 5 | ||
| | | 7 | ||
| | | 7 |
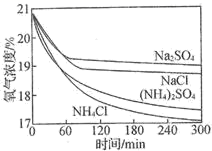
 B . 在不同溶液中,
B . 在不同溶液中,  是影响吸氧腐蚀速率的主要因素
C . 向实验
是影响吸氧腐蚀速率的主要因素
C . 向实验 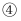 中加入少量
中加入少量 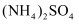 固体,吸氧腐蚀速率加快
D . 在300min内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液
固体,吸氧腐蚀速率加快
D . 在300min内,铁钉的平均吸氧腐蚀速率酸性溶液大于中性溶液
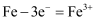 B . CH4 分子的比例模型:
B . CH4 分子的比例模型:  C . 结构示意图为
C . 结构示意图为 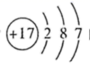 的原子,可表示为
的原子,可表示为 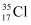 或
或 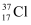 D . H2O2的电子式:
D . H2O2的电子式: | A | B | C | D |
| | | | |
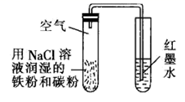
| 制取 | 验证 | 制取少量 | 检验该条件下铁发生了吸氧腐蚀 |
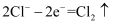 B . 酸性氢氧燃料电池正极的电极反应式:
B . 酸性氢氧燃料电池正极的电极反应式:  C . 粗铜精炼时,与电源正极相连的电极上的电极反应式:
C . 粗铜精炼时,与电源正极相连的电极上的电极反应式: 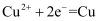 D . 钢铁发生吸氧腐蚀时,铁电极的电极反应式:
D . 钢铁发生吸氧腐蚀时,铁电极的电极反应式: 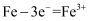
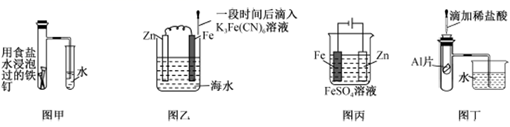
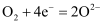 C . 原电池反应减缓了铁制品的腐蚀
D . 负极反应式:
C . 原电池反应减缓了铁制品的腐蚀
D . 负极反应式: 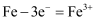
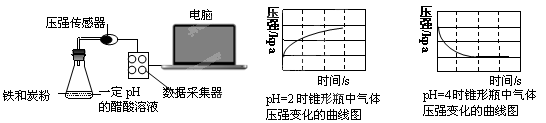
分析图像,以下结论不正确的是( )
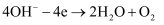
|
|
|
|
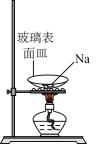
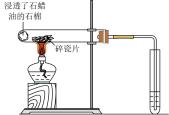
A.滴入酚酞溶液 | B.吸氧腐蚀 | C.钠的燃烧 | D.石蜡油的热分解 |
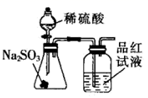
选项 | 实验目的 | 操作或装置 |
A | 除去苯中少量的苯酚 | 加入足量浓溴水后过滤 |
B | 制备 |
|
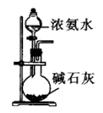
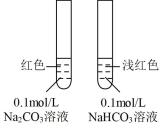
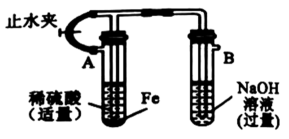
C | 验证铁钉发生了吸氧腐蚀 |
|
D | 检验麦芽糖中含有醛基 | 取样品加入新制 |
- ---Where may you advise me to start my business? ---In my op
- 下列设计方案是利用物质的化学性质达到实验目的的是 A.观察小木条燃烧情况,比较“人吸入空气和呼出气体”中氧气含量的大小B
- 所示为一块霍尔元件,其横载面为矩形,霍尔元件的长、宽、高分别为c、b、d。已知其单位体积内的电子数为n、电子电荷量e.将
- 张大爷家的小麦叶色发黄,有倒伏现象,张大爷应该给小麦施下列哪种化肥( ) A.硝酸钾 B.碳酸氢铵
- 通读下面的对话,然后根据上下文补全对话内容。A: Good afternoon, Miller! 【小题1】 ?B:
- 将一盛满Cl2的试管倒立于水槽中,当日光照射相当一段时间后,下列说法不正确的是( ) A.试管中气体颜色逐渐变浅
- 已知. (Ⅰ)求不等式的解集; (Ⅱ)若存在,使得成立,求实数的取值范围.
- 人体红细胞产生ATP的部位、所需ATP的来源、主要呼吸类型分别是() A. 线粒体;葡萄糖;有氧呼吸
- 函数的图象为C,: ①图象关于直线对称; ②函数在区间内是增函数; ③由的图象向右平移个单位长度可以得到图象. 以
- “旧时王谢堂前燕,飞入寻常百姓家”,一些本来只有少数人才买得起的高档商品,过了一段时间之后,其价格会逐渐降低,成为寻常
- —Do you have any plans for this weekend? —Yes.We will go on
- 若一个三角形的一边长为3cm,则它的周长可能为() A. 4cm B. 5cm C. 6cmD. 8cm
- 某可逆反应的正反应是放热反应,则温度对此反应的正、逆反应速率影响的曲线(如图所示)中,正确的是()
- 电脑与我们的生活联系越来越紧密,文字编辑、图片处理、上网浏览等等都离不开它。不知你是否注意,有些软件、网站的名字很有创意
- 如图2所示,C是水平地面,A、B是两个长方体物块,F是作用在物块B上沿水平方向的力,物体A和B一起加速运动.由此可见,A
- 有一列数,按一定规律排成1,-4,16,-64,256,-1 024,…,其中某三个相邻的数的和是-13 312,求这三
- 质量为 m的小车在水平恒力F推动下,从山坡底部A处由静止起运动至高为h的坡顶B,获得速度为,AB的水平距离为S。下列说法
- Della turned all of her pockets inside out only to find $ 1.
- 根据反应方程式 ① 2Fe3+ +2I― == 2Fe2+ + I2 ② 2Fe2++Br2 == 2Fe3+ +2
- 近年来,不少地方的河流被密密麻麻的水葫芦所覆盖,水葫芦泛滥成灾。下列哪项不是水葫芦泛滥的原因 A.繁殖速度快

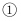

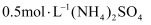
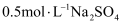
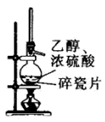
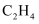
 具有漂白性
具有漂白性
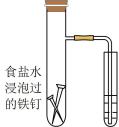
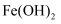
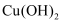 悬浊液中并加热
悬浊液中并加热


