化学用语 知识点题库
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A . CCl4的电子式: 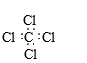 B . Cl-的结构示意图:
B . Cl-的结构示意图:  C . CO2的电子式:
C . CO2的电子式: 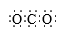 D . 质量数为37的氯原子:
D . 质量数为37的氯原子: 
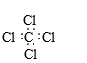 B . Cl-的结构示意图:
B . Cl-的结构示意图: 
化学与人类生产、生活密切相关,下列有关说法错误的是( )
A . “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化
B . 将“地沟油”变废为宝,可制成生物柴油和肥皂
C . 水泥冶金厂常用高压电除去工厂烟尘,利用了胶体的性质
D . 用活性炭为糖浆脱色和用SO2漂白纸浆的原理不同
LiAlH4和LiH既是金属储氢材料又是有机合成中的常用试剂。它们遇水均能剧烈反应释放出H2 , LiAlH4在125℃时分解为LiH、H2和Al。下列说法不正确的是( )
A . LiAlH4中AlH4-的结构式可表示为: 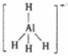 B . 1 mol LiAlH4在125℃完全分解,转移3 mol电子
C . LiAlH4与乙醛作用生成乙醇,LiAlH4作氧化剂
D . LiAlH4溶于适量水得到无色溶液,其反应可表示为:LiAlH4+2H2O=LiAlO2+4H2↑
B . 1 mol LiAlH4在125℃完全分解,转移3 mol电子
C . LiAlH4与乙醛作用生成乙醇,LiAlH4作氧化剂
D . LiAlH4溶于适量水得到无色溶液,其反应可表示为:LiAlH4+2H2O=LiAlO2+4H2↑
 B . 1 mol LiAlH4在125℃完全分解,转移3 mol电子
C . LiAlH4与乙醛作用生成乙醇,LiAlH4作氧化剂
D . LiAlH4溶于适量水得到无色溶液,其反应可表示为:LiAlH4+2H2O=LiAlO2+4H2↑
B . 1 mol LiAlH4在125℃完全分解,转移3 mol电子
C . LiAlH4与乙醛作用生成乙醇,LiAlH4作氧化剂
D . LiAlH4溶于适量水得到无色溶液,其反应可表示为:LiAlH4+2H2O=LiAlO2+4H2↑
下列属于碱性氧化物的是( )
A . Mn2O7
B . Al2O3
C . Na2O2
D . CaO
X、Y、Z、W、Q、R 是周期表中前 36 号元素,核电荷数依次增大,其中 X、Y、Z、 W 都是元素周期表中短周期元素。X 为非金属元素,且 X 原子的核外成对电子数是未成对电子数的 2 倍,Z 的次外层电子数是最外层电子数的  ,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。
回答下列问题:
,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。
回答下列问题:
 ,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。
回答下列问题:
,W 原子的 s 电子与 p 电子数相等,Q 是前四周期中电负性最小的元素,R 的原子序数为 29。
回答下列问题:
-
(1) X的最高价氧化物对应的水化物分子中,中心原子采取杂化。
-
(2) 化合物 XZ 与 Y 的单质分子互为,1mol XZ 中含有π键的数目为。
-
(3) W 的稳定离子核外有种运动状态的电子。W元素的第一电离能比其同周期 相邻元素的第一电离能高,其原因是:。
-
(4) Q 的晶体结构如图所示,则在单位晶胞中 Q 原子的个数为,晶体的配位数是。
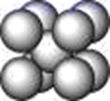
-
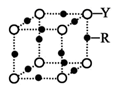
(5) R元素的基态原子的核外电子排布式为;Y 与 R 形成某 种化合物的晶胞结构如图所示,已知该晶体的密度为ρg·cm-3 , 阿伏加德罗常数的数值为 NA , 则该晶体中 R 原子和 Y 原子之间的最短距离为cm。(只写计算式)
下列离子方程式中,正确的是( )
A . 小苏打溶液与少量澄清石灰水混合:Ca2++OH-+  =CaCO3↓+H2O
B . AlCl3溶液中加入足量的氨水:Al3++4OH-=
=CaCO3↓+H2O
B . AlCl3溶液中加入足量的氨水:Al3++4OH-=  +2H2O
C . 将氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+
D . 钠与水反应:2Na + 2H2O = 2Na++ 2OH-+ H2↑
+2H2O
C . 将氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+
D . 钠与水反应:2Na + 2H2O = 2Na++ 2OH-+ H2↑
 =CaCO3↓+H2O
B . AlCl3溶液中加入足量的氨水:Al3++4OH-=
=CaCO3↓+H2O
B . AlCl3溶液中加入足量的氨水:Al3++4OH-=  +2H2O
C . 将氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+
D . 钠与水反应:2Na + 2H2O = 2Na++ 2OH-+ H2↑
+2H2O
C . 将氯气通入水中:Cl2+H2O=Cl-+ClO-+2H+
D . 钠与水反应:2Na + 2H2O = 2Na++ 2OH-+ H2↑
现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱:④二氧化碳;⑤葡萄糖:⑥氢氧化钾;⑦氢氧化铁胶体;⑧氨水;⑨空气;⑩硫酸铁溶液
-
(1) 上述十种物质中,属于电解质的有(填序号),属于非电解质的有(填序号)
-
(2) 除去③中少量②的操作是,化学方程式为;
-
(3) 现有100mL溶液中含Fe3+5.6g,则溶液中
 的物质的量浓度是;
的物质的量浓度是;
-
(4) 若在⑦中缓慢加入①的水溶液,产生的现象是。
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A . H2O的电子式: 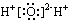 B . 乙炔的结构简式:HC≡CH
C . CH4分子的比例模型:
B . 乙炔的结构简式:HC≡CH
C . CH4分子的比例模型: 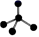 D . Cl-的结构示意图:
D . Cl-的结构示意图: 
下列化学用语表达正确的是( )
A . CH4分子的空间填充模型:  B . 氟原子的结构示意图:
B . 氟原子的结构示意图:  C . 具有6个质子和8个中子的核素符号:
C . 具有6个质子和8个中子的核素符号:  C
D . 乙烯的官能团:C=C
C
D . 乙烯的官能团:C=C
 C
D . 乙烯的官能团:C=C
C
D . 乙烯的官能团:C=C
“天问一号”着陆火星,“嫦娥五号”采回月壤。腾飞中国离不开化学,长征系列运载火箭使用的燃料有液氢和煤油等化学品。下列有关说法正确的是( )
A . 煤油是可再生能源
B .  燃烧过程中热能转化为化学能
C . 火星陨石中的
燃烧过程中热能转化为化学能
C . 火星陨石中的  质量数为20
D . 月壤中的
质量数为20
D . 月壤中的  与地球上的
与地球上的  互为同位素
互为同位素
 燃烧过程中热能转化为化学能
C . 火星陨石中的
燃烧过程中热能转化为化学能
C . 火星陨石中的  质量数为20
D . 月壤中的
质量数为20
D . 月壤中的  与地球上的
与地球上的  互为同位素
互为同位素
下列反应的离子方程式书写正确的是( )
A . Al与稀硫酸反应:Al + 2H+= Al3+ + H2↑
B . Na与水反应:Na + H2O = Na+ + OH- + H2↑
C . BaCl2溶液和Na2SO4溶液反应:Ba2++ SO  =BaSO4↓
D . CaCO3与盐酸反应:CO
=BaSO4↓
D . CaCO3与盐酸反应:CO 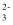 +2H+= H2O +CO2↑
+2H+= H2O +CO2↑
 =BaSO4↓
D . CaCO3与盐酸反应:CO
=BaSO4↓
D . CaCO3与盐酸反应:CO 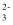 +2H+= H2O +CO2↑
+2H+= H2O +CO2↑
下列关于物质分类的符合题意组合是( )
| 选项 | 碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 |
| A | 苛性钾 | 硫酸 | 小苏打 | 生石灰 | 干冰 |
| B | 苛性钠 | 盐酸 | 食盐 | 氧化钠 | 一氧化碳 |
| C | 碱石灰 | 冰醋酸 | 胆矾 | 氧化镁 | 二氧化硫 |
| D | 纯碱 | HNO3 | 碳酸钙 | 氧化铁 | SO3 |
A . A
B . B
C . C
D . D
只能表示一个化学反应的离子方程式是( )
A .  B .
B .  C .
C . 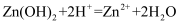 D .
D . 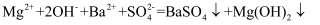
 B .
B .  C .
C . 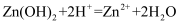 D .
D . 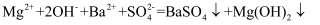
铬系和非铬系铜镍电镀污泥均含有Cu(Ⅱ)、Ni(Ⅱ)、Fe(Ⅱ)、Al(Ⅲ)的氢氧化物,前者还含有Cr(Ⅲ)的氢氧化物,一种综合回收铜、镍的新工艺流程如下:

已知:
Ⅰ、FePO4、CrPO4、AlPO4、Ni3(PO4)2的Ksp依次为1.3×10−22、2.4×10−23、5.8×10−19、5.0×10−31。
Ⅱ.Cr及其化合物的性质与铝类似。
回答下列问题:
-
(1) “电解Ⅰ”时,需严格控制电压,除了回收铜之外,第二个目的是,可通过一种试剂证明第二个目的是否达成,该试剂为(填化学式)。
-
(2) “除杂”时,若镍离子浓度为0.05mol·L−1 , 则应调整溶液中PO
 浓度范围为 mol·L−1 (溶液中离子浓度≤10-5mol·L−1时,认为该离子沉淀完全;
浓度范围为 mol·L−1 (溶液中离子浓度≤10-5mol·L−1时,认为该离子沉淀完全;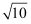 =3.2)。
=3.2)。
-
(3) “转溶”时,氢氧化钠加入量不宜过多,其原因为(用离子方程式表示)。
-
(4) “浸出Ⅱ”时,采取了多次浸取的方式,其目的为。
-
(5) “萃取Ⅱ”时,发生的反应为Cu(NH3)
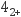 +2HR=CuR2+2NH
+2HR=CuR2+2NH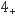 +2NH3和Ni(NH3)
+2NH3和Ni(NH3)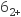 +2HR=NiR2+2NH
+2HR=NiR2+2NH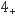 +4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为。
+4NH3和,则“反萃取Ⅱ”时含铜微粒发生反应的离子方程式为。
-
(6) “电解Ⅱ”时,若维持电流强度为0.5A,电流效率为90%,电解8min,理论上可获得铜g.(已知:电流效率是指电解时电极上实际沉积与理论沉积物质的量之比,F=96500C·mol-1)
-
(7) 流程中除了有机相之外,可以循环利用的物质还有(填化学式)。
下列有关化学用语表达正确的是( )
A . 四氯化碳的球棍模型: B . 次氯酸的电子式:
B . 次氯酸的电子式: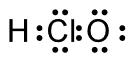 C . 质子数为35、中子数为45的溴原子:
C . 质子数为35、中子数为45的溴原子: Br
D . S2-的结构示意图:
Br
D . S2-的结构示意图: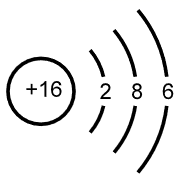
 B . 次氯酸的电子式:
B . 次氯酸的电子式: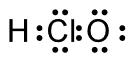 C . 质子数为35、中子数为45的溴原子:
C . 质子数为35、中子数为45的溴原子: Br
D . S2-的结构示意图:
Br
D . S2-的结构示意图:
下列关于新冠病毒说法不正确的是( )
A . 含有病毒的飞沫分散在空气中形成的分散系为气溶胶
B . N95口罩所使用的聚丙烯材料属于天然纤维
C . 用于盛装新冠疫苗的中硼硅玻璃管属于硅酸盐材质,既耐低温,又耐强酸
D . 用电解食盐水制取的次氯酸钠喷洒房间能杀死新冠肺炎病毒
下列有关说法正确的是( )
A . 使用广泛pH试纸测量“84”消毒液的pH
B . 反应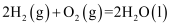 在一定条件能自发进行的原因是
在一定条件能自发进行的原因是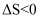 C . 常温下,将稀
C . 常温下,将稀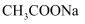 溶液加水稀释后,恢复至原温度,pH减小、
溶液加水稀释后,恢复至原温度,pH减小、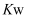 不变
D . 常温下,向
不变
D . 常温下,向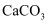 悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小
悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小
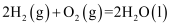 在一定条件能自发进行的原因是
在一定条件能自发进行的原因是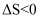 C . 常温下,将稀
C . 常温下,将稀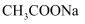 溶液加水稀释后,恢复至原温度,pH减小、
溶液加水稀释后,恢复至原温度,pH减小、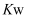 不变
D . 常温下,向
不变
D . 常温下,向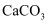 悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小
悬浊液中加入少量水,所得新悬浊液中c(Ca2+)减小
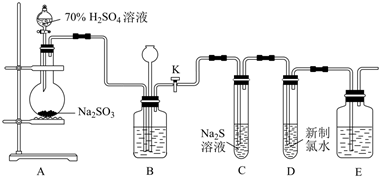
实验室可用下列装置(部分夹持仪器略去)制取SO2并验证其性质。
-
(1) 检查装置A、B气密性的操作为:先关闭装置A中分液漏斗活塞和装置B中止水夹K,往长颈漏斗中注水至水柱高于广口瓶液面,若观察到,则气密性良好。
-
(2) 装置A中反应的化学方程式为。
-
(3) 实验时,通气一段时间后,C中试管中出现大量淡黄色浑浊现象,证明二氧化硫具有(填“还原性”、“氧化性”或“漂白性”)。
-
(4) 取少量试管D中的溶液,加入BaCl2溶液,产生白色沉淀。
①该白色沉淀为(写化学式)
②原试管D中反应的离子方程式为。
-
(5) 用如图所示装置验证H2SO3酸性比H2CO3强。

请从下列试剂中选择合适试剂以完成实验(要求:试剂不重复,填代号):
a.品红溶液 b.酸性KMnO4溶液 c.饱和NaHCO3溶液 d.饱和Na2CO3溶液
X为,Y为,Z为。
下列说法正确的是( )
A .  与
与 互为同位素
B .
互为同位素
B .  与
与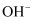 具有相同的质子数和电子数
C . 原子最外层电子数是2的元素一定处于IIA族
D . 最外层电子数比次外层电子数多的元素一定位于第2周期
具有相同的质子数和电子数
C . 原子最外层电子数是2的元素一定处于IIA族
D . 最外层电子数比次外层电子数多的元素一定位于第2周期
 与
与 互为同位素
B .
互为同位素
B .  与
与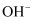 具有相同的质子数和电子数
C . 原子最外层电子数是2的元素一定处于IIA族
D . 最外层电子数比次外层电子数多的元素一定位于第2周期
具有相同的质子数和电子数
C . 原子最外层电子数是2的元素一定处于IIA族
D . 最外层电子数比次外层电子数多的元素一定位于第2周期
回收钴废料能有效缓解金属资源浪费、环境污染等问题。一种以含钴催化剂废料(主要含Co、Fe,还含有少量的CoO、FeO、 、CaO、
、CaO、 )制备氧化钴(Co2O3)的工艺流程如下图所示:
)制备氧化钴(Co2O3)的工艺流程如下图所示:
 、CaO、
、CaO、 )制备氧化钴(Co2O3)的工艺流程如下图所示:
)制备氧化钴(Co2O3)的工艺流程如下图所示: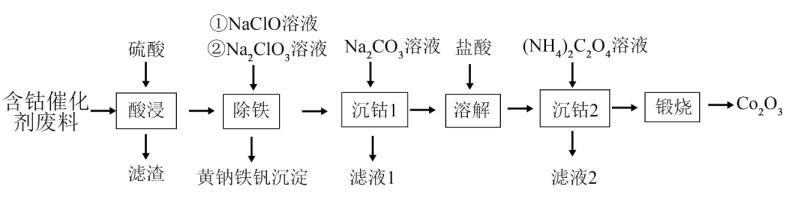
已知:i.金属钴与铁具有相似的化学性质;
ii.氧化性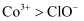 。
。
回答下列问题:
-
(1) 酸浸后,“滤渣”的主要成分有和(填化学式)。
-
(2) 基态钴原子的价电子排布式为。
-
(3) 已知CoO的熔点(1785℃)高于FeO的熔点(1369℃),其原因是。
-
(4) “除铁”时加入NaClO,主要反应的离子方程式为,再加入
 溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
-
(5)
 中N原子的杂化轨道类型为。
中N原子的杂化轨道类型为。 中除氢元素外,其他元素电负性由大到小的顺序为。
中除氢元素外,其他元素电负性由大到小的顺序为。
-
(6) “滤液2”中主要溶质的常见用途为。
-
(7) 所得
 可用于合成钓酸钴。一种钛酸钴的晶胞结构如图所示,该晶胞中与Co距离最近的O的数目为个。设
可用于合成钓酸钴。一种钛酸钴的晶胞结构如图所示,该晶胞中与Co距离最近的O的数目为个。设 为阿伏加德罗常数的值,该钛酸钴晶体的密度为
为阿伏加德罗常数的值,该钛酸钴晶体的密度为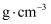 (列出计算式)。
(列出计算式)。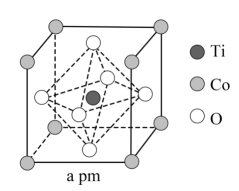
最近更新
- 已知盒中有3只螺口与7只卡口灯泡,这些灯泡的外形与功率都相同且灯口向下放着,现需用一只卡口灯泡,电工师傅每次从中任取一只
- 下列各句中,没有语病的一项是(3分) ( ) A.人类能从地面利用雷达和望远镜观测的太空碎片大约是13
- 现在城市的高楼楼身外表多镶嵌着大幅平板玻璃,小东一次经过十字路口,如图甲所示,路口右侧楼房上嵌有面对正西南的大平板玻璃,
- 已知扇形的半径为2cm,面积是,则扇形的弧长是 cm,扇形的圆心角为
- 在平面直角坐标系中,若不等式组(a为常数)所表示的平面区域的面积等于2,则a的值为
- 阅读下面语段,按要求回答问题: 美貌的人并不都有其他方面的才能。因为造物主是吝啬的,他给了此就不再予彼。所以许多容颜俊秀
- The human body isdesigned to move. But modern lifestyles and
- 已知之间满足 (1)方程表示的曲线经过一点,求b的值 (2)动点(x,y)在曲线(b>0)上变化,求x2+2y的
- 硼酸晶体成片状,有滑腻感,可作润滑剂,硼酸分子结构可表示为。硼酸对人体的受伤组织有缓和的防腐作用,故可用于医药和食品防腐
- 下图中的三股潮流组成了l9世纪世界历史的基本内容,引发这三股潮流的最主要因素是( ) A.工业革命 B.新航路的开辟
- 直线与圆相交于M、N两点,若的取值范围是 ( ) A. B. C. D.
- 下列疾病中属于遗传病的是:A.艾滋病B.流感行性感冒C.乙型肝炎D.血友病
- 在台湾漫画家几米《向左走,向右走》的漫画中,在50s的时间内,男孩提着重15N的小提琴水平向左匀速走了100m,女孩用5
- 人坐在顺流而下的船里,如果以 为参照物,则人是静止的;如果以 为参照物,则人是运动的;如果以船为
- 维新变法运动在十九世纪末之民以能取代洋务运动在中国政治舞台上出现,根本原因是( )A、洋务运动没有使中国走上富强之路
- 13.参与高等植物有丝分裂的细胞器是 ①线粒体 ②核糖体 ③高尔基体 ④中心体 ⑤内质网 A.①③
- 谷物中含量最丰富的多糖是( ) A.糖原和纤维素 B.蔗糖和麦芽糖 C.淀粉和纤维素 D.淀粉
- 若2-a,则a的取值范围是 ( )A.a=2B.a>2C.a≥2D.a≤2
- 在“探究小车速度随时间的变化规律”实验中,小车拖纸带运动,打点计时器在纸带上打出一系列点,从中确定四个计数点,每相邻两个
- 判断题:1.“虽然是满月,天上却有一层淡淡的云,所以不能朗照;但我以为这恰是到了好处——酣眠固不可少,小睡也别有风味”中



