以氯碱工业为基础的化工生产简介 知识点题库
如下图是工业电解饱和食盐水的装置示意图,下列有关说法中不正确的是( )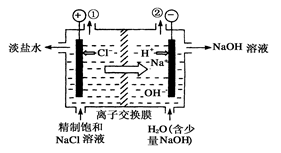
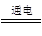 H2↑+Cl2↑+2OH-
D . 该装置是将电能转化为化学能
H2↑+Cl2↑+2OH-
D . 该装置是将电能转化为化学能
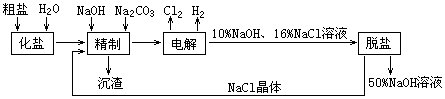
(1)工业食盐中含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为 .
(2)如果粗盐中SO42-含量较高,必须添加钡试剂除去,该钡试剂可以是 (选填a、b、c). a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(3)为了有效地除去Ca2+、Mg2+、SO42- , 加入试剂的合理顺序为 (选填a、b、c).
a.先加NaOH,后加Na2CO3 , 再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过、冷却、 (填写操作名称)除去NaCl.
(5)在电解过程中,与电源负极相连的电极上的电极反应式为 ,
若检验与电源正极相连的电极上的气体产物,实验室中通常选用的化学试剂是 .
技术的发展与创新永无止境,我国化工专家侯德榜改革国外路布兰、索尔维的纯碱生产工艺,使生产纯碱的成本明显降低.生产流程可简要表示如下图:
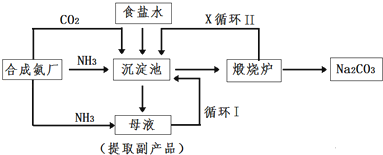
(1)向沉淀池中要通入CO2和氨气,应先通入 (填化学式).
(2)沉淀池中发生反应的化学方程式 ,煅烧炉中发生反应的化学方程式是 .
(3)向母液中通氨气后再加入细小食盐颗粒,冷却析出的副产品是 ,加入细小食盐颗粒的作用是 .
(4)写出路布兰制碱法的反应原理中属于氧化还原反应的化学方程式 ,该法与侯德榜制碱法相比的缺点是 (写出两点即可)
(5)侯氏制碱法制得的纯碱中含有碳酸氢钠杂质.现用沉淀法测定纯碱的纯度,取m1g样品,加水溶解,再加过量的CaCl2溶液,充分反应后,过滤、洗涤、干燥后称得沉淀的质量为m2g.则此样品中的纯度表达式为: .
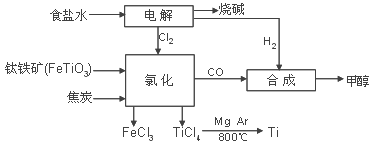
某化工厂将钛、氯碱工业和甲醇制备联合生产,大大提高原料利用率,并减少环境污染.流程如图:
回答下列问题:
-
(1) 写出以石墨为电极电解饱和食盐水的离子方程式
-
(2) 写出钛铁矿在高温下与焦炭经氯化得四氯化钛的化学方程式 ,生成1mol四氯化钛时转移电子的物质的量为 mol
-
(3) 利用四氯化钛制备TiO2•xH2O时,需加入大量的水并加热的目的是
-
(4) 钛广泛用于航天领域.氩气在冶炼钛的流程中的作用是
-
(5) 利用CO和H2制备甲醇
①已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为﹣285.8kJ/mol、﹣283.0kJ/mol和﹣726.5kJ/mol.写出CO和H2制备甲醇的热化学方程式
②假设联合生产中各原料利用率为100%,若得到6mol甲醇,则只需再补充标准状况下的H2 L.
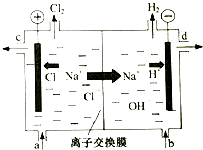
完成下列填空:
-
(1) 粗食盐的水溶液含有SO42﹣、Ca2+、Mg2+ . 若要除去SO42﹣ , 则需加的试列为.
-
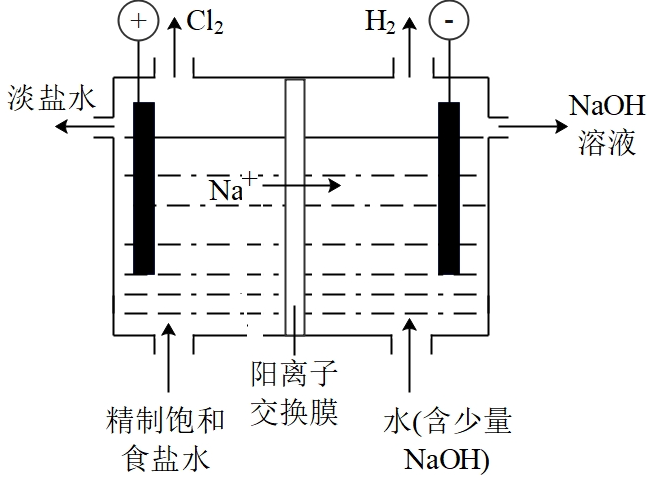
(2) 精制饱和食盐水从图中位置补充,氢氧化钠溶液从图中位置流出(选填“a”、“”“b”、“c”或“d”)
-
(3) 0.1mol/L的Na2SO3溶液中各离子浓度从人到小的顺序为.
-
(4) 室温下,0.1mol/L的NaClO溶液的pH0.1mol/L的Na2SO3溶液的pH.(选填“大于”、“小于”或“等于”)(已知:H2SO3 K1=1.54×10﹣2 K2=1.02×10﹣7;HClO K=2.95×10﹣8)
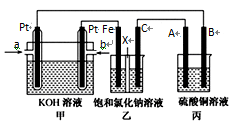
-
(1) 从 a口通入的气体为。
-
(2) B电极的电极材料是。
-
(3) 写出甲中通甲烷一极的电极反应式: 。
-
(4) 写出乙中发生的总反应的离子方程式为。
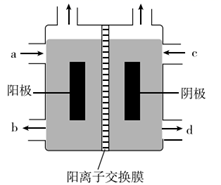
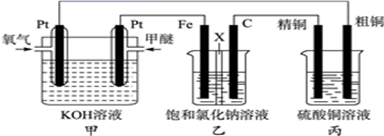
根据要求回答相关问题:(甲醚的化学式:CH3OCH3)
-
(1) 通入氧气的电极为(填“正极”或“负极”),写出负极的电极反应式。
-
(2) 铁电极为(填“阳极”或“阴极”),石墨电极(C)的电极反应式为。
-
(3) 如果粗铜中含有锌、银等杂质,反应一段时间,硫酸铜溶液浓度将 (填“增大”“减小”或“不变”)。
-
(4) 若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为;丙装置中阴极析出铜的质量为。
已知:pH升高时,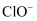 易歧化为
易歧化为 和
和 。
。
-
(1) 电解饱和食盐水的离子方程式为。
-
(2) 下列关于
 产生的说法中,合理的是(填序号)。
产生的说法中,合理的是(填序号)。
a.
 主要在阴极室产生
主要在阴极室产生b.
 在电极上放电,可能产生
在电极上放电,可能产生
c.阳离子交换膜破损导致
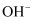 向阳极室迁移,可能产生
向阳极室迁移,可能产生
-
(3) 测定副产物
 含量的方法如下图。
含量的方法如下图。
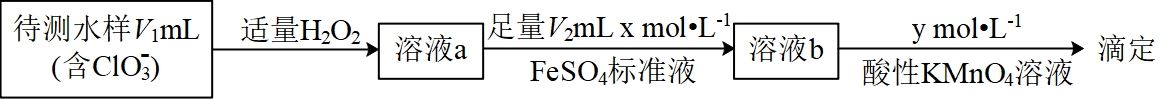
①加入
 的目的是消耗水样中残留的
的目的是消耗水样中残留的 和
和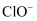 。若测定中未加入
。若测定中未加入 , 则测得的水样中
, 则测得的水样中 的浓度将(填“偏大”“偏小”或“不受影响”)。
的浓度将(填“偏大”“偏小”或“不受影响”)。②滴定至终点时消耗
 酸性
酸性 溶液,水样中
溶液,水样中 的计算式为。
的计算式为。 -
(4) 可用盐酸处理淡盐水中的
 并回收
并回收 。
。
①反应的离子方程式为。
②处理
 时,盐酸可能的作用是:
时,盐酸可能的作用是:i.提高
 , 使
, 使 氧化性提高或
氧化性提高或 还原性提高;
还原性提高;ii.提高
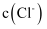 , 。
, 。③用如图装置验证i,请补全操作和现象:闭合K,至指针读数稳定后,。
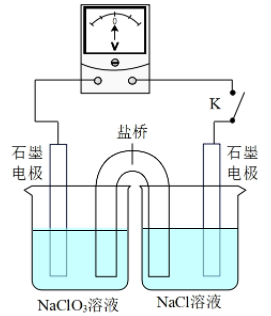
- 下列物质的水溶液不能吸收SO2的是 A.石灰水 B. 亚硫酸钠 C.纯碱
- 已知 是方程的解,则的值为 。
- 图表示人在吸气时,膈肌的运动情况。此时,膈肌所处 的状态、胸廓容积和肺内气压的变化分别是 A. 收缩、缩小、下降
- 已知f(x)= (a∈R)是R上的奇函数, (1)求a的值; (2)求f(x)的反函数f-1(x); (3)对任意给定的
- 《史记》和《资治通鉴》堪称史学双璧,成为研究中国古代历史的重要参考资料。下列史实可能在《史记》和《资治通鉴》中都能找到的
- (2011•山东省聊城市)3.将下面消息的内容概括为一句话新闻。(2分)昨日(5月30日)中午11时39分,刘若曦发表微
- 下列一段话排列正确的一项是:( ) ①范仲淹写《岳阳楼记》的时候正贬官在外,“处江湖之远”,本来可以采取独善其身的态
- 山 园 小 梅 林逋 众芳摇落独暄妍,占尽风情向小园。 疏影横斜水清浅,暗香浮动月黄昏。 霜禽欲下先偷眼,粉蝶如知合断魂
- 细胞质基质是细胞结构的重要组成部分。下列有关叙述中,错误的是 A.呈透明的胶质状态 B.是活细胞进行多种化学
- 阅读《满井游记》(节选),完成1——6题。(18分) 廿二日天稍和,偕数友出东直,至满井。高柳夹堤,土膏微润,一望空阔,
- 下列各组物质不能发生反应的是() A.镁与稀硫酸 B.锌与硫酸铜溶液 C.铝与硝酸银溶液 D.汞与氯化铜溶液
- 设向量a,b,c满足a+b+c=0,且a⊥b,|a|=1,|b|=2,则|c|2的值为( )A.1
- (2012年5月江苏淮安第四次调研)如图甲所示,理想变压器原、副线圈的匝数比 n1∶n2=3∶1,L1、L2为两相同灯泡
- Obviously, the book is _______ for children aged between th
- 在等高线地图上,等高线较稀疏,说明该地是( ) A.坡陡地区 B.山谷 C.陡崖
- 苯和甲苯相比较,下列叙述中不正确的是 A.都属于芳香烃 B.都能使KMnO4酸性溶液褪色
- 提纯下列物质(括号中为少量杂质),选择试剂和分离方法都正确的是 ()被提纯的物质 除杂试剂 分离方法 A 甲烷(乙烯
- 世界上50多亿人口的100多亿只手掌各不相同,且手掌上的每个手指的指纹都不相同。为此,华夏银行将储户的指纹输入计算机内,
- BUS SERVICE Edi
- 如图所示,已知R1 =10Ω,R2 =20Ω,R3 =20Ω,AB两端间电压恒为30V,若CD之间接理想电压表,则电压表



