纯碱工业(侯氏制碱法) 知识点题库
化工厂的设计是将实验室的研究成果转化为工业化生产的重要的基础工作.
(1)以硫铁矿为原料生产硫酸需经过 、 和三个主要生产阶段.
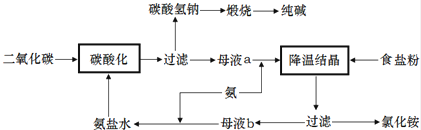
(2)侯氏制碱法是在索尔维制碱法的基础上创造出的一种新的制造纯碱的方法.具体工艺流程图如图所示:
①索尔维制碱法的原理是 .(用化学方程式表示)
②侯氏制碱法与索尔维制碱法相比,优点是 .
③侯氏制碱法可以循环使用的物质有 .
(3)食盐也是一种重要的化工原料,氯碱工业就是通过电解饱和食盐水来制备NaOH、H2和Cl2 . 海水中得到的粗盐中往往含有一些杂质,必须加入一些化学试剂,使杂质沉淀,处理后的盐水还需进入阳离子交换塔,其原因是 .电解食盐水在离子交换膜电解槽中进行,离子交换膜的作用是 .
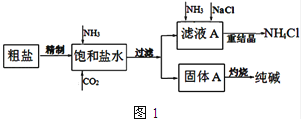
纯碱(Na2CO3)在生产生活中具有广泛的用途.如图1是实验室模拟制碱原理制取Na2CO3的流程图.
完成下列填空:
已知:粗盐中含有Ca2+、Mg2+、SO42﹣等杂质离子.
-
(1) 精制除杂的步骤顺序是 → →→→(填字母编号).
a.粗盐溶解 b.加入盐酸调pH c.加入Ba(OH)2溶液
d.加入Na2CO3溶液 e.过滤
-
(2) 向饱和食盐水中先通入NH3 , 后通入CO2 , 理由是 .在滤液a中通入NH3和加入精盐的目的是 .
-
(3) 请在图1流程图中添加两条物料循环的路线.
-
(4)
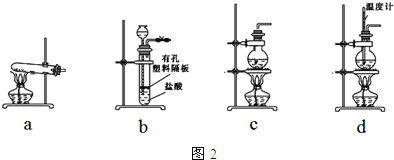
图2装置中常用于实验室制备CO2的是 (填字母编号);用c装置制备NH3 , 烧瓶内可加入的试剂是 (填试剂名称).
-
(5) 一种天然碱晶体成分是aNa2CO3•bNa2SO4•cH2O,利用下列提供的试剂,设计测定Na2CO3质量分数的实验方案.请把实验方案补充完整:
供选择的试剂:稀H2SO4、BaCl2溶液、稀氨水、碱石灰、Ba(OH)2溶液
① .
② .
③ .
④计算天然碱晶体中含Na2CO3的质量分数.
 Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O
Na2CO3+CO2↑+H2O
B . 氢氧化钠:2NaCl+2H2O H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2
H2↑+Cl2↑+2NaOH
C . 高温下制粗硅:C+SiO2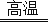 CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融)
CO2↑+Si
D . 电解法制金属镁:MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
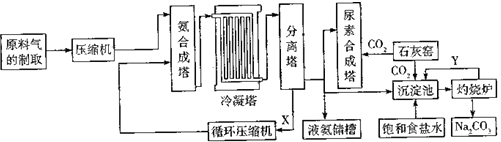
-
(1) 原料气进入压缩机前需要进行净化处理,其目的是.制备氨合成塔的材料(填“能”或“不能”)使用普通的碳素钢.
-
(2) N2、H2混合气体经压缩后再送入氨合成塔,优点是. 某整个生产中循环使用某些原料可提高生产效益,能循环利用的物质是.
-
(3) 请按要求填写下列空白.
①沉淀池中的离子方程式:.
②生产尿素的化学方程式:.
-
(4) 在较低温度下,可从沉淀池的溶液中分离出一种副产品由此可推断,低温下NH4Cl的溶解度很可能(填“小于”或“大于”)NaCL.NH4Cl是一种氮肥,但长期施用易使土壤酸化,用离子方程式表示其原因.
-
(5) 以焦炭、水为原料制备H2 (碳转化为CO2 , 则1000g纯度为a%((杂质不与水反应)焦炭最多可制备 g尿素(已知合成氨时h2的利用率为b%、合成尿素时NH3的利用率为c%)
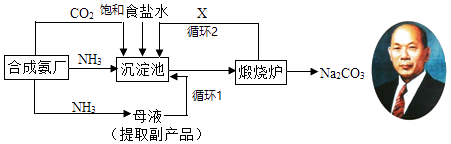
该生产纯碱的方法称联合制碱法或侯德榜制碱法联合制碱法或侯德榜制碱法,在制得纯碱的同时,还可得到一种副产品.
-
(1) 上述沉淀池中发生的化学反应方程式是,实验室分离出沉淀的操作是,该操作使用的玻璃仪器有;
-
(2) 写出上述流程中X物质的分子式;
-
(3) 使原料氯化钠的利用率从70%提高到90%以上,主要是设计了 的循环(填上述流程中的编号1、2);
-
(4) 为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,还需要的试剂有;
-
(5) 向母液中通氨气,加入细小食盐颗粒,冷却析出副产品.通氨气的作用有 .A . 增大NH4+的浓度,使NH4Cl更多地析出 B . 使NaHCO3更多地析出 C . 使NaHCO3转化为Na2CO3 , 提高析出的NH4Cl纯度.
-
(1) 我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下:
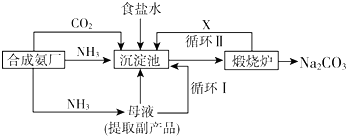
①向饱和食盐水中依次通入足量的NH3、CO2(氨碱法),而不先通CO2再通NH3的原因是
②从生产流程图可知,可循环利用的物质是
③写出沉淀池中、煅烧炉中反应的化学方程式
-
(2) 如何用CO2和50mL 2mol•L﹣1NaOH溶液制取50mL 1mol•L﹣1Na2CO3溶液?
①写出简要的实验步骤
②写出有关反应的化学方程式.
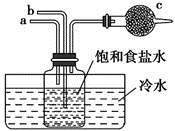
①金属钠投入FeCl3溶液中
②少量Ca(OH)2投入过量NaHCO3溶液中
③向饱和Na2CO3溶液中通入足量CO2
④向AlCl3溶液中滴入NaHCO3溶液
⑤过量NaOH溶液和明矾溶液混合
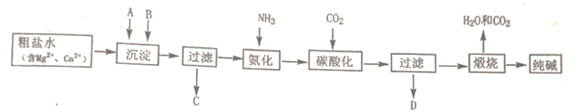
完成下列填空:
-
(1) 粗盐水加入沉淀剂A、B除杂质(沉淀剂A来源于石灰窑厂),写出A、B的化学式。A,B。
-
(2) 碳酸化后过滤,滤液D最主要的成分是(填写化学式),检验这一成分的阴离子的具体方法是:。
-
(3) 该工艺流程中可回收再利用的物质是。
-
(4) 产品纯碱中含有碳酸氢钠,如果取m1kg纯碱加热分解后剩余固体质量为m2kg,纯碱中碳酸氢钠的质量分数可表示为:。
-
(1) 工业生产纯碱的第一步是除去饱和食盐水的中Mg2+、Ca2+离子,从成本角度考虑加入试剂的化学式为、。某实验小组的同学模拟侯德榜制碱法制取纯碱,流程如下:
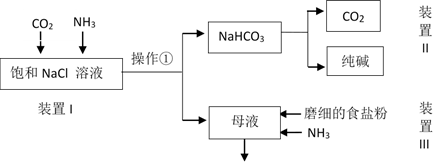
已知:几种盐的溶解度
NaCl
NH4HCO3
NaHCO3
NH4Cl
溶解度(20℃,100gH2O时)
36.0
21.7
9.6
37.2
-
(2) ①写出装置I中反应的化学方程式。
②从平衡移动角度解释该反应发生的原因。
③操作①的名称是。
-
(3) 写出装置II中发生反应的化学方程式。
-
(4) 请结合化学用语说明装置III中加入磨细的食盐粉及NH3的作用。
-
(5) 该流程中可循环利用的物质是。
-
(6) 制出的纯碱中含有杂质NaCl,为测定其纯度,下列方案中不可行的是。
a.向m克纯碱样品中加入足量CaCl2溶液,测生成CaCO3的质量
b.向m克纯碱样品中加入足量稀H2SO4 , 干燥后测生成气体的体积
c.向m克纯碱样品中加入足量AgNO3溶液,测生成沉淀的质量
 和
和 溶液制备
溶液制备
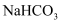 溶解度比NaCl、
溶解度比NaCl、 、
、 、
、 都小的性质,运用
都小的性质,运用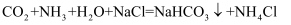 的反应原理制备纯碱。下面是在实验室进行模拟实验的生产流程示意图:
的反应原理制备纯碱。下面是在实验室进行模拟实验的生产流程示意图:
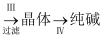
则下列叙述错误的是( )
 , B气体是CO2
B . 第Ⅲ步得到的晶体是发酵粉的主要成分
C . 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D . 第Ⅳ步操作的主要过程有溶解、蒸发、结晶
, B气体是CO2
B . 第Ⅲ步得到的晶体是发酵粉的主要成分
C . 第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒
D . 第Ⅳ步操作的主要过程有溶解、蒸发、结晶
-
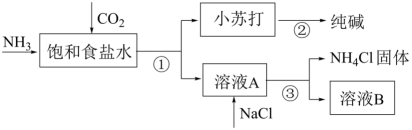
(1) ①~③所涉及的操作方法中,包含过滤的是(填序号)。
-
(2) 根据上图,写出①中发生反应的化学方程式:。
-
(3) 下列说法中,正确的是(填字母)。
a.
 可循环使用
可循环使用b.副产物
 可用作肥料
可用作肥料c.溶液B中一定含有
 、
、 、
、
-
(4) 除去
 粉末中混有的少量小苏打的方法是,所涉及的反应的化学方程式为。
粉末中混有的少量小苏打的方法是,所涉及的反应的化学方程式为。
-
(5) 若制出的纯碱样品中含有的杂质只有NaCl。
①检验用该纯碱样品配制的溶液中含有
 的方法是。
的方法是。②向m g纯碱样品中加入足量的
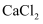 溶液,沉淀经过滤、洗涤、干燥,称其质量为b g。则该纯碱样品的纯度(质量分数)为(用m、b 来表示)。
溶液,沉淀经过滤、洗涤、干燥,称其质量为b g。则该纯碱样品的纯度(质量分数)为(用m、b 来表示)。
-
(1) 【方法一】路布兰以食盐、浓硫酸、焦炭和石灰石为原料,制得了纯碱。其反应原理为
①2NaCl+H2SO4(浓)
 Na2SO4+2HCl
Na2SO4+2HCl②2Na2SO4+4C
 Na2S+4CO↑
Na2S+4CO↑③Na2S+CaCO3
 Na2CO3+CaS
Na2CO3+CaS写出反应③的基本反应类型
-
(2) 用单线桥法表示反应②的电子转移方向和数目
-
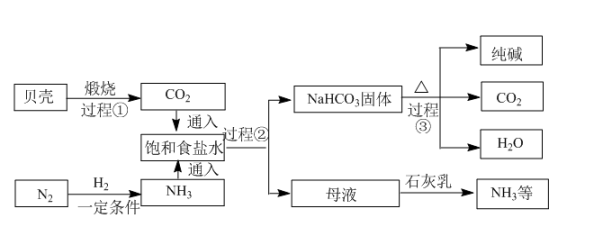
(3) 【方法二】索尔维和侯德榜又发明了新的制碱方法,其模拟流程如下:
【资料查阅】
I.通常情况下,1体积水中大约能溶解700体积氨气,1体积水中大约能溶解1体积二氧化碳。
Ⅱ.饱和食盐水中发生的主要反应为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl。
上述流程中过程②的主要操作的名称是,可以循环利用的物质是(填化学式)。
-
(4) 写出饱和食盐水中主要反应的离子方程式
-
(5) 为了提高产率,往饱和食盐水中通入气体时,你认为应该先通入(填“NH3”或“CO2”),你的理由是。
-
(6) 母液的主要成分为NH4Cl和NaCl,写出在加热条件下母液与石灰乳反应的化学方程式。
- The old man looks very unhappy, becausehe lives , and h
- 阅读理解。 阅读下列材料,从A、B、C、D四个选项中选出最佳答案。 John Smith was a good m
- 如图,在Rt△ABC中,∠C=90°,D是BC边上一点,且BD=AD=8, ∠ADC=60°则AC=_______。
- 新修订的《重庆市未成年人保护条例》确定了“未成年人的合法权益应当得到特殊、优先保护”的原则。确定这一原则是基于未成年人(
- 19. 将下列句子组成语意连贯的语段,排序最恰当的一项是() ①好看的是变幻。一匹马会变成什么呢?②孩子们看云,真正让他
- 常用的天气符号中表示 A.阴 B.小雨 C.中
- 经过20多年的探索实践,我国形成了多种领导干部公选方式,如江苏的“公推公选”模式、浙江宁波的“双推双考”模式等,为完善我
- 下图中几何体的左视图是( ).
- 在“测定小灯泡的电功率”的实验中,小明同学选用的小灯泡的额定电压为2.5V,电阻约为8Ω,滑动变阻器的最大阻值为10Ω。
- 下面哪种不是高尔基体的功能? A.把糖加到蛋白质中 B.贮存脂肪 C.包装分泌的产物 D
- 如图甲所示,边长为L的正方形区域ABCD内有竖直向下的匀强电场,电场强度为E,与区域边界BC相距L处竖直放置足够大的荧光
- 已知向量a=(,1),b是不平行于x轴的单位向量,且a·b=,则b等于( )A.(,)
- 关于黄埔军校的叙述,正确的是 ①在中国和苏联的帮助下创办 ②创校于1924年的广州 ③孙中山任校长 ④军校培养了大
- 王老师上课展示了一幅有关北宋画家张择端的《清明上河图》教学图片,你认为它反映出的最主要历史信息是 A.描绘了大运河两岸繁
- 为了比较蔬菜中维生素C含量,黎明同学根据维生素C可使高猛酸钾溶液褪色的原理,设计了如下实验:在四只同样的试管中分别加入2
- 根据α粒子散射现象,提出带核的原子结构模型的科学家是A.汤姆生 B.卢瑟福 C.道尔顿
- “臭名昭著的‘解放’实际上是对农民进行残酷地掠夺。”这里列宁评价的是 A.光荣革命 B.美国内战
- 无铅汽油一般是加入甲基叔丁基醚【CH3OC(CH3)3】作为高辛烷值组分。下列关于甲基叔丁基醚叙述错误的是
- 已知15 g A物质和10.5 g B物质恰好完全反应生成7.2 g C、1.8 g D和0.3 mol E,则E物质的
- 我们常吃的大白菜、卷心菜、萝卜属于 A.菊



