物质的相互转化和制备 知识点题库
空气中氮气的含量最多,氮气在高温、高能量条件下可与某些物质发生反应.图1是以空气和其他必要的原料合成氮肥(NH4NO3)的工业流程.请按要求回答下列问题:

(1)步骤①中发生的是 变化(填“物理”或“化学”).
(2)写出步骤③中发生反应的化学方程式 .
(3)上述化学反应中属于化合反应的有 个.
(4)图2是化肥硝酸铵包装袋上的部分说明:硝酸铵应具有的性质是 (填字母).
A.易溶于水 B.有挥发性 C.受热易分解
施用该类肥料时,要避免与碱性物质混合使用,写出硝酸铵与熟石灰反应的化学方程式 .

-
(1) 减少二氧化硫的排放,主要为了 (填序号);A . 减缓温室效应 B . 减少酸雨形成 C . 防止破坏臭氧层
-
(2) 操作a的名称,氧化塔通入的气体A是;(氧气、氮气、二氧化碳)
-
(3) 写出制碱釜中反应的符号表达式;
-
(4) 该流程中可循环使用的是.

-
(1) 二氧化硅属于(填“酸”、“碱”、“盐”、“氧化物”或“有机物”中一种).
-
(2) 与碱反应时,SiO2和CO2有相似的化学性质.装NaOH溶液的试剂瓶不能用玻璃塞,是因为在常温下,NaOH与玻璃塞中的SiO2缓慢地反应,生成有粘性的硅酸钠,进而使瓶口与瓶塞粘合在一起的缘故.试写出该反应的化学方程式.
-
(3) 硅是太阳能电池和电脑芯片不可缺少的材料.制备粗硅的反应为:SiO2+2C
 Si+2CO↑,属于反应类型(填“分解”、“化合”、“置换”、“复分解”之一).
Si+2CO↑,属于反应类型(填“分解”、“化合”、“置换”、“复分解”之一).
-
(4) 物质A通常状况下为无色有刺激性气味的气体,排放到空气中会引起环境污染,下列试剂可以吸收A的是 (填字母序号).A . 氢氧化钠溶液 B . 浓硫酸 C . 金属铁 D . 氯化钠溶液.

-
(1) 加入过量A溶解后,再进行操作a时玻璃棒的作用是.
-
(2) 工厂废液中加入过量A的目的是.
-
(3) 溶液甲中的金属离子是(写离子符号).
-
(4) 步骤①②③中所发生的化学反应,其中属于置换反应的是(填序号).
-
(5) 步骤③中发生反应的化学方程式是.

-
(1) 反应②的基本反应类型是;
-
(2) 反应②后进行的分离操作名称是,完成该操作所需要的玻璃仪器除烧杯、玻璃棒外,还需要,若得到的氯化铵溶液仍然浑浊,原因可能是(写出一种即可);
-
(3) 反应③属于分解反应,除得到氧化锌外还生成两种常见气体,其化学式为和.
-
(4) 高纯氧化锌属于(填“混合物”或“纯净物”)

-
(1) 从“海水叶粗盐叶精盐”的过程包括溶解、过滤、蒸发等实验操作,实验室中上述3种操作都需要使用的仪器是(填名称),该仪器在蒸发操作中的作用是。
-
(2) “食盐水”中常含有NaCl,MgCl2 , CaCl2等物质,“精制”过程中加入NaOH的目的是。
-
(3) 20℃时,“饱和食盐水”的溶质质量分数为26.47%,则该温度下,氯化钠的溶解度为(计算结果精确到0.1)。
-
(4) 写出“电解槽”中发生反应的化学方程式:。
-
(5) 流程中可以循环使用的物质有(填化学式)。
-
(6) 氯碱工业生产的碱样品中常含有Na2CO3和NaCl等杂质,碱样品中含有Na2CO3的原因是;检验碱样品中是否含有Na2CO3 , 下列试剂中可选择使用的是(填字母)。
A 酚酞试液 B 石蕊试液 C 硝酸铵溶液 D 澄清石灰水
-
(7) 用“离子交换膜法”生产的碱样品质量主要标准如下表所示:
等级
氢氧化钠含量
碳酸钠含量
优等品
≥99.0%
≤0.5%
一等品
≥98.5%
≤0.8%
合格品
≥98.0%
≤1.0%
化学兴趣B组设计并完成了如下实验来判断碱样品的等级(不考虑其他杂质参加反应)。称取20.3 g碱样品,加入足量的水溶解,再加入足量的氯化钡溶液,充分反应后,过滤得到滤渣和滤液;将滤渣洗涤、干燥,得到碳酸钡固体0.197 g;向滤液中加入2滴酚酞,再逐滴加入稀盐酸至恰好完全反应,共消耗溶质质量分数为5.0%的稀盐酸365 g。
①该碱样品中碳酸钠的含量(质量分数)为(计算结果精确到0.01% )。
②列式计算该碱样品中氢氧化钠的含量(计算结果精确到0.01% )。
③该碱样品的等级为。
| 选项 | 甲 | 乙 | 丙 | 丁 |
| A | CuO | H2SO4 | CO2 | O2 |
| B | Na2SO4 | Ba(OH)2 | HCl | Ba(NO3)2 |
| C | NaOH | CO2 | Ca(OH)2 | MgCl2 |
| D | Mg | Cu(OH)2 | NaOH | H2SO4 |

-
(1) 钛被称为“21世纪金属”,主要用于航天和航海工业。从物质分类来看,钛合金属于。
-
(2) 炼铁厂常以焦炭赤铁矿等为主要原料炼铁,请写出一氧化碳与氧化铁反应的化学方程式:。
-
(3) 矿物的储量有限,而且不可再生,我们必须保护金属资源并进行金属的回收利用。某兴趣小组同学欲从含有硫酸、硫酸亚铁和硫酸铜的废液中回收全部金属铜,应先加入过量的,反应的化学方程式为:、。充分反应后过滤,滤渣中含有。 将滤液蒸发结晶可得到硫酸亚铁固体,滤渣加酸处理可得到纯净的金属铜。
 B . 反应②中稀有气体的作用是隔绝空气
C . 反应①②中钛元素的化合价均发生改变
D . 反应②中金属的总质量保持不变
B . 反应②中稀有气体的作用是隔绝空气
C . 反应①②中钛元素的化合价均发生改变
D . 反应②中金属的总质量保持不变

 (不考虑H2O2的自身分解),请回答:
(不考虑H2O2的自身分解),请回答: 
-
(1) 用酸浸泡可将废旧电子设备中的铝、 铁等金属除去,请从金属活动性顺序的角度解释原因:。
-
(2) 写出一个提炼过程中还可能存在的化学反应方程式。
-
(3) 提炼出的贵重金属中有。
-
(4) 经过操作①得到的滤液中,含有硫酸铝、硫酸铜、硫酸铁、水,除此以外,还一定含有的物质是。

已知:①SiO2在“碱溶”时转化为铝硅酸钠沉淀。
②Na2CO3可转化为 NaHCO3 , 反应的化学方程式为:  。
。
回答下列问题:
-
(1) “碱溶”时,其中一个反应的化学方程式为:
 ,X的化学式为,“碱溶”的目的是。
,X的化学式为,“碱溶”的目的是。
-
(2) 在实验室里完成“操作1”,需要用到的玻璃仪器有。
-
(3) 在“滤液1”中加入NaHCO3溶液,三种物质反应(化学计量数之比为1:1:1)生成氢氧化铝固体和碳酸钠溶液,反应的化学方程式为。
-
(4) 流程中可循环利用的物质(水除外)是(填化学式)。
-
(5) “灼烧”是使氢氧化铝受热分解为两种氧化物,反应的化学方程式为。
-
(6) 100kg含Al2O360%的铝土矿,理论上可得到Al的质量为kg(计算结果精确到0.1)。
-
(1) 向盛有适量碳酸钠溶液的四支试管中分别加入下列试剂,实验现象记录如下:
试管编号
1
2
3
4
加入试剂
无色酚酞试液
稀盐酸
澄清石灰水
氯化钡溶液
实验现象
有气泡产生
有白色沉淀产生
有白色沉淀产生
-
(2) 试管3中发生反应的化学方程式为。
-
(3) 化学兴趣小组的同学对反应后溶液中溶质的成分进一步探究:小组同学将试管3中的物质过滤,得到滤液A。
(提出问题)滤液A中溶质的成分是什么?
(猜想与假设)猜想一:NaOH 猜想二:NaOH和Na2CO3
猜想三: 猜想四:NaOH、Na2CO3和Ca(OH)2
-
(4) (活动探究)
①小组讨论:有同学认为猜想四不成立,原因是。
②甲、乙两位同学分别用不同的方法进行实验:
实验操作
实验现象
实验结论
甲:取少量滤液A于试管中,加
入过量的稀盐酸
有气泡生成
猜想成立
乙:取少量滤液A于试管中,加入适量的Ba(NO3)2溶液
-
(5) (反思与评价)①碳酸钠溶液呈性,可以和盐酸、氢氧化钙、氯化钡等物质发生反应。
②要验证反应后物质的成分,既要考虑生成物,还应考虑。
 H2SO4
B . NaHCO3
H2SO4
B . NaHCO3  NaCl
C . H2O
NaCl
C . H2O 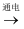 O2
D . NH4Cl
O2
D . NH4Cl  NH3
NH3

-
(1) 写出对应物质的名称:甲、丁。
-
(2) A→丙反应的文字表达式。
-
(3) A→乙反应的实验现象。
-
(4) 写出图中四个化学反应的共同点:(写一点)。


-
(1) 步骤①中发生的是(填“物理”或“化学”)变化。
-
(2) 步骤②中反应物单质X的化学式为。
-
(3) 步骤③中发生反应的化学方程式为。
-
(4) 根据图2说明,推测硝酸铵可能具有的一条性质是。该化肥中硝酸铵的质量分数至少是。

-
(1) 系统1中电解水的化学方程式为。
-
(2) 系统2的作用是。
-
(3) “反应器”中在一定条件下发生反应的化学方程式为。

-
(1) 比较生铁和钢,二者的区别是。
-
(2) 焦炭的主要成分是碳,在生铁冶炼过程中,焦炭参与了下列反应:A.C+O2
 CO2;B.C+CO2
CO2;B.C+CO2 2CO,其中为冶炼生铁提供热量的反应是(填序号)。
2CO,其中为冶炼生铁提供热量的反应是(填序号)。
-
(3) 铁与物质甲发生反应的化学方程式是。
-
(4) 若铁与物质乙反应时,火星四射,则生成物中固体的化学式是;若固体为红色单质,则铁与物质乙反应的化学方程式是(任写一个)。


- 为提纯下列物质(括号内为杂质),所选用的试剂和分离方法均正确的是 ( ) A、溴乙烷(乙醇):水,分液
- 下表是某年人口流动的地区构成,分析完成2- 3题。2.表中显示人口流动特征是 A.城市到农村 B.城市到城市 C.中西部
- 民生问题是2010年“两会”代表委员关注的热点。据此回答32—33题。 “两会”期间,代表委员们就社会热点问题,展开讨论
- 亚硝酸(HNO2)既可作氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的是( ) A.N2O5
- 如右图,一有界区域内,存在着磁感应强度大小均为B,方向分别垂直于光滑水平桌面向下和向上的匀强磁场,磁场宽度均为L,边长为
- 测得某金属冶炼厂的酸性工业废水中,含有一定量的Fe3+、Cu2+、Au3+等离子。按照“变废为宝”的原则,设计了下图中的
- Each time tourists travel to Beijing, they_______ the Forbid
- 有四种粒子的结构示意图,下列说法不正确的是( ) ① ②
- Books are made __________ paper while paper is mainly made _
- Mrs. King put acoat ________ the sleeping girl to keep her w
- 下列关于细胞核的说法,不正确的是 A.所有的真核细胞均有细胞核 B.细胞核是遗传物质贮存和复制的场所 C.DNA主要
- 设向量a=(-2sinα,2cosα)(0<α<π),向量b=(-,0),则a·b的夹角是 A.α
- At a laboratory in Germany ,volunteers slide into a machine
- 28.人体细胞中组成核酸的五碳糖、碱基和核苷酸种类依次是A.2 4 4 B.4
- 2.下列各句中,加点的成语使用不恰当的一项是( ) A.在三十年的教学生涯中,她倾情投入,取得了巨大的成就,在当地教育
- 医生在检验某病人的尿液时发现了较多的红细胞,如果是肾脏有疾病,可能是肾脏的哪个部位出现了病症 A.肾小管
- 3.下列用横线连接的成语,意思全都相近的一项是( ) A.自始至终——有头无尾 聚精会神——心无二用 B
- 某溶液中可能含有Na+、K+、Mg2+、I—、SO32—、SO42—等离子中的全部或其中的几种。现分别进行以下实验操作:
- --I’vebeen thinking about those questions you asked m
- 有一个随机交配的种群,在没有迁移等条件下,两年内该种群的基因频率的变化如下表,根据现代生物进化理论,在这两年中,与这对基



