盐的化学性质 知识点题库
化学兴趣小组的同学发现实验台上一瓶标签破损的无色溶液(标签如图).他们提出可能是Na2SO4、NaHCO3、Na2CO3溶液中的一种,于是决定对这瓶溶液进行实验探究.查阅资料:三种物质溶液在常温下的pH如下表
溶液 | Na2SO4 | NaHCO3 | Na2CO3 |
pH | pH=7 | pH>7 | pH>7 |

-
(1) 小新同学认为该溶液不可能的是 , 理由是 .
-
(2) 标签破损的原因 .
-
(3) 为确定其成分,小新同学设计如下方案进行探究
实验步骤
现象
结论
取该溶液少许于试管中,滴加过量的BaCl2溶液,振荡.
①
则该溶液是Na2CO3溶液
过滤,向滤渣滴加稀盐酸.
②
-
(4) 小芳认为可以设计更简单的实验方案,该方案是:(写出实验步骤、现象及结论).
| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
-
(1) 哪几次反应中碳酸钙有剩余?
-
(2) 上表中m的值为 。
-
(3) 试计算这种石灰石中碳酸钙的质量分数。
A.对安全的认识 | B.用“化学”眼光分析 |
①点燃可燃性气体前一定要验纯 ②煤气泄漏立即打开排气扇 ③煤矿矿井要保持通风、严禁烟火 | ①洗涤剂去除油污是因为乳化作用 ②用适量的熟石灰可中和土壤的酸性 ③用水灭火是降低温度至可燃物的着火点以下 |
C.化学与健康 | D.对除杂和鉴别的认识 |
①霉变的大米洗净烧熟后可以食用 ②利用甲醛水溶液浸泡水产品防腐 ③人体缺铁会导致贫血 | ①用灼热的CuO除去CO中少量CO2 ②用Ca(OH)2溶液除去NaOH溶液中的Na2CO3 ③用燃烧的方法区分羊毛和涤纶 |
一种“环保石头纸”开始被人们使用,其主要成分是碳酸钙.某班同学对它产生了浓厚的兴趣,把“环保石头纸”带到实验室,完成了如右图所示的两个实验.请回答问题: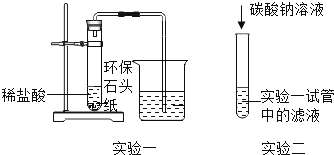
-
(1) 实验一:试管中产生大量的气泡,烧杯中澄清的石灰水变浑浊,请写出“环保石头纸”与稀盐酸发生反应的化学方程式 (假设“环保石头纸”中的其他成分既不溶于水,又不与盐酸发生反应);
-
(2) 实验二:试管中有白色沉淀产生.小刚同学想探究该实验反应后溶液中溶质的成分.
提出猜想:猜想①:NaCl、CaCl2和HCl;猜想②:NaCl;猜想③:NaCl和CaCl2 .
同学们经过讨论排除了猜想,理由是.
有同学认为小刚的猜想不全面,又提出猜想④:NaCl和Na2CO3 , 并通过实验验证了该猜想成立.请你将实验报告补充完整.
实验操作
实验现象
实验结论
取实验二反应后的上层清液少量于试管中,滴加少量 .
猜想④成立
-
(3) 实验结束后,未经处理的废液 (填“能”或“不能”)直接倒入下水道.
-
(1) 以上操作合理的而先后顺序为(数字序号不能重复使用).
-
(2) 请写出BaCl2溶液与Na2CO3溶液反应的化学方程式.
-
(3) 上述试剂中的Na2CO3不能用K2CO3代替,请说明原因.
|
A |
B |
C |
D |
|
|
|
|
|
|
在一定量的AgNO3溶液中逐滴加入NaCl溶液 |
等物质的量的Zn和Mg分别与等体积等质量分数的稀硫酸(足量)反应 |
向稀盐酸溶液中逐滴加入氢氧化钠溶液 |
等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 |
①取少量样品溶于水得到无色溶液,然后滴加过量的氯化钡溶液,出现白色沉淀A,过滤.
②沉淀A中加入过量的稀硝酸,沉淀部分消失并放出气体.往步骤①所得的滤液中加入适量硝酸银溶液和稀硝酸,生成白色沉淀B,过滤.回答下列问题:
-
(1) 白色沉淀B是,步骤②中放出的气体是.
-
(2) 杂质中一定含有,一定没有.
-
(3) 最终所得滤液中含有的阳离子是.
【猜想假设】
猜想1:该溶液没有变质,为NaOH溶液.
猜想2:该溶液全部变质,为Na2CO3溶液.
猜想3:该溶液部分变质,为NaOH和Na2CO3的混合溶液.
-
(1) 【设计方案】请你完善下表几组同学探讨的设计方案
实验操作
可能出现的现象与结论
同学评价
第1组
取少量样品溶液于试管中,向其中滴加酚酞试剂
若溶液变红,则猜想2不成立
第2组同学认为:此方案结论不正确,理由是:.
第2组
取少量样品溶液于试管中,向其中滴加足量的溶液CaCl2溶液
若产生白色沉淀,反应方程式是:,
则猜想(1)不成立
第3组同学认为:此方案还不能确定猜想(2)还是猜想(3)成立
第3组
第一步:将第2组实验后的混合物过滤.第二步:取滤液于试管中,向其中滴加酚酞试剂
若滤液不变红,则猜想(2)成立;若滤液变红,则猜想(3)成立.
第1组同学认为:不需过滤也能达到实验目的,更简单的操作方法是:
.
-
(2)
【探究实验】综合各小组的方案后,动手实验.
【结论与反思】NaOH溶液易与空气中CO2反应而变质,所以要密封保存.
【拓展延伸】同学们设计了下列两套装置进行实验:用胶头滴管吸取某种液体,锥形瓶中充入一种气体或放入一种固体物质,挤压胶头滴管.一段时间后,两装置中气球明显胀大.

甲装置中可能发生反应的方程式是.
-
(3) 若乙装置中胶头滴管吸取的是稀盐酸,则锥形瓶中放入的固体可能是(填化学式).
【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]

-
(1) 【实验步骤】
① ;
②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体为止;
⑤打开弹簧夹a,;
编 号
1
2
3
实验前
228.00
228.00
228.00
实验后
229.10
229.11
229.09
⑥准确称量C装置的质量(如右表);
⑦重复上述步骤;
⑧根据数据进行计算.
-
(2) 【实验分析及数据处理】
A装置中盛放的溶液是,其目的是;
-
(3) D装置的作用是;
-
(4) 计算碳酸镁晶须中的n值:(要有计算过程)
-
(5) 【实验反思】
实验结果与理论值有偏差,可以在B、C增加一个装置以减少误差;
-
(6) 下列选项中,会造成实验结果偏大的是;偏小的是;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
-
(7) 为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热重分析,并绘制出如图2所示的热重曲线示意图.则:
①t2℃时,剩余固体为(填化学式);
① 最终剩余的4.0g物质是(填化学式);
② 碳酸镁晶须完全分解的化学方程式为:.
选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
A | CaCO3(CaO) | ﹣﹣ | 高温煅烧 |
B | KOH溶液(K2CO3) | 适量Ca(OH)2溶液 | 滴加试剂、过滤 |
C | Cu(Fe) | 适量CuSO4溶液 | 滴加试剂、过滤 |
D | CO2(CO) | 足量NaOH溶液 | 洗气、干燥 |
艾江南同学做出以下猜测:
猜测一:只有Cu2(OH)2CO3;猜测二:只有CuSO4•3Cu(OH)2 . 你认为还有一种可能性,你的猜测是.
资料(一):Cu2(OH)2CO3的化学性质可看成Cu(OH)2和CuCO3混合物的性质;CuSO4•3Cu(OH)2的化学性质可看成Cu(OH)2和CuSO4混合物的性质.
资料(二):CuCO3的分解温度约为220℃,CuSO4分解温度约为650℃,酒精灯外焰温度约为400℃.
经过分析,你认为验证你的猜测只要判断铜锈中有无和(填离子符号)两种离子即可.
为此,你利用如图装置设计了如下实验方案:

实验步骤 | 实验现象 | 实验结论 |
取样品放于试管中,加热. | 若观察到 | 则证明有Cu2(OH)2CO3 |
取加热后试管中的残留固体投入装有水的烧杯中,并向其中滴入几滴BaCl2溶液 | 若观察到溶液先变蓝色,后有 | 则证明有CuSO4•3Cu(OH)2 |


-
(1) 实验1中,两支试管的溶液都变成色。
-
(2) 实验2中,若试管B中盛装的是NaOH溶液,发生反应的化学方程式为,该反应的基本类型是反应。
-
(3) 实验3中,某同学向两支试管中吹气,A中有白色沉淀产生,发生反应的化学方程式为。B中无明显现象,为了探究吹气后B中溶质的成分,该同学进行了如下探究。
(提出猜想)猜想1:溶质是氢氧化钠;
猜想2:溶质是碳酸钠;
猜想3:溶质是。
溶质中出现碳酸钠的原因是氢氧化钠与发生了反应。
(实验和结论)
实验
实验现象
结论
取B中少量溶液,加入澄清石灰水至不再产生沉淀为止,静置后取上层清液,向其中滴加几滴酚酞溶液
猜想3成立
(反思与评价)
老师评价该同学得出的结论错误,是因为猜想2也会产生相同的现象。如果要验证“猜想3成立”,必须要将氢氧化钙溶液换成溶液。

-
(1) 镁原子的质子数为,x值为。
-
(2) 镁属于元素(填“金属”或“非金属”),金属镁在化学反应在容易(填写“得到”或“失去”)电子。
-
(3) 海水中含有丰富的氯化镁,目前工业上绝大多数的金属镁是从海水中提取的,其生产流程如图:

在上述流程中,通过操作a分离出固体Mg(OH)2 , 操作a的名称是,试剂C为:。
反应①的化学方程式为。
反应②的化学方程式为。
-
(4) 上述流程中没有涉及到的基本反应类型是反应。
(实验探究)
-
(1) A,B,C,D四组同学分别进行了下列实验

写出下列的两个化学方程式:
①A中的反应;
②D中的反应。
-
(2) (挖掘实质)
如下图是A组反应的微观过程示意图,该化学反应的实质可以表示为:H++OH-=H2O

(实践运用)
完成试验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀,用无色溶液滴加紫色石蕊试剂,变为红色。
①溶液中的白色沉淀一定是,理由是
②废液中一定不含有的离子是和。
-
(3) 为了验证该溶液中能会含有的离子是否存在,我设计如下实验进行验证:
溶液中可能含有的
离子
实验步骤
实验现象
实验结论
①。
②取滤液滴加。
现象明显
含有该离子
-
(1) 碳酸钠俗称苏打或。如图为侯氏制碱法的流程图,通过步骤I后得到的悬浊液中有小苏打(在该溶液中难溶)和一种氮肥,请写出步骤I中发生反应的化学方程式:;上述过程中得到的氮肥遇碱会生成具有刺激性气味的(填化学式),该气体能使;从流程图中可得出小苏打的一条化学性质是。

-
(2) 氢氧化钠在空气中容易变质生成碳酸钠,现有放在空气中一段时间的氢氧化钠溶液,其中溶质的成分可能是:猜想①:NaOH;猜想②:Na2CO3;猜想③:。请设计实验证明猜想③正确。(写出相关的步骤和现象)
-
(3) 某海洋化工集团生产的碳酸钠产品中含有少量氯化钠杂质,其产品包装袋上标明:碳酸钠≥96%。为测定该产品中碳酸钠的质量分数,现取11.0g碳酸钠样品放入烧杯中,称得烧杯及所盛碳酸钠样品的总质量为158.0g,然后向烧杯中加入100g稀盐酸,充分反应,实验数据记录如下:
反应时间/min
3
6
9
12
烧杯及所盛物质的总质量/g
255.8
254.0
253.6
253.6
请你据此分析计算,该产品中碳酸钠的质量分数(是、否)符合标准。(写出计算过程,结果精确到0.1%)
-
(4) 小强同学想在社区宣传栏出一期“低碳减排·绿色生活”专刊,内容之一是汽车耗油量与二氧化碳排放量间关系。已知:①汽油密度约为0.7kg/L;②汽油(假定其为纯净物,根据汽油中C、H组成关系,其化学式可简单表示为CH2 , 其燃烧的化学方程式可表示为:2CH2+3O2
 2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量?
2CO2+2H2O;请计算4升汽油完全燃烧生成二氧化碳的质量?
- US president George Bush ____ the war in Iraq on March 20,20
- 2010年11月10日,网络热词“给力”登上了《人民日报》头版头条标题。网络热词成为日常用语,并进入主流官方语言,是语言
- 实验室加热高锰酸钾制氧气,可直接采用的发生装置是( ) A. B. C. D.
- 某学生将2.5%的脲滴加在载玻片上的蚕豆表皮上,观察到植物细胞的质壁分离。2小时后企图再次观察时却发现理想的视野找不到了
- 改革开放后,逐渐形成了一个全方位、多层次、宽领域的对外开放格局,对这个格局表述正确的是 A.经济特区----
- 地图的基本要素包括比例尺、图例注记和( ) A.信息 B.方向
- 读材料,回答问题:(13分) 材料一:我国水土流失面积占耕地总面积的1/3,主要分布在黄土高原、南方丘陵地区以及北方石山
- 某同学在尝试“用鲜奶制作酸奶”和“用葡萄制作葡萄酒”的过程中遇到了一系列问题,其中分析正确的是() A.制作酸奶需要密封
- 阅读下面的文言文,完成后面小题。 晋厉公欲尽去其大臣而立其左右。胥童谓厉公曰:“必先杀三郄。族大多怨。去大族不逼。”公
- (1)多用电表测未知电阻阻值的电路如图(a)所示,电池的电动势为E、内阻为r, R0为调零电阻,Rg为表头内阻,电路中电
- NA表示阿伏加德罗常数的值,下列说法不正确的是
- 测量视力时,利用平面镜成像特点可以节省空间.如图所示,让被测者面对镜子背对视力表,此人看到视力表的像离他的距离是:
- “竹外桃花三两枝,春江水暖鸭先知”。主要描述的是哪种因素对鸭生活的影响( )A.阳光 B.江水 C
- The flowers ____ sweet in the botanic garden attract the vis
- Like most people, I was brought up to look upon life
- 下列各句中没有语病的一项是( ) (3分) A.卫生部专家表示,我国流感疫情已经进入流行高发期,医学专家正积极进
- 如图,用下面四种方式将轻绳拴住小球放在倾角为a 的光滑斜面上,小球均处于平衡状态,则下列说法中正确的有
- 读“中纬度某地某日河流、晨昏线、风向、等值线的组合图”,回答39~40题。39.关于图中内容说法正确的有 ①该地位于南半
- 已知:H2(g)+F2(g)= 2HF(g) ΔH= -27kJ/mol,下列说法正确的是() A.2 L氟化氢气体分解
- 根据短文内容,从短文后的选项中选出能填入空白处的最佳选项。选项中有两项为多余选项。 Getting your child







