还原反应与金属的冶炼 知识点题库
(1)写出利用木炭还原氧化铜的化学方程式 .
(2)根据你平常的所见所闻及所学的化学知识,写出保护金属资源的方法(要求至少写出两种不同的方法)①;② .
(1)工业上用磁铁矿炼铁的原理为 ,其中高炉内加入焦炭的作用是 .
(2)农业生产中常用15%的食盐水来选种,现有50g质量分数为25%的氯化钠溶液,欲稀释为质量分数为15%的氯化钠溶液,需要加入水的质量为 .
我们的祖先很早就掌握了用孔雀石[主要成分是Cu2(OH)2CO3]和木炭一起加热进行火法炼铜的工艺,早在3000多年前的商朝就造出“后母戊鼎”等许多精美的青铜器.
有关的化学方程式:①Cu2(OH)2CO3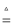 2CuO+H2O+CO2↑;②C+2CuO
2CuO+H2O+CO2↑;②C+2CuO 2Cu+CO2↑.
2Cu+CO2↑.
在西汉时期就开始湿法炼铜的应用,当时刘安所著的《淮南万毕术》中,就有曾青(硫酸铜溶液)得铁则化为铜的记载,请回答下列问题:
(1)上述反应①属于 反应(选填“分解”、“化合”或“置换”).
(2)青铜属于 (填“氧化物”、“单质”、“化合物”或“混合物”).
(3)写出湿法炼铜发生反应的化学方程式: .
(4)以“绿色化学”的观点,对照火法炼铜,谈谈湿法炼铜的优点: .
一无色气体,可能有H2、CO、CO2中的一种或数种,现将无色气体进行如图所示的实验,观察到甲装置中黑色粉末变成光亮的红色物质,乙装置中澄清的石灰水变浑浊,下列分析正确的是( )


如图表示了x、y、z事物间的从属关系,下列选项中不符合图中事物间从属关系的是( )
X | Y | Z | |
A | 氧化物 | 化合物 | 纯净物 |
B | 基因 | DNA | 染色体 |
C | 中和反应 | 复分解反应 | 氧化还原反应 |
D | 质子 | 原子核 | 原子 |

 2Fe+3CO2 的反应中,铁元素由+3价变为0价,碳元素由+2价变为+4价.像这类凡有元素化合价升降的反应都属于氧化还原反应,判断下列反应一定不属于氧化还原反应的是( )
2Fe+3CO2 的反应中,铁元素由+3价变为0价,碳元素由+2价变为+4价.像这类凡有元素化合价升降的反应都属于氧化还原反应,判断下列反应一定不属于氧化还原反应的是( )
 2Al2O3
B . C+2CuO
2Al2O3
B . C+2CuO  2Cu+CO2↑
C . 2H2O
2Cu+CO2↑
C . 2H2O  2H2↑+O2↑
D . NaOH+HCl═NaCl+H2O
2H2↑+O2↑
D . NaOH+HCl═NaCl+H2O
 H2O+CO↑,下列说法错误的是( )
H2O+CO↑,下列说法错误的是( )


-
(1) 湿法炼铜:Fe+CuSO4=Cu+FeSO4 , 反应生成物中盐的名称为 ;
-
(2) 干法炼铜:CO+CuO
 Cu+CO2 , 这是利用CO的性。
Cu+CO2 , 这是利用CO的性。

 2Fe + 3CO2
B . 2H2O2
2Fe + 3CO2
B . 2H2O2  2H2O + O2↑
C . 2CuO + C
2H2O + O2↑
C . 2CuO + C  2Cu + CO2↑
D . 2Cu + O2
2Cu + CO2↑
D . 2Cu + O2  2CuO
2CuO

-
(1) 在上述两个实验中氢气和木炭表现出相同的化学性质是性。
-
(2) 实验步骤的先后次序非常重要,比如甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生爆炸;反应结束后必须先后,否则生成的红色的铜会变成黑色。
-
(3) 某同学正确操作做完乙实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡这说明该反应并没有生成。
-
(4) 该同学查阅资料得到关于铁的氧化物如下信息:
铁的氧化物化学式
Fe2O3
Fe3O4
FeO
颜色
红
黑
黑
化学性质
可溶于酸
常温下不溶于稀酸
可溶于酸
根据以上信息,试写出乙实验试管中反应的化学方程式。
经分析后,该同学试着提高反应温度后,实验出现了预期的现象。

试回答:
-
(1) 该装置存在的一个明显的缺陷,你的改进方法是:。
-
(2) 实验开始时,为什么要先通一会一氧化碳,再给A处的氧化铜加热?。

-
(1) B装置中盛放足量浓氢氧化钠溶液,其作用是。
-
(2) C装置中发生的化学方程式是。
-
(3) A装置和D装置完全相同,其作用的不同之处是。
-
(4) 为了将氧化铁还原成铁,C、E点燃的顺序是,熄灭的顺序是
-
(5) 该小组同学认为废气中的一氧化碳可以利用,于是设计如图2装置除去废气中的二氧化碳,并收集一瓶一氧化碳,准备进行后续的探究。其中最合理的装置是,瓶内盛放的液体是。


 2Fe+CO2
D . 尾气处理时发生反应的化学方程式为2CO+O2
2Fe+CO2
D . 尾气处理时发生反应的化学方程式为2CO+O2  2CO2
2CO2

-
(1) 实验过程中,氧化铜粉末变成红色,这时因为氧化铜发生(填“氧化”或“还原”)反应。
-
(2) 甲装置中浓硫酸的作用。
-
(3) 实验过程应先点燃处(填“乙”或“丙")酒精灯。


-
(1) 写出B装置玻璃管内发生反应的化学方程式为。
-
(2) 若没有A装置,则该实验不能达到检验气体生成物的目的,请说明原因。
-
(3) 5.6克铁粉样品(含有杂质铝或铜中的一种)与足量的盐酸反应产生0.19克氢气,则该样品的组成为,将一定量的该样品加入到硝酸镁和硝酸银的混合溶液中,待反应结束后,过滤在残渣中加入适量的稀盐酸有气泡,产生则滤液中一定含有的溶质是 。
实验室可用下图装置模拟工业炼铁.

-
(1) 装置图末端的导气管口放一盏燃着的酒精灯,这样做的目的是。
-
(2) 若工厂用100吨含Fe2O3的质量分数为80 %的铁矿石炼铁,可提炼出含铁的质量分数为96 %的生铁多少吨?(计算结果保留一位小数)
- 2014年2月12日新疆于田县发生7.3级地震,政府相关部门立即安排了救援行动。据此回答8~9题。 8.在第一时间掌握整
- 第二次工业革命极大地促进了世界经济的互动的整体化趋势,世界市场进一步发展。为论证该观点,你将选择的证据是( ) ①
- 选出划线词词性不同的一项 A 老者安之,朋友信之,少者怀之 B 诲女知之乎 C 之祭者,乞其余 D 禹、汤被之矣
- 一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量分数如 下:物质 甲 乙 丙 丁 反应前质量分数 48
- 词汇运用 根据句子意思,用括号中所给汉语提示或英语单词的适当形式填空。写出空缺处所填单词的正确形式。(每空一词) 1.
- 农贸市场上有新鲜的白菜、萝卜、大葱等多种蔬菜,还有活的鸡、猪、鲜蘑菇,以及附着在这些蔬菜、鸡、猪等上面的细菌等微生物,它
- 2008年6月13日,中共中央、国务院在京召开省区市和中央部门主要负责同志会议。会议指出要按照“一省帮一重灾县”的原则,
- 王安石认为可以“广积蓄,平物价,使农人有以赴时趋事,而兼并不得乘其急”的变法措施是 ( ) A.青苗法
- 已知k∈Z,=(k,1),=(2,4),若||≤4,则△ABC是直角三角形的概率是___________.
- 下列动物中能在空中飞行的无脊椎动物是 ( ) A、蝙蝠
- This is a nice room. It’s . A. Bob’ andFran
- 若纯虚数满足(其中是虚数单位,是实数),则 ()A. B. C.-4 D.4
- 美国夏威夷联合天文中心的科学家发现了氢的新微粒,该微粒是由3个氢原子核(只含质子)和2个电子构成,关于这种微粒的下列说法
- 补写出下列名篇名句中的空缺部分。 (1)敏而好学,____________________,是以谓之文也。(《论语·公冶
- 下列关于有机物在空气中燃烧的说法正确的是( )A.只有碳的氧化物和水B.只有CO2和水C.可能有碳的氧化物、水及其
- 13......
- 小明用如图7所示的电路,探究影响金属丝电阻大小的因素,他手边除了有电路中的器材外,还有一根金属丝,则( )
- 复合肥硝酸钾(KNO3)中,氮元素的化合价为() A.+3 B.+4 C.+5 D.+7
- 甲、乙、丙、丁四种物质分别含两种或三种元素,它们的每个分子中均含18个电子。甲是气态氢化物,在水中可分步电离出两种阴离子
- 解不等式组



