有关化学式的计算和推断 知识点题库
葡萄糖是重要的糖类物质,其化学式为C6H12O6 , 下列有关它的叙述错误的是( )
A . 葡萄糖属于有机化合物
B . 葡萄糖是由碳、氢、氧三种元素组成的
C . 一个葡萄糖分子由6个碳原子和6个水分子构成
D . 葡萄糖在人体内缓慢氧化为二氧化碳和水
2015年,我国科学家屠呦呦获得诺贝尔生理学或医学奖。她提取的青蒿素化学式为C15H22O5 , 下列关于C15H22O5的说法正确的是( )
A . 每个分子的质量为282克
B . 氧元素的质量分数最大
C . 碳、氢、氧元素属于金属元素
D . 碳、氢、氧原子个数比为15∶22∶5
与其他食品中的钙相比,牛奶是最优质的钙源。牛奶中的钙约有30%为可溶性钙,在可溶性钙中约有10%为磷酸钙。磷酸钙的化学式为Ca3(PO4)2。请计算:
-
(1) 磷酸钙的相对分子质量。
-
(2) 磷酸钙中钙元素与氧元素的质量比。
-
(3) 磷酸钙中钙元素的质量分数(精确到1%)。
-
(4) 若每100毫升牛奶含钙元素100毫克,则100毫升牛奶含磷酸钙的质量是多少?(精确到0.1毫克)
俗话说“骨头的精髓在汤里”。有人认为骨头中钙、磷含量雄厚,骨头汤必然钙含量很高,是补钙的好材料。为了验证骨头汤能否有效补钙,某科研小组将猪排骨 500g、蒸馏水 1500mL、食用醋
70mL,加热煮沸后维持 70 分钟,得到骨头汤 1243mL,用仪器检测结果:每 100mL 骨头汤含有 2mg 钙(而每 100mL 牛奶约含有 105mg 钙)。
查阅资料:人体骨骼中的钙存在形式是羟基磷酸钙[Ca10(PO4)6(OH)2],该物质难溶于水。人体平均每天需要补钙 800mg。
-
(1) “骨头汤能补钙”中的钙是指 (填字母编号);A . 钙离子 B . 单质钙 C . 钙元素 D . 羟基磷酸钙
-
(2) 羟基磷酸钙中磷元素的化合价是价 ;
-
(3) 假设某人只能从骨头汤中获取钙,则此人每天需要喝L 骨 头 汤 ;
-
(4) 某品牌钙片每片的规格是:维生素 D3100IU(相当于 2.5 微克),碳酸钙 1000mg,若某人只从钙片中获取钙,则每天需要服用此品牌钙片片。
浓硫酸具有脱水性,能把小木棍、蔗糖等中的氢元素和氧元素“脱出”结合生成水。
-
(1) 用小木棍蘸取浓硫酸少许,一段时间后,小木棍上出现的实验现象是。
-
(2) 在蔗糖(C12H22O11)分子中,氢、氧原子个数比是。如果蔗糖完全脱水,则生成C和H2O的质量比是。
-
(3) 将44克有机物完全燃烧,生成88克CO2和36克H2O(无其他产物).已知该有机物的相对分子质量为88,则44克有机物中含碳元素克,该有机物的化学式为.
甲醛(化学式为CH2O)是室内污染物的主要成分之一,它来源于室内装璜所用的油漆、胶合板等材料。
-
(1) 甲醛属于化合物(填“无机”或“有机”)。
-
(2) 每个甲醛分子共由个原子构成。
-
(3) 甲醛中C、H、O三种元素的质量比为。
在CO、HCOOH、OHC-COOH的混合物中,已知氢元素的质量分数为y,则碳元素的质量分数为( )
A . 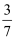 (1-9y)
B .
(1-9y)
B . 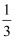 (1-y)
C .
(1-y)
C . 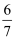 (1-y)
D .
(1-y)
D . 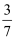 (1-6y)
(1-6y)
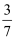 (1-9y)
B .
(1-9y)
B . 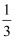 (1-y)
C .
(1-y)
C . 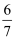 (1-y)
D .
(1-y)
D . 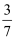 (1-6y)
(1-6y)
肉毒碱(化学式为C7H15NO3)是一种具有多种生理功能的物质,被公认为人体必需的营养物质和最佳的减肥营养素。下列关于肉毒碱的叙述错误的是( )
A . 由四种元素组成
B . 该物质的各元素中,氮元素质量分数最小
C . 相对分子质量为161
D . 碳、氢、氮、氧四种元素的质量比为7:15:1:3
在国庆阅兵中,受阅飞机编队在空中留下彩色的烟带。尾烟是由军事专用的拉烟罐喷射出来的,拉烟罐内物质的主要成分为六氯乙烷和氧化锌等,可发生化学反应生成具有酸性的ZnCl2气溶胶。以下有关说法正确的是( )
A . ZnCl2是由氯化锌分子构成的
B . 六氯乙烷和氧化锌都属于有机材料
C . 若不小心吸入这种烟,会损伤身体,可用小苏打溶液治疗
D . 六氯乙烷的化学式为CCl3CCl3 , 则相对分子质量为237克
2020 年4月,国家药监局下发的《药品补充申请批件》显示,连花清瘟胶囊(颗粒)被批准可用于新冠病毒性肺炎轻型引起的发热、咳嗽、乏力,根据化合物的光谱分析发现连花清瘟胶囊总浸膏中含有连翘脂素(C29H36O15) 等18种化合物,请通过分析计算回答下列问题:
-
(1) 连翘脂素属于(填“无机物”或“有机物”)。
-
(2) 连翘脂素中碳、氢、氧三种元素的原子个数比为。
-
(3) 试计算312g连翘脂素中碳元素质量为多少?
“面对突如其来的严重新冠疫情,中国同世界各国携手合作、共克时艰,为全球抗疫贡献了智慧和力量。”研究表明某品牌消毒液,其主要成分是酒精(C2H5OH),可有效杀灭病毒。

-
(1) 酒精中碳原子、氢原子、氧原子的个数比;
-
(2) 酒精中氧元素的质量分数是。(保留到0.1%)
下图装置是用燃烧法来确定有机物组成的常用装置,这种方法是在电炉加热时用纯氧气氧化硬质玻璃管内样品,根据氧化产物的质量确定有机物的组成(在装置中C里的氧化铜是确保有机物中的碳元素完全转化为二氧化碳).请回答有关问题:

-
(1) 写出A装置中发生反应的化学方程式.
-
(2) 若去掉B装置会对元素的测定结果有影响。
-
(3) 若准确称取1.12克样品(样品只含C、H、O三种元素中的两种或三种).经充分燃烧,D装置增重1.44克,E装置增重3.52克,则该有机物样品中所含的元素为.
我国铁路进入“高铁”时代,为将短轨连成长轨,常用下列反应进行焊接:8Al+3X  4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作。其中X的化学式为,该反应所属基本反应类型为,反应时会(填“吸收”或“放出”)热量。
4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作。其中X的化学式为,该反应所属基本反应类型为,反应时会(填“吸收”或“放出”)热量。
 4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作。其中X的化学式为,该反应所属基本反应类型为,反应时会(填“吸收”或“放出”)热量。
4Al2O3+9Fe,该反应发生后,不需要再持续加热就可保持高温继续进行,方便野外操作。其中X的化学式为,该反应所属基本反应类型为,反应时会(填“吸收”或“放出”)热量。
2017年5月,我国在南海首次试采可燃冰成功。
材料一:可燃冰的化学式为CH4·8H2O,相对分子质量为160,它是由甲烷气体与水在高压低温务件下形成的类冰状水合物,可燃冰热值高,储藏量大,燃烧不产生污染物。
材料二:将CO2注入海底的可燃冰储层,能将可燃冰中的CH4 “挤走”,而形成二氧化碳水合物。
回答下列问题:
-
(1) 写出甲烷(CH4)燃烧的化学方程式。
-
(2) CH4·8H2O属于(选填“有机物”或“无机物”)。CH4·8H2O中碳元素的质量分数为。
-
(3) 下列关于可燃冰的说法正确的是 。A . 可燃冰是一种清洁能源 B . 甲烷和水形成可燃冰的过程是化学变化 C . 用CO2 “挤走”可燃冰中CH4的过程属于置换反应
甲烷(CH4)分子结构的比例模型如图,下列说法正确的是( )


A . 一个甲烷分子由五个原子构成
B . 四个氢原子在同一平面上
C . 甲烷中碳、氢两种元素质量比为1∶4
D . 甲烷中氢元素质量分数为80%
下列判断正确的是( )
A . 微粒的大小:分子>原子
B . 相对分子质量:H2O>H2O2
C . 碳元素的质量分数:C2H4<C3H6
D . 一个分子中的质子总数:H2O= NH3
过氧乙酸(分子模型如图)能有效杀灭病毒。下列关于过氧乙酸的说法中正确的是( )

A . 过氧乙酸的分子式为CH3COOH
B . 过氧乙酸是由碳、氢、氧三种原子构成
C . 过氧乙酸的相对分子质量是76
D . 过氧乙酸中碳元素的质量分数最大
有A、B两种物质组成的混合物四份,总质量均为12克。A和B在一定条件下可发生化合反应生成物质C。四份混合物内所含A和B的质量以及充分反应后生成C的质量如表所示。
|
物质 |
第一份 |
第二份 |
第三份 |
第四份 |
|
反应前A的质量(克) |
11 |
8 |
a |
|
|
反应前B的质量(克) |
1 |
4 |
b |
|
|
反应后生成C的质量(克) |
5 |
10 |
7.5 |
-
(1) 第一份混合物中参加反应的A和B的质量比为。
-
(2) 第二份混合物在反应结束后,反应物中的有剩余。
-
(3) 若第三份混合物恰好能完全反应,则a的值是 。
-
(4) 第四份混合物反应前,A和B的质量比为 。
模型可以反映客观现象,简单明了地表示事物。
-
(1) 提起压在容器中水面上方的活塞,容器中的水发生汽化,如下图所示。则右下图中最能表示水汽化后在相同空间内粒子分布的是 (从A,B,C,D中选一个)并说出理由。

-
(2) 某矿石样品中可能含有碳酸钙、二氧化硅、氧化铝、氧化铁等化合物,经测定各元素质量分数的模型如图甲。由此可推测,该样品中不可能含有的化合物是。
-
(3) 图乙是小明同学模仿甲图构建的尿素[CO(NH2)2]中各元素质量分数的模型,则图中的A表示的是元素。

疫情防控期间用到一种免洗手消毒凝胶,其中含有正丙醇(化学式为C3H8O)。
-
(1) 正丙醇中有种元素;
-
(2) 正丙醇的相对分子质量为;
-
(3) 正丙醇中H、C、O元素的质量比为(最简整数比)。
最近更新
- 玉米的甜和非甜是一对相对性状,随机取非甜玉米和甜玉米进行间行种植,其中一定能够判断甜和非甜的显隐性关系的是()
- 在我国,人民政协和人民代表大会都对国家事务和国家机关实施监督。对这两种监督的认识正确的是 ①政协监督的基本方式是听取“一
- 在△ABC中,·=1,·=-2,则||的值为A.1 B.3
- 在0℃的环境中,把一块0℃的冰投入0℃的水中,将会发生的现象是 ( ) A.冰全部熔化
- Theblue bag _________ be Anna’s. Her bag is red. A. should
- 选出下列词语中没有错别字的一项。( )(2分) A.物竞天择 养精畜锐 冥思苦想 B.按部就班
- That cake is delicious, but I can’t get ______ more. A. any
- 下图为正常人体内肝细胞与内环境之间物质交换的示意图,其中①②③④分别表示体液的成分,a、b、c、d、e分别表示物质运输的
- 12. He sat at the desk ,________a novel. A. read B.
- 一对基因型为XBXb、XbY的夫妇,生了一个基因型为XBXbY的孩子。如果这对夫妇中只有一方在减数分裂时发生异常,且没有
- 实验室中,将98%的浓硫酸稀释成200 g 20%的稀硫酸。请回答下列有关问题: (1)实验仪器有胶头滴管、量筒、细口瓶
- 选出下列加点字读音完全相同的一项( ) A.蛮横 横祸 大发横财 横加指责 B.奔跑 奔走 疲于
- 在空气中能稳定存在的物质是( ) A.石灰水 B.氯水 C.次氯酸钠
- Huge quantities of fresh water ______there since the serious
- 在20世纪40、50年代开始的新技术革命中,奠定了现代信息技术基础、具有划时代意义的发明创造是 ( ) A
- 填写句子,要求与上下文衔接连贯。 我谓江南文化以灵动,水的灵动;我谓西北文化以沉稳,山的沉稳。求之于诗,若 江南
- 在△ABC中,AB=12,AC=10,BC=9,AD是BC边上的高.将△ABC按如图所示的方式折叠,使点A与点D重合,折
- 英法联军在广州实行的殖民统治结束于 A.1857年 B.1858年 C.1859年 D.1860年
- Everyone should fight for the_______ of their own country.
- 如图所示,在直角坐标系的方格纸中将△DEF经过平移、旋转、翻折等变换得到△OPQ.写出变换步骤,并画出相应的图形,在变换



