专题4 硫与环境保护 知识点题库
下列实验装置图所示的实验操作或实验仪器,不能达到相应实验目的的是( )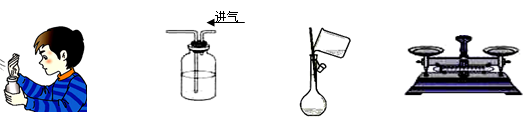
A B C D
A . 闻气体的气味
B . 用浓硫酸干燥氯气
C . 向容量瓶中转移液体
D . 称量2.1g氯化钠
下列关于SO2的说法中,不正确的是( )
A . SO2是硫及某些含硫化合物在空气中燃烧的产物
B . SO2具有漂白性,可以使品红溶液褪色
C . SO2与水反应生成H2SO4
D . SO2是一种大气污染物,它主要来自于化石燃料的燃烧
已知X为一种常见酸的浓溶液,能使蔗糖变黑.A与X反应的转化关系如图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
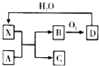
A . 若A为碳单质,则将C通入少量的澄清石灰水中,一定可以观察到白色沉淀产生
B . 若A为铁,则足量A与X在室温下即可完全反应
C . X使蔗糖变黑的现象主要体现了X的脱水性
D . 工业上,B转化为D的反应条件为高温、常压、使用催化剂
化学与生活、社会可持续发展密切相关,下列叙述错误的是( )
A . CO2的大量排放会导致酸雨的形成
B . 黄河三角洲的形成体现了胶体聚沉的性质
C . 推广使用燃料电池汽车,可减少颗粒物、CO等有害物质的排放
D . 轮船上挂锌锭防止铁腐蚀,属于牺牲阳极的阴极保护法
现有下列三个氧化还原反应:①2B-+Z2=B2+2Z- ②2A2++B2=2A3++2B- ③2XO4-+10Z-+16H+=2X2++5Z2+8H2O,根据上述反应,判断下列结论中正确的是( )
A . 要除去含有A2+、Z-和B-混合溶液中的A2+ , 而不氧化Z-和B- , 应加入B2
B . 氧化性强弱顺序为:XO4-﹥Z2﹥A3+﹥B2
C . X2+是XO4-的氧化产物,B2是B-的还原产物
D . 在溶液中不可能发生反应: XO4-+5A2++8H+=X2++5A3++4H2O
以下物质间的每步转化,不能通过一步反应实现的是( )
A . S→SO2→SO3
B . Al→Al2O3→Al(OH)3
C . Fe→FeCl2→Fe(OH)2
D . NH3→NO→NO2
近年来人们为改善空气质量,治理雾霾而启动了“蓝天工程”,根据你所学知识,判断下列措施不利于“蓝天工程”建设的是( )
A . 把燃煤的火力发电厂的烟囱造高,减少酸雨的污染
B . 实施绿化工程,防治扬尘污染
C . 发展新能源汽车,减少传统燃油车的尾气污染
D . 推广使用燃煤脱硫技术,有效减少SO2的污染
下列说法正确的是( )
A . Cl2、SO2均能使品红溶液褪色且褪色的原理相同
B . 常温下,铜片放入浓硫酸中,无明显变化,说明铜在冷的浓硫酸中发生钝化
C . Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应
D . 铵盐与浓的强碱的溶液共热都能产生氨气
金属及其化合物的种类很多,我们可以按照“金属单质、金属氧化物、金属氢氧化物、盐”的类别进行研究。A是短周期元素中原子半径最大的金属元素(“→”所指的转化都是一步完成)。
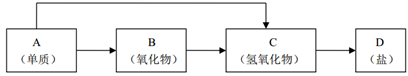
-
(1) A与水反应的离子方程式:。
-
(2) 若B为呼吸面具中的供氧剂,其供氧时每生成1molO2 , 反应过程中转移的电子数为(用NA表示阿伏加德罗常数,用含NA的代数式表示)。
-
(3) 200℃时,11.6gCO2和H2O的混合气体与足量的B反应,反应后固体增加了3.6g,则原混合物的平均相对分子质量为。
-
(4) 若称取10.5 g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02 g。如果把剩余的固体全部加入到100 mL 2 mol·L-1的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度(设溶液的体积变化及盐酸的挥发忽略不计)。
-
(5) 某化学反应方程式(未配平):KMnO4+KI+H2SO4→MnSO4+I2+KIO3+K2SO4+H2O,若该反应方程式中I2和KIO3的计量数分别是6和3,请将方程式配平;KMnO4+KI+H2SO4→MnSO4+6I2+3KIO3+K2SO4+H2O,并用单线桥标出电子转移的方向和数目:。
几种含硫物质的转化如图所示(部分产物可能略去)。下列说法错误的是( )
SO2  Na2SO3 溶液
Na2SO3 溶液  Na2SO4溶液
Na2SO4溶液
A . X可以是Na2CO3溶液
B . Y一定是O2
C . 反应①的离子方程式可能为:SO2+2OH- =SO  + H2O
D . SO2、Na2SO3都能使酸性高锰酸钾溶液褪色
+ H2O
D . SO2、Na2SO3都能使酸性高锰酸钾溶液褪色
 + H2O
D . SO2、Na2SO3都能使酸性高锰酸钾溶液褪色
+ H2O
D . SO2、Na2SO3都能使酸性高锰酸钾溶液褪色
2007年2月6日,国务院新闻办公布:中国节能15年共减排二氧化碳18亿吨。关于镁条在二氧化碳气体中燃烧的反应:2Mg+CO2  2MgO+C,下列说法错误的是( )
2MgO+C,下列说法错误的是( )
 2MgO+C,下列说法错误的是( )
2MgO+C,下列说法错误的是( )
A . 该反应属于置换反应
B . 还原性:Mg>C
C . CO2在该反应中作还原剂
D . 氧化性:CO2>MgO
化学与人类生活、生产和社会可持续发展密切相关,下列说法错误的是( )
A . 水华、赤潮等水体污染与大量排放含氮、磷的污水有关
B . 光化学烟雾与氮的氧化物排放有关
C . 医疗废弃物经过处理、消毒后可加工成儿童玩具,变废为宝
D . 因垃圾后期处理难度大,所以应做好垃圾分类,便于回收利用,节约资源
“低碳经济”是以低能耗、低污染、低排放为基础的可持续发展经济模式。下列说法与“低碳经济”不符合的是( )
A . 大力研发新型有机溶剂替代水作为萃取剂
B . 加强对煤、石油、天然气等综合利用的研究,提高燃料的利用率
C . 利用CO2合成聚碳酸酯类可降解塑料,实现“碳”的循环利用
D . 甲烷和乙醇的燃烧热分别是891.0 kJ·mol-1、1366.8 kJ·mol-1 , 利用甲烷更“低碳”
某化学兴趣小组设计如下图所示的实验装置,探究SO2的性质。[部分夹持仪器已略去]
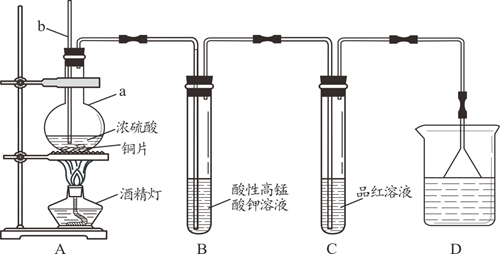
-
(1) [实验探究]
装置A中反应的化学方程式是,仪器a的名称是,导管b的作用是。
-
(2) 实验一段时间后,装置B中观察到现象是。
-
(3) 装置C中溶液褪色说明SO2具有性。
-
(4) 装置D烧杯中盛放的试剂是(填“氢氧化钠溶液”或“浓硫酸”)。
-
(5) 实验结束时需从导管b通入大量空气,其目的是。
-
(6) 用12.8g铜与足量浓硫酸反应,理论上最多可生成LSO2气体(标准状况下)。
-
(7) [知识拓展]
酸雨造成的危害是:(举一例)。
-
(8) 探究SO2形成硫酸型酸雨的途径:将SO2通水入中,测得所得溶液的pH7(填“>”“=”或“<”)。然后每隔1h测定其pH,发现pH逐渐变小,直至恒定,其原因)是(用化学方程式表示)。
研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2 , NO2在上述过程中体现了什么样的性质或起了什么作用:( )
①氧化性;②还原性;③催化剂;④酸性
A . ①③
B . ③④
C . ③
D . ②④
为了减轻酸雨的危害,我国研发了“海水法烟气脱硫(含SO2)”工艺,“海水法烟气脱硫”工艺全过程海水的pH变化大致趋势如图所示。图中最低点硫的主要存在形式是( )
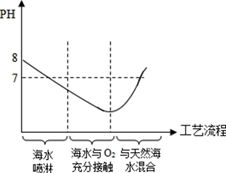
A . SO2
B . SO3
C . H2SO3
D . H2SO4
10℃时,分别向4支小试管中滴加8滴1mol/LCuSO4溶液,再分别向其中滴加2mol/LNaOH溶液,边滴加边振荡,实验数据及现象如下表:
| 试管编号 | 1 | 2 | 3 | 4 |
| 滴加NaOH溶液的量 | 2滴 | 6滴 | 12滴 | 16滴 |
| 立即观察沉淀的颜色 | 浅绿色 | 浅绿色 | 蓝色 | 蓝色 |
| 酒精灯加热浊液后沉淀的颜色 | 浅绿色 | 浅绿色 | 黑色 | 黑色 |
取浅绿色沉淀用蒸馏水反复洗涤,加入稀盐酸完全溶解,再加入适量BaCl2溶液,产生大量白色沉淀。取蓝色沉淀重复上述实验,无白色沉淀。经检验,试管3、4中黑色沉淀中含有CuO。
下列说法错误的是( )
A . 由实验现象可知浅绿色沉淀中可能含有碱式硫酸铜
B . CuSO4溶液与NaOH溶液反应时,其相对量不同可以得到不同的产物
C . 试管3、4中的固体在加热过程中发生了反应:Cu(OH)2  CuO+H2O
D . 取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
CuO+H2O
D . 取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
 CuO+H2O
D . 取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
CuO+H2O
D . 取浅绿色沉淀再滴加适量NaOH溶液后加热仍不会变黑
“蓝天保卫战”需要持续进行大气治理,有效处理  、
、  等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。
等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。
 、
、  等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。
等大气污染物。化学研究为生产、生活处理废气,防止大气污染做出重要贡献。
将  转化为
转化为 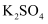 的工艺流程如下,下列说法正确的是( )
的工艺流程如下,下列说法正确的是( )
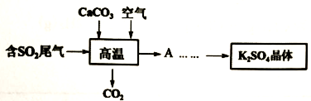
A . 通入空气的目的是将  完全吹出
B . 反应时应将
完全吹出
B . 反应时应将 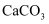 粉碎
C . 固体产物A是
粉碎
C . 固体产物A是 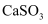 D . “高温”时只发生
D . “高温”时只发生 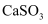 分解反应
分解反应
 完全吹出
B . 反应时应将
完全吹出
B . 反应时应将 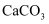 粉碎
C . 固体产物A是
粉碎
C . 固体产物A是 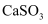 D . “高温”时只发生
D . “高温”时只发生  分解反应
分解反应
关于反应 , 下列说法正确的是( )
, 下列说法正确的是( )
 , 下列说法正确的是( )
, 下列说法正确的是( )
A .  是氧化剂,发生氧化反应
B .
是氧化剂,发生氧化反应
B .  是还原剂,只表现还原性
C . 反应生成18g水时,转移1.2mol电子
D . 还原性:
是还原剂,只表现还原性
C . 反应生成18g水时,转移1.2mol电子
D . 还原性:
 是氧化剂,发生氧化反应
B .
是氧化剂,发生氧化反应
B .  是还原剂,只表现还原性
C . 反应生成18g水时,转移1.2mol电子
D . 还原性:
是还原剂,只表现还原性
C . 反应生成18g水时,转移1.2mol电子
D . 还原性:
为减轻环境污染,提高资源的利用率,可将钛厂、氯碱厂和甲醇厂联合进行生产。生产工艺流程如下:
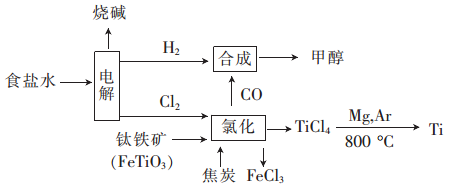
已知:“氯化”过程在高温下进行,且该过程中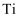 元素的化合价没有变化。下列叙述错误的是( )
元素的化合价没有变化。下列叙述错误的是( )
A . 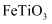 中
中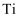 为+4价
B . “合成”过程中原子利用率为
为+4价
B . “合成”过程中原子利用率为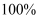 C . “氯化”时发生反应的化学方程式为
C . “氯化”时发生反应的化学方程式为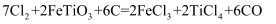 D . 上述流程中生成钛时可用
D . 上述流程中生成钛时可用 代替
代替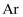
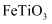 中
中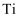 为+4价
B . “合成”过程中原子利用率为
为+4价
B . “合成”过程中原子利用率为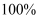 C . “氯化”时发生反应的化学方程式为
C . “氯化”时发生反应的化学方程式为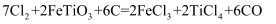 D . 上述流程中生成钛时可用
D . 上述流程中生成钛时可用 代替
代替
最近更新
- 若病人肾功能衰竭,就会出现尿毒症,最终因此而死亡。这一事实不能说明() A.人体维持稳态的调节能力是有一定限度的 B.内
- 如图为经过体外受精和胚胎分割移植培育优质奶牛的过程,请回答下列问题: (1)在进行体外受精前要对精子进行_____处理。
- 宋朝有一条规矩,“官员不入酒肆”,一旦发现官员在酒店吃喝,不管公款私款,即刻遭到御史弹劾,重则罢官免职,轻则纪律处分。另
- 提出“穿衣吃饭,即是人伦物理”的思想家是( ) A. 黄宗羲 B. 李贽 C.王夫之 D.
- 以下说法正确的是() A.分子间距离增大时,分子势能也增大 B.已知某种液体的密度为ρ,摩尔质量为M,阿伏加德罗常数为N
- 已知二次函数的图象如图所示,它与x轴的一个交点坐标为(-1,0),与y轴的交点坐标为(0,3)。(1)求出b,c的值,并
- 下列各项中,对作品故事情节的叙述,不正确的两项是 ( ) A.抄检大观园时,当凤姐和王善保家的抄检到探
- 波兰迅速灭亡的原因包括 ①德军使用“闪电战”新战术 ②波军部署不当,装备落后 ③英法军队未能全力配合
- 某市在第二届人民代表大会常务委员会第三十六次会议上,设立了8个公民旁听席。关于人大常委会,下列认识正确的是 A.是最高
- 针对目前出现的暴力恐怖活动,广大穆斯林(伊斯兰教徒的名称)明确表示,穆斯林与恐怖分子绝无任何关系,不能将宗教与恐怖活动联
- ( )17、姚剧是全国发展最快的剧种。姚剧人继承了前辈经历千辛万苦留下的传统和那些土生土长的姚剧根。同时,在舞美、灯光
- –Do you like watching cooking programs onTV? --No, I
- (08年宣武区质量检一)的值是 ( )A B C
- (11分)(1)H2O2的水溶液为二元弱酸,科学家对H2O2结构的认识经历了较为漫长的过程,最初他们提出了两种观点:a.
- 下面各组加线字读音,与注音全相同的一组是( ) A.恶(è) 恶心 恶意 玩恶作剧 深恶痛绝
- Cancer is a terrible . It kills millions of people every yea
- 为近代中国化学工业做出巨大贡献的人物是( )A、张謇 B、范旭东 C、荣宗敬 D、荣德生
- 一个色盲女人和一个正常男人结婚,生了一个性染色体为XXY的不色盲儿子,此染色体畸变是发生在什么之中? 如果父亲是色盲,母
- 磷元素是植物生长所需的营养元素之一。在元素周期表中,磷元素的某些信息如右图所示,下列有关磷元素的说法不正确的是 A.原子
- 春节期间,在哈尔滨读大学的小强乘火车回广州过年,沿途所见景观最不可信的是( ) A.东北银装素裹 B.



