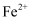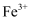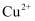第二单元 金属钠及钠的化合物 知识点题库
X、Y、Z、W有如图所示的转化关系,则X、W可能是( )
①C、O2 ②AlCl3、NaOH ③Fe、HNO3 ④CO2、NaOH.
![]()
A . ①②③
B . ①②
C . ③④
D . ①②③④
下列电离方程式正确的是( )
A . NH4Cl⇌NH4++Cl﹣
B . H2S⇌2H++S2﹣
C . K2CO3⇌2K++CO32﹣
D . CH3COONH4=NH4++CH3COO﹣
如表所示,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
A | NaHCO3可用于治疗胃病 | NaHCO3可与盐酸反应 | Ⅰ对,Ⅱ对,无 |
B | 向滴有酚酞的水溶液中加入Na2O2变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
D | Na2O2可为航天员供氧 | Na2O2能与CO2和H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
A . A
B . B
C . C
D . D
下列物质在水溶液中的电离方程式书写正确的是( )
A . HBr  H++Br-
B . HF
H++Br-
B . HF  H++F-
C . NaHSO3===Na++H++SO
H++F-
C . NaHSO3===Na++H++SO 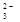 D . NaOH===Na++O2-+H+
D . NaOH===Na++O2-+H+
在含有大量H+、Ba2+、NO3-溶液中,还可以大量共存的离子是( )
A . HCO3-
B . Cl-
C . Fe2+
D . SO42-
能正确表示下列化学反应的离子方程式是( )
A . 石灰石与稀盐酸的反应:CO32-+2H+=H2O+CO2↑
B . Cl2通入水中: Cl2 +H2O=2H++Cl-+ClO-
C . 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓
D . 稀盐酸与铁粉反应:2Fe+6H+=2Fe3++3H2↑
关于强、弱电解质的叙述正确的是( )
A . 强电解质都是离子化合物,弱电解质都是共价化合物
B . 强电解质都是可溶性化合物,弱电解质都是难溶性化合物
C . 强电解质的水溶液中无溶质分子,弱电解质的水溶液中有溶质分子
D . 强电解质的水溶液导电能力强,弱电解质的水溶液导电能力弱
下列各组离子可能大量共存的是( )
A . pH=0的溶液中:Na+、K+、ClO-、AlO2-
B . 能与金属铝反应放出氢气的溶液中: K+、NO3-、Cl-、NH4+
C . 常温下水电离出的c(H+)·c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32-
D . 无色透明溶液:K+、NO3-、Fe3+、SO42-
25℃下,现有0.1mol·L-1的H2SO4和0.1 mol·L-1一元弱酸HA两种溶液。
-
(1) 写出0.1 mol·L-1一元弱酸HA的电离方程式。
-
(2) 0.1mol·L-1的H2SO4中水电离出的C(H+)为。
-
(3) 向0.1mol·L-1的硫酸中加入一定体积的pH=13的NaOH溶液,反应后溶液的pH为2,则所需NaOH溶液与硫酸的体积比为;
-
(4) 向0.1 mol·L-1一元弱酸HA加入一定体积的水,在此过程中,下列数值变大的是。
①c(H+) ②n(A-) ③c(OH-) ④ Ka ⑤c(A-)/ c(HA)
-
(5) 实验室在配制溶液时,一些物质存在水解的情况,在配制Fe2(SO4)3溶液时,Fe3+也存在水解,请书写水解离子方程式。
次磷酸(H3PO2)是一种精细化工产品,回答下列问题。
-
(1) H3PO2是一元中强酸,写出其电离方程式。
-
(2) NaH2PO2是正盐还是酸式盐? 。
-
(3) 次磷酸的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成pH3气体和可溶性盐Ba(H2PO2)2 , 后者再与硫酸反应,写出制备过程中发生的两步离子反应: 。
某无色透明的溶液中只含有Cu2+、Mg2+、Ba2+、H+、Ag+、SO42-、HCO3-、OH-、NO3-中的三种离子,若向其中加入石蕊试剂,溶液显蓝色,则原溶液中能大量存在的离子组是( )
A . Ba2+、OH-、NO3-
B . Ag+、HCO3-、NO3-
C . Mg2+、Ag+、SO42-
D . Cu2+、SO42-、OH-
室温下,下列各组离子在指定溶液中一定能大量共存的是( )
A . c(Al3+)=0.1 mol·L-1的溶液:Na+、NH4 + 、SO42-、NO3-
B . c(Fe3+)=0.1 mol·L-1 的溶液:K+、Ba2+、OH-、SCN-
C . c(NO3-)=0.1 mol·L-1 的溶液:H+、K+、I-、Cl-
D . 水电离的 c(H+)=1×10-13mol·L-1 的溶液:Na+、Mg2+、SO42-、HCO3-
将某碳酸钠和碳酸氢钠混合物 2.74 g加热到质量不再变化时,剩余物质的质量为 2.12 g,求混合物中碳酸钠的质量分数。(写出简要的计算过程)
-
(1) 碳酸氢钠的质量为克?
-
(2) 碳酸钠的质量分数为?
下列反应的离子方程式书写正确的是( )
A . 铝片放入氢氧化钠溶液中: 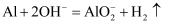 B . Cu与浓硝酸反应:
B . Cu与浓硝酸反应:  C . 向AlCl3溶液中加入过量NaOH溶液:
C . 向AlCl3溶液中加入过量NaOH溶液: 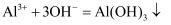 D . AlCl3溶液中滴入过量的氨水:
D . AlCl3溶液中滴入过量的氨水: 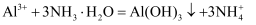
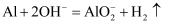 B . Cu与浓硝酸反应:
B . Cu与浓硝酸反应:  C . 向AlCl3溶液中加入过量NaOH溶液:
C . 向AlCl3溶液中加入过量NaOH溶液: 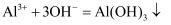 D . AlCl3溶液中滴入过量的氨水:
D . AlCl3溶液中滴入过量的氨水: 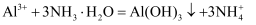
现有含有Fe2+杂质的硫酸铜晶体(CuSO4·5H2O),为了制取纯净的 CuSO4·5H2O),首先将其制成水溶液,然后按图示步骤进行提纯:
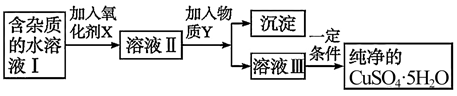
已知:各离子开始沉淀和完全沉淀时的pH如下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| | 6.4 | 9.6 |
| | 1.5 | 3.2 |
| | 4.7 | 6.7 |
请回答下列问题:
-
(1) 加入氧化剂的目的是,最适合的氧化剂X是(填字母)。
A.KMnO4 B.氯水 C.H2O2 D.HNO3
-
(2) 物质Y是(写一种即可)(填化学式)。
-
(3) 本实验用加碱沉淀法能不能达到目的?,原因是。
-
(4) 除去 Fe3+的有关离子方程式为。
-
(5) 请设计一种实验方案检验溶液中Fe3+是否被完全除去(写出操作步骤、现象和结论):。
-
(6) 除铁后得到的 Fe(OH)3可用KClO 溶液在碱性环境中将其氧化得到一种高效的多功能水处理剂——K2FeO4 , 写出该反应的离子方程式:。
下列对应的离子方程式正确的是( )
A . 向偏铝酸钠溶液中加入足量的小苏打: AlO +HCO
+HCO +H2O=Al(OH) 3↓+CO
+H2O=Al(OH) 3↓+CO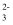 B . 过量氯气通入到FeI2溶液中: 2Cl2+2Fe2++2I-=2Fe3++4Cl- +I2
C . MgSO4 溶液中加入Ba(OH)2溶液: Ba2++ SO
B . 过量氯气通入到FeI2溶液中: 2Cl2+2Fe2++2I-=2Fe3++4Cl- +I2
C . MgSO4 溶液中加入Ba(OH)2溶液: Ba2++ SO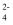 =BaSO4↓
D . NaClO 溶液中通入少量的CO2气体: 2ClO-+ H2O+CO2=2HClO+CO
=BaSO4↓
D . NaClO 溶液中通入少量的CO2气体: 2ClO-+ H2O+CO2=2HClO+CO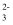
 +HCO
+HCO +H2O=Al(OH) 3↓+CO
+H2O=Al(OH) 3↓+CO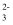 B . 过量氯气通入到FeI2溶液中: 2Cl2+2Fe2++2I-=2Fe3++4Cl- +I2
C . MgSO4 溶液中加入Ba(OH)2溶液: Ba2++ SO
B . 过量氯气通入到FeI2溶液中: 2Cl2+2Fe2++2I-=2Fe3++4Cl- +I2
C . MgSO4 溶液中加入Ba(OH)2溶液: Ba2++ SO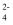 =BaSO4↓
D . NaClO 溶液中通入少量的CO2气体: 2ClO-+ H2O+CO2=2HClO+CO
=BaSO4↓
D . NaClO 溶液中通入少量的CO2气体: 2ClO-+ H2O+CO2=2HClO+CO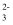
下列各组离子在指定溶液中一定可以大量共存的是( )
A . 使石蕊变红的溶液:Na+、Fe3+、SO32-、Cl-
B . 饱和SO2的水溶液中:NH4+、Fe3+、NO3-、SO42-
C . 在强碱性溶液中:Na+、K+、AlO2-、CO32-
D . 加入铝粉放出氢气的溶液:K+、Ba2+、SO42-、NO3-
回答问题
-
(1) 现有以下物质:①NaCl固体;②CO2;③液态醋酸;④石墨棒;⑤盐酸;⑥酒精(C2H5OH)⑦熔融K2SO4;请回答下列问题(用序号填写);
其中能导电的是 ;属于电解质的是 ;属于非电解质的是 。
-
(2) 某河道两旁有甲、乙两厂。它们排放的工业废水中,共含 K+、Ag+、Cu2+、OH-、Cl-和
 六种离子。
六种离子。①甲厂的废水明显呈碱性,故甲厂废水中含有的三种离子是;
②乙厂的废水中含有另外三种离子。如果加一定量(选填:活性炭、硫酸亚铁、铁粉),可以回收其中的金属
 填写金属元素符号
填写金属元素符号 。
。③另一种设想是将甲厂和乙厂的废水按适当的比例混合,可以使废水中的
 填写离子符号
填写离子符号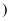 转化为沉淀。经过滤后的废水主要含,可用来浇灌农田。
转化为沉淀。经过滤后的废水主要含,可用来浇灌农田。
下列叙述错误的是( )
A . 当光束通过氢氧化铁胶体时可以看到一条光亮的通路,是因为分散质粒子直径介于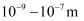 之间,对光线的散射形成的
B . 同温同压下,两种气体的体积不同,是因为分子体积不同
C . 英国科学家道尔顿于1803年提出原子学说,为近代化学的发展奠定了基础
D . 侯德榜发明联合制碱法,为我国的化学工业发展和技术创新作出了重要贡献
之间,对光线的散射形成的
B . 同温同压下,两种气体的体积不同,是因为分子体积不同
C . 英国科学家道尔顿于1803年提出原子学说,为近代化学的发展奠定了基础
D . 侯德榜发明联合制碱法,为我国的化学工业发展和技术创新作出了重要贡献
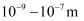 之间,对光线的散射形成的
B . 同温同压下,两种气体的体积不同,是因为分子体积不同
C . 英国科学家道尔顿于1803年提出原子学说,为近代化学的发展奠定了基础
D . 侯德榜发明联合制碱法,为我国的化学工业发展和技术创新作出了重要贡献
之间,对光线的散射形成的
B . 同温同压下,两种气体的体积不同,是因为分子体积不同
C . 英国科学家道尔顿于1803年提出原子学说,为近代化学的发展奠定了基础
D . 侯德榜发明联合制碱法,为我国的化学工业发展和技术创新作出了重要贡献
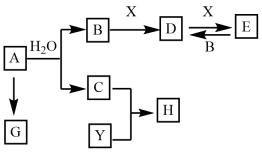
如图所示物质之间的转化,已知:A是金属单质,且焰色试验为黄色,Y是非金属单质,且呈黄绿色,X为常见温室气体。按要求回答下列问题:
-
(1) D的化学式:。
-
(2) A→B的离子方程式:。
-
(3) C在Y中燃烧的实验现象:。
-
(4) 下列说法正确的是。
a.D、E两种溶液,可以滴加氢氧化钙溶液鉴别,也可以滴加氯化钙溶液鉴别
b.A在Y中加热反应,有黄色火焰产生
c.若G是A在空气中加热生成的,则在一定条件下G能转化为B,但不能转化为D
d.将A投入到E的溶液中,也会有D生成
-
(5) C与Y反应后的混合气体通入200mL2.0 mol∙L−1的NaOH溶液中,NaOH恰好完全反应,产物中存在YO-(与消毒液有效成分相同的阴离子),其物质的量为0.1mol,则C与Y的物质的量之比为:。
最近更新
- 联合国气候变化框架公约《京都议定书》要求发达国家限制CO2等温室气体的排放量,以控制日趋严重的温室效应。 试回答下列问题
- 对于惯性的大小,下面说法中正确的是A两个质量相同的物体,在阻力相同的情况下,速度大的不容易停下来,所以速度大的物体惯性大
- 明成祖时,有人主张对入贡互市的外商征税,明成祖答复:“今夷人慕义远来,乃侵其利,所得几何?而亏辱大体多矣”。对此认识正确
- 下列叙述中,不正确的个数有( )①所有的正数都是整数②一定是正数 ③无限小数一定是无理数④没有平方根 ⑤的平方
- 执行右图所示的程序框图,则输出__ ___.
- “以史为鉴,勿忘国耻”。近代使上海蒙辱开放为通商口岸的第一个不平等条约是 A.《南京条约》 B.《北京条
- 2、根据中国古代宗法制,能够继承周王王位的人首先是( ) A、周王最聪明的儿子
- 阅读下面一首唐诗,然后回答问题。 移家别湖上亭 戎昱 好是春风湖上亭,柳条藤蔓系离情。 黄莺久住浑相识,欲别频啼四五声。
- 亚洲东部和南部的冬季风和夏季风分别来自( )。 A.亚欧大陆和太平洋、北冰洋 B
- 能增加反应物分子中活化分子的百分数的是 A.降低温度 B.使用催化剂 C.增大压强 D.增加浓
- 用铜作催化剂,使1-丙醇氧化为某有机物,下列物质中,与该有机物互为同分异构体是 A. CH3OCH2
- 一圆锥被平行于底面的平面截成一个小圆锥和一个圆台,若小圆锥及圆台的体积分别是y和x,则y关于x的函数图象的大致形状为
- 有口无肛门的动物是 A、海
- 1689年,英国国王威廉接受了阐明议会至高无上的基本原则的文件,虽然这个文件产生并不意味着英国已经成为一个民主国家,但
- She isn' t good ___________ maths. Could you help her ______
- 下列汉字书写没有错误的一组是( ) A.度假 内讧 水笼头 彬彬有礼 B.起讫
- 已知点A(-2,0),B(2,0),若点P(x,y)在曲线+=1上,则|PA|+|PB|=____________.
- 探究弹力和弹簧伸长的关系时,在弹性限度内,悬挂15 N重物时,弹簧长度为0.16 m;悬挂20 N重物时,弹簧长度为0.
- 若,则下列不等式中正确的是( ) A. B. C. D.
- 静电透镜是利用静电场使电子束汇聚或发散的一种装置,其中某部分静电场的分布如图所示.虚线表示这个静电场在xOy平面内的一簇