实验活动3 同周期、同主族元素性质的递变 知识点题库
下列叙述正确的是( )
A . Li在氧气中燃烧只生成Li2O
B . 将SO2通入过量BaCl2溶液可生成BaSO3沉淀
C . 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色
D . 将稀硫酸滴加到Fe(NO3)2溶液中无明显现象
下列关于碱金属的原子结构和性质的叙述中不正确的是( )
A . 碱金属原子最外层都只有一个电子,在化学反应中容易失去
B . 碱金属单质都是强还原剂
C . 碱金属单质都能在O2中燃烧生成过氧化物
D . 碱金属单质都能与水反应生成碱
已知:在金属活动顺序表中,钾(K)排在钠的前面,请预测钾单质可能与下列哪类(非金属单质、某些氧化物、酸、盐)物质反应(已知:钾在化合物中的化合价为+1价).(注:每类写一种物质反应即可)
(1)K单质与 反应 化学方程式:
(2)K单质与 反应 化学方程式:
(3)以上预测你应用了哪些研究物质性质的基本方法: .
下列关于砹(85At)及其化合物的说法中,正确的是( )
A . 稳定性:HAt>HCl
B . 氧化性:At2>I2
C . At2为分子晶体
D . NaAt的水溶液呈碱性
F、Cl和Br都是 VIIA族元素,关于这三种元素原子的说法正确的是( )
A . 原子半径:F>Cl>Br
B . 最外层电子数都相同
C . 核外电子层数都相同
D . 最外层电子数依次增多
下列说法中正确的是( )
①锂在空气中燃烧生成的Li2O
②Al2(SO4)3可除去碱性废水及酸性废水中的悬浮颗粒
③盐酸既有氧化性又有还原性
④Fe(OH)3、FeCl2、H2SiO3都不能直接用化合反应制备
⑤SO2能使酸性高锰酸钾溶液褪色,所以它具有漂白性.
A . ②③④
B . ①②③
C . ①③
D . ①②
溴的氧化性介于氯和碘之间.利用这一性质判断,下列说法正确的是( )
A . Cl﹣、I﹣离子加入到含Br﹣的溶液中,均可以将Br﹣氧化为Br2
B . 将Cl2缓慢通入含有相同物质的量浓度的Br﹣、I﹣的混合溶液中,Br﹣先被氧化
C . 湿润的淀粉碘化钾试纸遇到氯气会变蓝色
D . 在KBr溶液中加入碘水,发生如下反应:2Br﹣+I2=2I﹣+Br2
与Li<Na<K<Rb<Cs的变化规律不符合的是( )
A . 原子半径
B . 单质熔沸点
C . 与水或酸反应置换氢气的剧烈程度
D . 最高价氧化物对应水化物的碱性
化学科学需要借助化学语言来描述,下列化学用语正确的是( )
A . Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱
B . NH4I的电子式 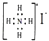 C . 钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比不同
D . Al2O3的化学键类型与AlCl3的化学键类型相同
C . 钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比不同
D . Al2O3的化学键类型与AlCl3的化学键类型相同
关于钠元素的单质及其化合物的叙述中,不正确的是( )
A . 钠是银白色、质软、熔点相对较低、密度比水小的金属单质
B . 大量的钠着火时可以用沙子扑灭
C . 金属钠在空气中长期放置,最终变为碳酸钠
D . 过氧化钠是白色固体
下列关于卤素的叙述说法错误的是( )
A . 单质的颜色随核电荷数的增加逐渐加深
B . 元素的最高化合价均为+7
C . 从上到下原子半径递增
D . 从上到下非金属性减弱
碱金属是典型的活泼金属,其根本原因是( )
A . 碱金属原子最外电子层上都只有1个电子,容易失去
B . 碱金属在常温下易被氧化
C . 碱金属单质的密度小,熔点和沸点低
D . 碱金属原子的核电荷数比较小
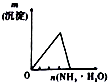
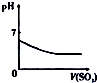
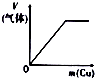
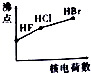
下列相关示意图正确的是( )
A | B | C | D |
将氨水滴到氯化铝溶液中至过量 | 将二氧化碳逐渐通入氯水中至过量 | 将铜粉加入到浓硝酸中至过量 | 卤族元素的氧化物沸点随核电荷数的变化 |
| | | |
A . A
B . B
C . C
D . D
向含有NaBr、NaI的溶液中通入过量的Cl2 , 然后将溶液蒸干,并灼烧固体,最后得到的物质是( )
A . NaCl
B . NaCl和NaBr
C . NaCl和NaI
D . NaCl和I2
卤素单质的性质按  、
、  、
、 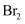 、
、  的顺序依次增强的是( )
的顺序依次增强的是( )
 、
、  、
、 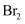 、
、  的顺序依次增强的是( )
的顺序依次增强的是( )
A . 与氢气反应的剧烈程度
B . 非金属活泼性的强弱
C . 对应离子的还原性
D . 氢化物的稳定性
中国传统文化蕴含着很多科学知识,下列说法错误的是( )
A . 唐·王建“内园分得温汤水,二月中旬已进瓜”,所利用的能源为地热能
B . 宋·王希孟《千里江山图》中的绿色颜料铜绿的主要成分是碱式碳酸铜
C . 《梦溪笔谈》记载“以剂钢为刃,柔铁为茎干,不尔则多断折”,说明铁合金的硬度比纯铁的高
D . 《本草纲目》中“石碱”条目下记载“采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面”,这里的“石碱”主要成分是KOH
金属钾在空气中燃烧的产物有过氧化钾和超氧化钾(KO2),超氧化钾的电子式为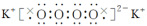 , 简写成KO2;KO2与Na2O2的性质相似,与H2O、CO2都能发生反应,与水反应的方程式为4KO2+2H2O=4KOH+3O2↑。下列有关KO2的说法,不正确的是( )
, 简写成KO2;KO2与Na2O2的性质相似,与H2O、CO2都能发生反应,与水反应的方程式为4KO2+2H2O=4KOH+3O2↑。下列有关KO2的说法,不正确的是( )
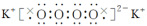 , 简写成KO2;KO2与Na2O2的性质相似,与H2O、CO2都能发生反应,与水反应的方程式为4KO2+2H2O=4KOH+3O2↑。下列有关KO2的说法,不正确的是( )
, 简写成KO2;KO2与Na2O2的性质相似,与H2O、CO2都能发生反应,与水反应的方程式为4KO2+2H2O=4KOH+3O2↑。下列有关KO2的说法,不正确的是( )
A . KO2属于离子化合物,含有离子键和共价键
B . 与水反应,KO2既是氧化剂又是还原剂
C . 与CO2反应,产物是K2CO3和O2
D . 与水反应,若生成1molO2 , 则有2mole-发生转移
由于锂电池的需求急剧增长,全球陷入锂资源“争夺战”。下列有关锂的说法正确的是( )
A . 电解LiCl 熔盐可制取金属Li
B . 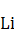 Li 与
Li 与 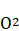 O2 反应能生成
O2 反应能生成 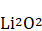 Li2O2
C .
Li2O2
C . 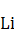 Li 、Cu 及海水构成的电池中,Li 为电池正极
D .
Li 、Cu 及海水构成的电池中,Li 为电池正极
D . 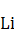 Li 的原子半径是第二周期所有主族元素中原子半径最小的
Li 的原子半径是第二周期所有主族元素中原子半径最小的
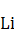 Li 与
Li 与 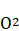 O2 反应能生成
O2 反应能生成 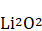 Li2O2
C .
Li2O2
C . 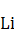 Li 、Cu 及海水构成的电池中,Li 为电池正极
D .
Li 、Cu 及海水构成的电池中,Li 为电池正极
D . 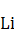 Li 的原子半径是第二周期所有主族元素中原子半径最小的
Li 的原子半径是第二周期所有主族元素中原子半径最小的
下列有关物质的性质与用途不具有对应关系的是( )
A . 铝合金耐腐蚀,可用于制造门窗
B . 硫酸钡难溶于水和酸,可用作医疗钡餐
C . 干冰易升华,可用于人工降雨
D . 钾的金属性比钠强,工业上可用钠制取钾
有关单质钾的说法如下:①在 中燃烧生成
中燃烧生成 并能产生紫色火焰;②与
并能产生紫色火焰;②与 溶液反应时能产生蓝色沉淀;③少量单质钾可保存在煤油中;④熔点、沸点均比钠的高。下列组合正确的是( )
溶液反应时能产生蓝色沉淀;③少量单质钾可保存在煤油中;④熔点、沸点均比钠的高。下列组合正确的是( )
 中燃烧生成
中燃烧生成 并能产生紫色火焰;②与
并能产生紫色火焰;②与 溶液反应时能产生蓝色沉淀;③少量单质钾可保存在煤油中;④熔点、沸点均比钠的高。下列组合正确的是( )
溶液反应时能产生蓝色沉淀;③少量单质钾可保存在煤油中;④熔点、沸点均比钠的高。下列组合正确的是( )
A . ②③
B . ①④
C . ③④
D . ①③
最近更新
- X、Y、Z和W代表原子序数依次增大的四种短周期元素,它们满足以下条件:①元素周期表中,Z与Y相邻,Z与W相邻;②X分别与
- .----could you please drive faster. The flight _______- in a
- 原子结构对于元素化学性质关系最密切的是( ) A.电子层数 B.质子数 C.最外层
- 设函数,若为奇函数,则=__________
- 用NA表示阿伏加德罗常数的值,下列说法中正确的是A.46gNO2和N2O4的混合物中含有的原子总数一定是3NAB.500
- 已知五种元素的原子序数的大小顺序为C>A>B>D>E;A、C同周期;B、C同主族;A与B形成的离子化合物A2B中所有离子
- 关于元素周期表的说法正确的是 A.元素周期表有8个主族 B.ⅠA族的元素全部是金属元素
- 对同一样事物,可以有不同的评价,请依照例句,任选一事物(例如:橡皮、黑板、星星、菊花、彩虹、竹……),写两句对人生有警示
- 银行能够把“死钱”变“活钱”,把“小钱”变“大钱”,是通过什么实现的( ) A.吸收存款 B.吸收存款和发放贷款 C.转
- (1)解方程:+1= ; (2)解不等式组:,并写出它的自然数解.
- “子龙鼎”是已发现的商代青铜圆鼎中形体最大的一件,也是带有“龙”字铭文最早的青铜器。通过上述材料,我们可以推测出()
- We are veryglad ______ you . A.see B.to see C.seei
- Have you seen the film “Titanic”, ____ leading actor is wor
- 下列搭配正确的是( ) A.乔托——“欧洲绘画之父” B.达·芬奇——《西斯廷圣母》 C.马基雅维利——《奥赛罗》
- 人体稳态的调节能力是有一定限度的。下列现象属于内环境稳态失调的是 A.寒冷时出现寒颤 B.从平原到高原,有的人出现肺水肿
- 如右图所示食物网中,E是生产者,共含有7.1×109 kJ的能量,B生物种群总能量为2.3×108 kJ,从理论上计算A
- 阅读下面的文字,根据要求作文。 有一老一小两个人同时在沙漠里种胡杨树。年轻人待树苗成活以后,每隔三天就要来给它浇水,而老
- “三国同盟”与“三国协约”两大军事集团的核心分别是 ( ) A.德国 法国 B.奥匈帝国 俄国
- 我国最大的湖泊是( ) A、青海湖 B、鄱阳湖 C、洞庭湖
- 距离地球最近的天体是() A.太阳 B.金星 C.土星 D.月