第2节 氮的循环 知识点题库
下列说法正确的是( )
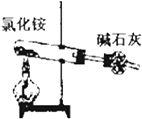 实验室制NH3
B .
实验室制NH3
B . 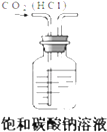 除去CO2中的HCl
C .
除去CO2中的HCl
C . 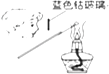 检验K2CO3中的K+
D .
检验K2CO3中的K+
D . 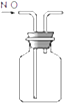 收集NO
收集NO
-
(1) 甲同学取一束细铜丝用砂纸打磨后在酒精灯上加热至红热,再伸到Cl2的集气瓶中.你认为甲同学在实验中应该观察到的现象是.
-
(2) 乙同学为验证Fe在冷的浓HNO3中发生钝化但能和热的浓HNO3反应,设计了如图1、2所示的实验,请你指出其中的两处错误:、;纠正上述错误后,请你从绿色化学的角度出发,对图2装置提出改进建议,使装置既能控制反应的进行,又能减少氮氧化物的排放:.
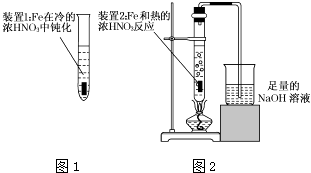
-
(3) 丙同学在Fe和浓HNO3反应后的溶液中加入一块Cu片,Cu片逐渐溶解,反应一段时间后不再溶解(Cu有剩余).
①丙同学依据反应现象得出Cu片溶解的原因是和HNO3发生反应.他依据的反应现象是.
②丁同学认为丙同学的结论不完全正确.他的理由是.
-
(4) 请你设计实验证明在加入Cu片并反应完全后的溶液中含有Fe2+但不含有Fe3+ . 说明具体的操作和实验现象.
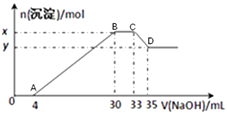
-
(1) B点的沉淀物的化学式为。
-
(2) 原溶液中Cu2+的物质的量为,原溶液中Cl-物质的量浓度为。
-
(3) 原溶液的pH=,x-y= 。
-
(4) 经过滤得到D点的沉淀物,并多次用蒸馏水洗涤沉淀,判断沉淀是否洗涤干净的方法是
 B .
B . 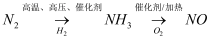 C .
C .  D .
D . 
实验目的 | 实验方案、现象 | 结论 | |
A | 检验溶液中有无NH4+ | 用试管取少量的待检测溶液,加入少量的稀NaOH溶液,用一块湿润的红色石蕊试纸放在试管口 | 若试纸变蓝,则有 NH4+ , 否则无NH4+ |
B | 检验溶液中有无K+ | 用洁净的铂丝蘸取待测液进行焰色反应,火焰呈黄色 | 原溶液中一定无K+ |
C | 检验溶液中有无SO42- | 用试管取少量的待检测溶液,加入稀盐酸无现象,再加入BaCl2溶液,出现白色沉淀 | 原溶液中有SO42- |
D | 检验淀粉水解产物有无还原性 | 用试管取少量的淀粉溶液加入适量的稀硫酸,加热一段时间后,加入少量的新制Cu(OH)2悬浊液,加热至沸腾,产生大量的砖红色沉淀 | 水解产物有还原性 |
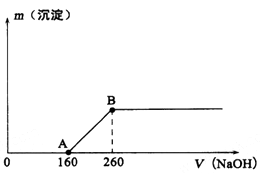
-
(1) B点所表示溶液中只含一种溶质,该物质是(填化学式)。
-
(2) 收集的气体中,NO2的物质的量为mol。
-
(3) 原浓硝酸的浓度为mol/L。
-
(4) 欲使铜与硝酸产生的混合气体在氢氧化钠溶液中全部转化为硝酸钠,至少需要30%的双氧水g(保留两位有效数字)。
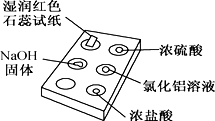
| 选项 | 实验现象 | 解释 |
| A | 红色石蕊试纸变蓝 | NH3极易溶于水 |
| B | 浓硫酸附近无白烟 | NH3与浓硫酸不发生反应 |
| C | 氯化铝溶液变浑浊 | NH3与AlCl3溶液反应:Al3++3OH-=Al(OH)3↓ |
| D | 浓盐酸附近有白烟 | NH3与挥发出的HCl反应:NH3+HCl=NH4Cl |
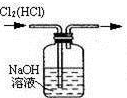 除去氯气中的氯化氢
B .
除去氯气中的氯化氢
B . 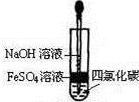 制备Fe(OH)2
C .
制备Fe(OH)2
C . 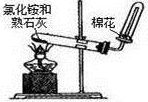 实验室制备氨气
D .
实验室制备氨气
D . 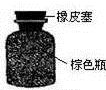 保存浓硝酸
保存浓硝酸
-
(1) 硫酸铵是某地PM2.5雾霾的主要成分,收集一定量的雾霾固体进行验证。取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份盛于试管中:
操作步骤
实验现象
结论
①向其中一份
有白色沉淀生成
证明雾霾固体中含有SO42-
②向另一份中加适量NaOH浓溶液并加热,用镊子夹持湿润的红色石蕊试纸靠近试管口
③试管中有气泡产生,靠近试管口的红色石蕊试纸
证明雾霾固体中含有NH4+。综合上面实验,初步说明雾霾固体颗粒中含有(NH4)2SO4
-
(2) 用如图所示简易装置测定空气中SO2的含量。
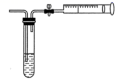
①测定原理:SO2通入碘的淀粉溶液中,溶液由蓝色变为无色,反应的化学方程式为。
②测定方法:在某监测点,量取5.0mL5.0×10-4mol/L的碘溶液,注入图中的试管中,加几滴淀粉指示剂,此时溶液呈蓝色,按图中装置连接好仪器,利用止水夹控制,进行抽气,取下注射器排气,重复操作直到溶液的蓝色全部褪尽为止,共抽取空气8.0L,则测得该监测点空气中SO2的含量为mg/L。
-
(3) 探究H2SO3的部分性质。选用下面的装置和药品探究H2SO3与HClO的酸性强弱。
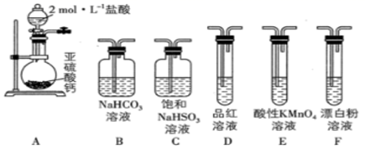
①甲同学认为按照A→C→F→尾气处理的顺序连接装置,可以证明H2SO3与HClO的酸性强弱,乙同学认为该方案不合理,其理由是。
②丙同学采用间接法证明,实验方案为按照A→C→→→→(填字母)→尾气处理顺序连接装置,证明H2SO3的酸性强于HClO的实验现象是。
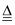 NaCl +N2↑+2H2O
B . 装置II的作用是冷凝水蒸气
C . 装置II末端收集纯净干燥的N2只能用向下排空气法
D . 加热片刻后需要将酒精灯移开,说明该反应是放热反应
NaCl +N2↑+2H2O
B . 装置II的作用是冷凝水蒸气
C . 装置II末端收集纯净干燥的N2只能用向下排空气法
D . 加热片刻后需要将酒精灯移开,说明该反应是放热反应
回答下列问题:
-
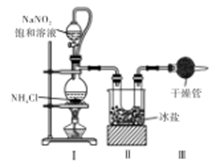
(1) A装置中盛有浓氨水的仪器名称为;B装置中盛有的药品是。
-
(2) E装置的作用是;F装置中发生反应的离子方程式为。
-
(3) C装置内发生置换反应,并有浓厚的白烟产生,则C中发生反应的化学方程式为,该反应中氧化剂与还原剂的物质的量之比为。
-
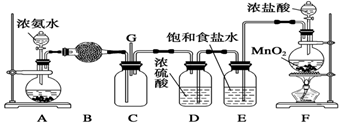
(4) C装置的G处需连接一个装置,可选用图中的(填序号)。
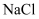 的
的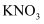 固体,可通过蒸发结晶、趁热过滤的方法
B . 取燃尽的火柴头加水浸泡,滴加
固体,可通过蒸发结晶、趁热过滤的方法
B . 取燃尽的火柴头加水浸泡,滴加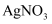 溶液和稀硝酸,可检测火柴头中的氯元素
C . 测定镀锌铁皮锌镀层厚度时,腐蚀后的铁皮烘干时间过长,测得结果偏低
D . 轻微烫伤时,可先用洁净的冷水洗涤伤处,再涂烫伤药膏
溶液和稀硝酸,可检测火柴头中的氯元素
C . 测定镀锌铁皮锌镀层厚度时,腐蚀后的铁皮烘干时间过长,测得结果偏低
D . 轻微烫伤时,可先用洁净的冷水洗涤伤处,再涂烫伤药膏
-
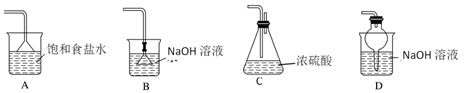
(1) Ⅰ.物质的类别和核心元素的化合价是研究物质性质的两个重要维度。氮及其化合物的转化关系如下图。
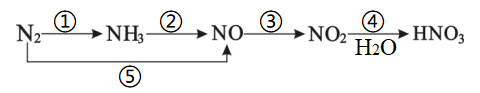
路线①~⑤中表示氮的固定的是(填标号)。
-
(2) 完成路线②的转化,从原理上分析,加入下列试剂可行的是____(填标号)。A .
 B .
B . 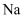 C .
C .  D .
D . 
-
(3) 路线④的反应中氧化剂与还原剂的物质的量之比为。
-
(4) 请用化学方程式说明浓硝酸一般盛放在棕色试剂瓶中的原因。
-
(5) Ⅱ.某同学在实验室制备氨气,准备了一些如图装置。
 为实验室制取氨气的发生装置,反应的化学方程式为。
为实验室制取氨气的发生装置,反应的化学方程式为。 -
(6) 装置
 中仪器的名称为。
中仪器的名称为。
-
(7) 欲收集一瓶干燥的氨气,挑选出上图中的适当装置,其连接顺序为:发生装置
 (按气流方向,用小写字母表示)。
(按气流方向,用小写字母表示)。
- 《大国崛起》的热播说明了人们对历史的喜爱的关注。其中有这样一段:17世纪英国“在历史性的转变中抢占了先机,已经率先到达了
- 一物块停在水中时,露出水面的体积为6×10-6m3,它的总体积为8×10-6m3,求:(1)物块在水中所受的浮力为多大?
- (本小题满分7分)选修:不等式选讲 已知为实数,且, (Ⅰ)求的最小值; (Ⅱ)设,求实数的取值范围.
- X、Y、Z、W均为短周期元素且原子序数依次增大,其中Y、W同主族;常温下,Y、W的单质为有色气体,W气体同冷烧碱溶液作用
- 已知a、b为正数,且a≠b,比较a3+b3与a2b+ab2的大小.
- 古诗文名句、常识默写。(10分)1.善学者尽其理, 。(《荀子》)2.
- (14分)用磁场可以约束带电离子的轨迹,如图所示,宽d=2cm的有界匀强磁场的横向范围足够大,磁感应强度方向垂直纸面向里
- 把下列句子组合成语意连贯的一段话。(只填序号) ①与这儿相距十多里的张家湾消水洞的水就是从此洞流出。②雄伟的高山
- 在固定于地面的斜面上垂直安放一个挡板,截面为 圆的柱状物体甲放在斜面上,半径与甲相等的光滑圆球乙被夹在甲与挡板之间,没
- 对英国国家元首伊丽莎白二世和政府首脑卡梅伦表述正确的是()①卡梅伦的权力受到伊丽莎白二世的制约②如果现在议会通过对政府的
- 若函数在上是奇函数,则的解析式为( ). A. B. C. D
- 二战中,40%的资本主义世界贸易仍用英镑结算,英镑仍然是资本主义世界的一种国际储备货币。英国不满美国的方案,英国财政部顾
- 在相同条件下,将相同物质的量的Na、Mg、Al分别加入盛有相同浓度相同盐酸的甲、乙、丙三支试管中充分反应,生成气体的体积
- 如图所示,下列实验操作与方法正确的是:
- “买船出海,扬帆中国梦”,某传媒股份有限公司成功收购了一家美国当地的传媒企业后,两年建起了16个频道,收视人群超700
- p{font-size:10.5pt;line-height:150%;margin:0;padding:0;}td{f
- 温家宝总理在2010年的政府工作报告中指出,创造条件让人民批评政府、监督政府,让权力在阳光下运行。这意味着( )
- 某灯泡厂生产的一批灯泡的寿命均匀分布在区间[28,98]天内,从这批灯泡中任取一只寿命超过60天的概率为( )A.
- NA代表阿伏加德罗常数的值,以下说法正确的是( ) A.2NA个HCl分子与44.8L H2和Cl2的混合气体所含
- 若函数为奇函数,则



