实验3-1 几种无机离子的检验 知识点题库
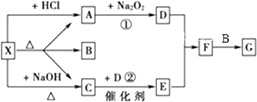
图中每一方格表示有关的一种反应物或生成物,其中A、C为无色气体,请填写下列空白:
-
(1) 物质X可以是,C是,F是.
-
(2) 反应①的化学方程式是,反应②的化学方程式是
-
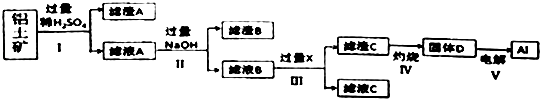
(1) 滤渣A是,滤渣B是.
-
(2) 过程 I、II、III的分离操作的名称是.
-
(3) 过程 IV中灼烧时盛放药品的仪器名称是,发生反应的化学方程式是.
-
(4) 过程 III中发生反应生成滤渣C的离子方程式表示为.
-
(5) 取滤液B100mL,加入1molL﹣1盐酸200mL时,沉淀量达到最大且质量为11.7g.则溶液B中c(AlO2﹣)=,c(Na+)> mol•L﹣1 .
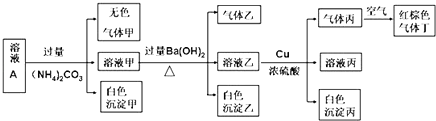
回答下列问题:
-
(1) 溶液A中一定不存在的阴离子有.
-
(2) 生成沉淀甲和沉淀乙的离子方程式分别为.
-
(3) 气体乙的结构式为.
-
(4) 生成气体丙的离子方程式为若实验消耗Cu 144g,则最多生成气体丁的体积(标准状况下)为.
 SiCl4
SiCl4  Si
B . Mg(OH)2
Si
B . Mg(OH)2  MgCl2(aq)
MgCl2(aq)  Mg
C . Fe2O3
Mg
C . Fe2O3  FeCl3(aq)
FeCl3(aq)  无水FeCl3
D . AgNO3(aq)
无水FeCl3
D . AgNO3(aq) 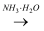 [Ag(NH3)2]OH(aq)
[Ag(NH3)2]OH(aq)  Ag
Ag
-
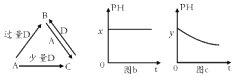
(1) 若A为金属单质,D是某强酸的稀溶液,则反应C+D→B的离子方程式为.
-
(2) 若A为强碱,D为气态氧化物.常温时,将B的水溶液露置于空气中,其pH随时间 t变化可能如上图的图b或图c所示(不考虑D的溶解和水的挥发).
①若图b符合事实,则D的化学式为;
②若图c符合事实,则其pH变化的原因是(用离子方程式表示)
-
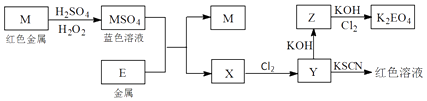
(1) 写出M溶于稀H2SO4和H2O2混合液的化学方程式:.
-
(2) 写出X生成Y的离子方程式:.
-
(3) 某同学取Y的溶液,酸化后加入KI淀粉溶液,溶液变为蓝色.写出与上述变化过程相关的离子方程式:.
-
(4) 写出将Cl2通入足量氢氧化钾溶液中反应的离子方程式:.
-
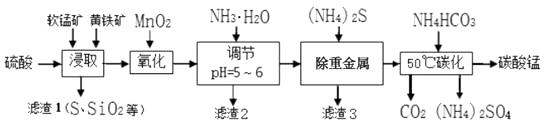
(1) 为了提高锰元素的浸出率,在“浸取”时可采取的措施有:
①适当升高温度,②搅拌,③等。
-
(2) 流程“氧化”中加入MnO2与Fe2+发生反应的离子方程式为。
-
(3) “滤渣2”中主要成分的化学式为。
-
(4) 流程“除重金属”时使用(NH4)2S而不使用Na2S的原因是。
-
(5) 流程“50℃碳化”得到碳酸锰,该反应的化学方程式为。
-
(6) 生成的碳酸锰产品需经充分洗涤,检验产品完全洗净的方法是。
-
(1) b的最小值为。
-
(2) 当b=时,产物中水的质量最多。
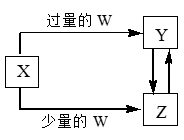
| 选项 | W | X |
| A | 盐酸 | 碳酸钠溶液 |
| B | 氢氧化钠溶液 | 氯化铝溶液 |
| C | 二氧化碳 | 氢氧化钙溶液 |
| D | 氯气 | 铁单质 |
已知生成氢氧化物沉淀的pH如下表所示:
| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀 | 4.2 | 6.5 | 1.5 |
| 完全沉淀 | 6.7 | 9.7 | 3.7 |
-
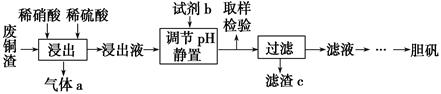
(1) 写出浸出时铜与稀硫酸、稀硝酸反应生成硫酸铜的化学方程式:。
-
(2) 取样检验是为了确认Fe3+是否除净,你的检验方法是。
-
(3) 试剂b是,滤渣c是(均写化学式)。
-
(4) 气体a可以被循环利用,用化学方程式表示气体a被循环利用的原理为2NO+O2=2NO2、。
-
(5) 一定温度下,硫酸铜受热分解生成CuO、SO2气体、SO3气体和O2气体,且n(SO3)∶n(SO2)=1∶2,写出硫酸铜受热分解的化学方程式:。
-
(6) 某同学设计了如下图所示的实验装置分别测定生成的SO2、SO3气体的质量和O2气体的体积。此设计有不合理之处,请说明理由:。
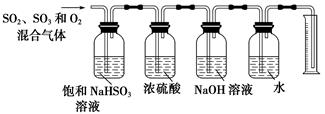
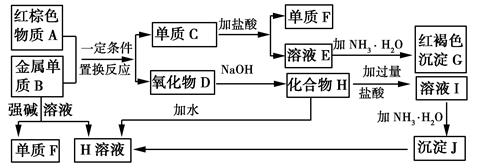
请回答下列问题:
-
(1) 物质A的化学式为。
-
(2) 写出单质B与强碱溶液反应的离子方程式,氧化物D与NaOH溶液反应的化学方程式。
-
(3) 溶液E中加入氨水时,先生成白色沉淀L,L最终变为红褐色沉淀G,写出L变为G的化学反应方程式。
-
(4) 溶液E敞口放置容易变质,写出检验溶液E是否变质的实验操作、现象及结论,为了防止溶液E的变质,可往溶液中加入。
-
(5) 溶液I中所含金属离子是。
-
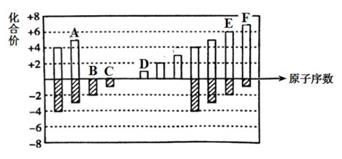
(1) 元素F在周期表中的位置是 。
-
(2) 元素C,D,E原子半径由大到小的顺序是 (填元素符号)。
-
(3) A、B、C的单质与氢气反应的难易程度由易到难的顺序是 (用单质的化学式表示)。
-
(4) 应用元素周期律和元素周期表的知识,写出D和E所形成的化合物的化学式 、(写2种)。
-
(5) D在B单质中燃烧生成的物质电子式为,氢原子与B原子以1:1结合的物质结构式为 。
-
(6) 根据氯、溴、碘单质间的置换反应,判断F的单质和E的最简单氢化物之间能否发生反应(填“能”或“不能”),若能则写出反应的化学方程式 。
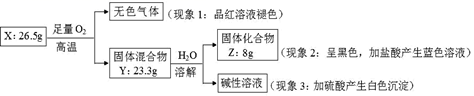
请回答:
-
(1) 由现象 1 得出化合物 X 含有元素(填元素符号),X 的化学式。
-
(2) 固体混合物 Y 的成分(填化学式)。
-
(3) 实验室常将氨气(NH3)通过红热的黑色固体化合物 Z 制备氮气,该反应的化学方程式是,当有28克氮气生成时转移的电子的物质的量为mol。
-
(1) Ⅰ.化合物Ⅹ由四种短周期元素组成,加热X,可产生使湿润的红色石蕊试纸变蓝的气体Y,Y为纯净物;取
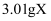 ,用含
,用含 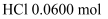 的盐酸完全溶解得溶液A,将溶液A分成
的盐酸完全溶解得溶液A,将溶液A分成 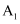 和
和  两等份,完成如下实验(白色沉淀C可溶于
两等份,完成如下实验(白色沉淀C可溶于  溶液):
溶液):
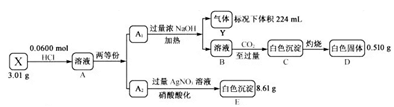
请回答:
组成X的四种元素是N、H和(填元素符号),X的化学式是。
-
(2) 溶液B通入过量
 得到白色沉淀C的离子方程式是。
得到白色沉淀C的离子方程式是。
-
(3) 写出一个化合反应(用化学方程式或离子方程式表示)。要求同时满足:
①其中一种反应物的组成元素必须是X中除N、H外的两种元素;
②反应原理与“
 ”相同。
”相同。 -
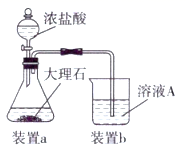
(4) Ⅱ.某兴趣小组为验证浓硫酸的性质进行实验,如图。实验中观察到的现象有:锥形瓶内有白雾,烧杯中出现白色沉淀。请回答:
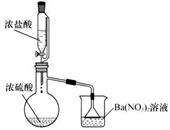
将浓硫酸和浓盐酸混合可产生
 气体的原因是。
气体的原因是。 -
(5) 烧杯中出现白色沉淀的原因是。
-
(1) 司南是由天然磁石制成的,其主要成分是(填字母序号)。
a.Fe b.FeO c.Fe3O4 d.Fe2O3
-
(2) 现代利用铁的氧化物循环裂解水制氢气的过程如下图所示。整个过程与温度密切相关,当温度低于570℃时,Fe3O4(s)和CO(g)反应得到的产物是Fe(s)和CO2(g),阻碍循环反应的进行。
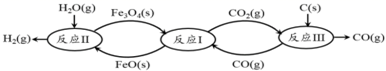
①已知:Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g)ΔH1=+19.3kJ·mol-1
3FeO(s)+CO2(g)ΔH1=+19.3kJ·mol-13FeO(s)+H2O(g)
 Fe3O4(s)+H2(g)ΔH2=-57.2kJ·mol-1
Fe3O4(s)+H2(g)ΔH2=-57.2kJ·mol-1C(s)+CO2(g)
 2CO(g)ΔH3=+172.4kJ·mol-1
2CO(g)ΔH3=+172.4kJ·mol-1铁氧化物循环裂解水制氢气总反应的热化学方程式是。
②下图表示其他条件一定时,Fe3O4(s)和CO(g)反应达平衡时CO(g)的体积百分含量随温度的变化关系。
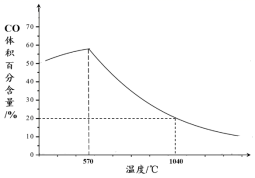
i.反应Fe3O4(s)+4CO(g)
 3Fe(s)+4CO2(g)ΔH0(填“>”、“<”或“=”),理由是。
3Fe(s)+4CO2(g)ΔH0(填“>”、“<”或“=”),理由是。ii.随温度升高,反应Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g)平衡常数的变化趋势是;1040℃时,该反应的化学平衡常数的数值是。
3FeO(s)+CO2(g)平衡常数的变化趋势是;1040℃时,该反应的化学平衡常数的数值是。 -
(3) ①古老而神奇的蓝色染料普鲁士蓝的合成方法如下:

复分解反应ii的离子方程式是。
②如今基于普鲁士蓝合成原理可检测食品中CN- , 方案如下:
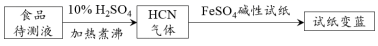
若试纸变蓝则证明食品中含有CN- , 请解释检测时试纸中FeSO4的作用。
-
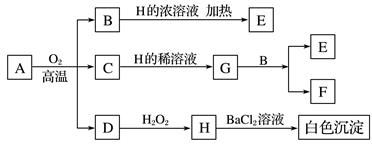
(1) 化合物A的化学式:。
-
(2) 检验气体D的实验方法:。
-
(3) 写出B与H浓溶液反应的化学方程式:。
-
(4) 写出A在氧气中充分煅烧的化学方程式:。
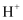 )=0.1mol∙L-1的溶液中:
)=0.1mol∙L-1的溶液中:  、
、 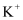 、
、  、
、 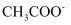 B .
B .  =10-12的溶液中:
=10-12的溶液中:  、
、 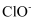 、
、 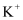 、
、  C . c(
C . c(  )=0.1mol∙L-1的溶液中:
)=0.1mol∙L-1的溶液中: 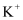 、
、 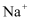 、
、  、
、  D . 加入KSCN显血红色的澄清透明溶液中:
D . 加入KSCN显血红色的澄清透明溶液中: 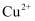 、
、 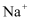 、
、  、
、 
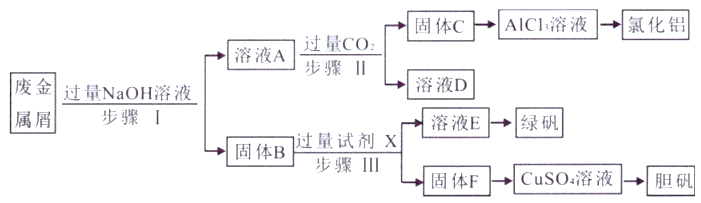
请回答:
-
(1) 写出步骤Ⅰ反应的离子方程式:、。
-
(2) 试剂X是,溶液D是。
-
(3) 在步骤Ⅱ时,用如图装置制取CO2并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可采取的改进措施是。
-
(4) 由固体F制取硫酸铜溶液,通常有两种方案:
方案一:将固体F在加热条件下与浓硫酸反应;
方案二:将固体F投入热的稀硫酸中,然后不断鼓入空气。
方案一的缺点为:。
请写出方案二中发生反应的化学方程式:。
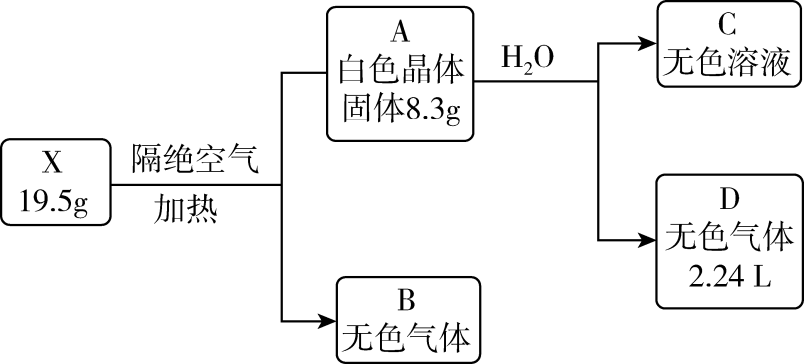
已知:B是空气的主要成分之一;A与H2O反应属于非氧化还原反应,且C是一种强碱;D遇湿润的红色石蕊试纸变蓝。
-
(1) X的组成元素为。
-
(2) B的组成元素在元素周期表中的位置是。
-
(3) 写出C的电子式为。
-
(4) X受热分解转变成A和B的化学方程式为。
- 中国古代专制皇权不断加强,中枢权力体系也发生相应的变化。下列表述符合史实的是 A.汉武帝时建立的“中朝”决策机构,废除了
- 细胞核内DNA分子数和染色体数相同的细胞是 A.刚刚形成的次级精母细胞 B.初级
- 材料一 公元前356年,秦国任用商鞅变法。变法明确规定:“僇(lù)力本业(努力搞好农业),耕绢致粟帛多者,复其身(免
- 逻辑推理是化学学习中常用的一种思维方法,以下推理中正确的是 A.酸碱中和反应生成盐和水,则生成盐和水的反应一定是中和反应
- 关于天然放射现象,下列说法正确的是A.放射性元素的原子核内的核子有半数发生变化所需的时间就是半衰期B.放射性物质放出的射
- 下图是细胞有丝分裂示意图,据图回答:(1)图1中的A图表示的是________细胞进行有丝分裂的________期。此期
- 三个互不重合的平面把空间分成六个部份时,它们的交线有 ( )
- 近十几年来,我国蝗灾加重趋势的原因主要有( ) ①气候异常 ②蝗虫天敌减少 ③生态环境恶化 ④农药的使用太少 A.①
- 《大公报》载文说:“几千年来,中国人所怀抱的观念是‘天下',是‘家族',近代西方的民族意识和国家观念,始终没有打入我们老
- 阅读下面的文字,完成下面小题。 特别的礼物 郁葱译 早上,阿尔琼被收音机定时的7点新闻闹醒。他摸着旁边空空的枕头
- 某一个个体的基因型为AABbDdFf,这些基因分别位于4对同源染色体上,问此个体能产生配子的类型为( ) A、4
- 如下图,某几何体的主视图与左视图都是边长为1的正方形,且其体积为. 则该几何体的俯视图可以是
- 消化淀粉的消化液是由下列哪些腺体分泌的( ) ①唾液腺 ②胃腺 ③肝脏 ④肠腺 ⑤胰腺 A.①④⑤
- 下列关于原子的说法中,正确的是( )A.原子不显电性,说明原子内的质子数等于中子数B.同种原子内的质子数相同C.含
- “过去我们从书本上或从其他资料里面也都了解到,埃及是世界上的文明古国,但是到实地去看一看以后,感受还是不一样
- Rich or poor, we all have problems: that unfaithful mate, th
- Copernicus was born in Torun,Poland,onFebruary 19,1473.Littl
- 科学家用枪乌贼的神经细胞研究钠离子通过细胞膜的运输方式,实验如下: 实验方法 现象 ① 向枪乌贼的神经细胞内注入微量的放
- ---You’ve made great progress in your studies of English, ha
- p{font-size:10.5pt;line-height:150%;margin:0;padding:0;}td{f



